กลุ่มอาการแอนตัน (Anton Syndrome) เป็นภาวะที่ผู้ป่วยที่มีภาวะตาบอดจากสมองส่วนการเห็น (cortical blindness) ไม่รับรู้ถึงการสูญเสียการมองเห็น ของตนเอง และเล่าประสบการณ์ทางการเห็นที่ไม่มีอยู่จริง ซึ่งเรียกว่า visual anosognosia (การไม่รับรู้ความบกพร่องทางการเห็น) ผู้ป่วยแม้จะตาบอดแต่ยังพยายามอธิบายรายละเอียดสิ่งที่พวกเขา “เห็น” โดยการสร้างเรื่องขึ้นมา (confabulation)
โรคนี้ตั้งชื่อตาม Gabriel Anton นักประสาทวิทยาชาวออสเตรีย ซึ่งรายงานผู้ป่วยอายุ 69 ปีที่มีภาวะไม่รับรู้ความบกพร่อง (acquired anosognosia) และหูหนวกจากรอยโรคที่สมองกลีบขมับทั้งสองข้าง คำว่า “anosognosia” (การไม่รับรู้ความบกพร่อง) ถูกบัญญัติโดย Joseph Babinski ดังนั้นจึงมีอีกชื่อว่า “Anton-Babinski syndrome” บันทึกแรกของ visual anosognosia ย้อนไปถึงทาสชาวโรมันชื่อ Harpaste ซึ่งปฏิเสธว่าตนเองตาบอดและบ่นว่าห้องมืด
ความแตกต่างจากกลุ่มอาการชาร์ลส์ บอนเน็ต ควรให้ความสำคัญ กลุ่มอาการชาร์ลส์ บอนเน็ตคือผู้ป่วยที่มีความบกพร่องทางการมองเห็น มีภาพหลอน แต่ยังคงมีความเข้าใจในความบกพร่องทางการมองเห็น ของตนเอง ซึ่งแตกต่างโดยพื้นฐานจากกลุ่มอาการแอนตัน
ระบาดวิทยา อายุมัธยฐานคือ 55 ปี (ช่วง 6-96 ปี) และไม่มีความแตกต่างทางเพศ กรณีส่วนใหญ่เกิดจากโรคหลอดเลือดสมอง (CVA) และพบมากในผู้สูงอายุที่มีปัจจัยเสี่ยงต่อหลอดเลือดหลายประการ โรคหลอดเลือดสมองในสมองส่วนหลัง (PCA) คิดเป็น 5-10% ของโรคหลอดเลือดสมองทั้งหมด 1) ระหว่างปี 1965-2016 มีรายงานกลุ่มอาการแอนตัน-บาบินสกีเพียง 28 ราย ซึ่งเป็นโรคที่หายากมาก 2)
Q
กลุ่มอาการแอนตันและกลุ่มอาการชาร์ลส์ บอนเน็ตแตกต่างกันอย่างไร?
A
กลุ่มอาการแอนตันคือผู้ป่วยตาบอดจากสมองส่วนหลังที่ปฏิเสธการตาบอดของตนเองและสร้างเรื่องขึ้นมา โดยขาดความเข้าใจ ในขณะที่กลุ่มอาการชาร์ลส์ บอนเน็ตคือผู้ป่วยที่มีความบกพร่องทางการมองเห็น มีภาพหลอน แต่ยังคงมีความเข้าใจในความบกพร่องทางการมองเห็น ของตนเอง ทั้งสองมีพื้นฐานจากความบกพร่องทางการมองเห็น แต่แตกต่างกันโดยพื้นฐานในเรื่องการมีหรือไม่มีภาวะไม่รู้โรค
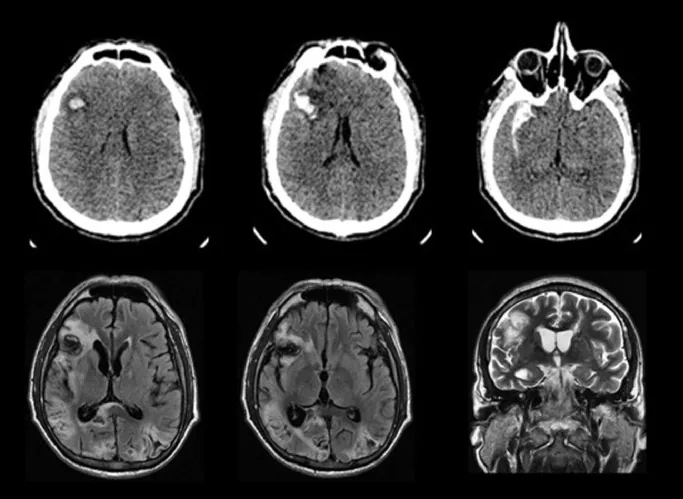
ภาพ CT/MRI ของภาวะสมองขาดเลือดในกลีบท้ายทอยทั้งสองข้างซึ่งเป็นสาเหตุของกลุ่มอาการแอนตัน Ricardo BM, et al. Anton syndrome after subarachnoid hemorrhage and delayed cerebral ischemia: A case report. Cereb Circ Cogn Behav. 2021. Figure 1. PM
CI D: PMC9616440. License: CC BY.
ภาพ CT แสดงเลือดออกและก้อนเลือดในกลีบหน้าผากด้านขวา ส่วนภาพ FLAIR และ T2-weighted ของ MRI แสดงภาวะสมองขาดเลือดร่วมกับเลือดออกในกลีบท้ายทอยทั้งสองข้าง ซึ่งสอดคล้องกับภาวะสมองขาดเลือดในกลีบท้ายทอยทั้งสองข้างที่กล่าวถึงในหัวข้อ “2. อาการหลักและผลการตรวจทางคลินิก”
การปฏิเสธการสูญเสียการมองเห็น : ผู้ป่วยไม่รับรู้ถึงการสูญเสียการมองเห็น ของตนเอง เมื่อชนวัตถุ มักจะโทษปัจจัยภายนอก เช่น ห้องมืดการสร้างเรื่อง : อธิบายรายละเอียดเกี่ยวกับบุคคลหรือสถานการณ์ที่ไม่มีอยู่จริง เมื่อถูกขอให้จับมือ จะยื่นมือไปผิดทิศทางการคงไว้ของการมองเห็น สีบางส่วน : การมองเห็น สีอาจคงอยู่ได้ สามารถรับรู้สิ่งของที่เคลื่อนไหวได้ แต่ยากต่อการรับรู้สิ่งของที่อยู่นิ่ง เกิดจากวิถีประสาทใต้คอร์เทกซ์ที่บริเวณ V5 ผ่าน V1 1)
การมองเห็น รีเฟล็กซ์รูม่านตา : ปกติ เนื่องจากรอยโรคที่สมองกลีบท้ายทอยอยู่ด้านหลัง lateral geniculate body จึงไม่ส่งผลต่อทางเดินของรูม่านตา ทางเดินนำเข้าของรีเฟล็กซ์ต่อแสงจะไปยัง pretectal area ของสมองส่วนกลางก่อนถึง lateral geniculate bodyการตรวจอวัยวะภายในลูกตา : ปกติ ไม่พบความผิดปกติทางโครงสร้างภายในลูกตา 1) รีเฟล็กซ์กระพริบตาต่อสิ่งคุกคาม : ไม่มีการเคลื่อนไหวของลูกตา : ปฏิบัติตามคำสั่งด้วยวาจาได้ปกติ แต่ไม่สามารถติดตามด้วยสายตาได้รีเฟล็กซ์กระจกตา : ปกติ (ไม่ขึ้นกับอินพุตจากคอร์เทกซ์)การตรวจลานสายตา 1) ปรากฏการณ์ Riddoch : ไม่สามารถรับรู้วัตถุที่อยู่นิ่งได้ แต่สามารถรับรู้วัตถุที่เคลื่อนไหวได้ เป็นปรากฏการณ์ที่ Riddoch รายงานในปี 1917 และเป็นลักษณะหนึ่งของ cortical blindnessการมองเห็น โดยไม่รู้ตัว (blindsight)การมองเห็น อื่นนอกเหนือจากวิถี LGB-V1 (เช่น V2, V3, V4, V5/MT, FST, LIP)
Q
เหตุใดผู้ป่วย cortical blindness จึงยังคงมีรีเฟล็กซ์รูม่านตาต่อแสงปกติ?
A
วิถีประสาทนำเข้าของรีเฟล็กซ์รูม่านตา ต่อแสงจะไปยังบริเวณ pretectum ของสมองส่วนกลางก่อนถึง lateral geniculate body (LGB) และไม่ผ่าน occipital lobe (visual cortex แรก) ดังนั้นแม้ occipital lobe จะเสียหาย รีเฟล็กซ์รูม่านตา ต่อแสงก็ยังคงอยู่ เมื่อรวมกับผลตรวจอวัยวะภายในตาที่ปกติ จึงเป็นลักษณะเด่นของ cortical blindness
สาเหตุหลักและปัจจัยเสี่ยงที่เกี่ยวข้องของกลุ่มอาการแอนตันมีดังนี้
สาเหตุจากหลอดเลือด
ภาวะสมองขาดเลือดใน PCA ทั้งสองข้าง : สาเหตุที่พบบ่อยที่สุด เกิดจากกล้ามเนื้อสมองตายในหลอดเลือดสมองส่วนหลังทั้งสองข้าง ทำให้สมองกลีบท้ายทอยถูกทำลายอย่างกว้างขวาง
หลังการบาดเจ็บหรือเนื้องอก : อาจเกิดขึ้นหลังการบาดเจ็บที่ศีรษะ เนื้องอกในสมอง หรือการผ่าตัด
การผ่าตัดหัวใจและการตรวจหลอดเลือดสมองด้วยสารทึบรังสี : เป็นปัจจัยเสี่ยงที่เกิดจากทางการแพทย์
พิษจากคาร์บอนมอนอกไซด์และกลุ่มอาการPRES : อาจเกิดจากพิษและกลุ่มอาการสมองส่วนหลังที่สามารถกลับคืนได้ (PRES) ยาเคมีบำบัดเช่นซิสพลาตินก็เป็นสาเหตุได้
สาเหตุที่ไม่เกี่ยวกับหลอดเลือด
MELAS : โรคกล้ามเนื้อและสมองจากไมโตคอนเดรีย มีรายงานการเกิดในผู้ป่วยที่มีการกลายพันธุ์ mt.3243A>G 2)
การกำเริบของ MS , ภาวะครรภ์เป็นพิษ, ภาวะเลือดออกทางสูติกรรม : เกิดตามหลังภาวะทางระบบต่างๆ
โรคติดเชื้อ : โรคสมองอักเสบจากไวรัสเวสต์ไนล์ (WNV), PML ที่เกี่ยวข้องกับ HIV เป็นต้น 3)
อื่นๆ : โรคเม็ดเลือดขาวผิดปกติต่อมหมวกไต, หลอดเลือดอักเสบในระบบประสาทส่วนกลาง, ภาวะขาดเลือดที่เกิดจากเลือดออกใต้เยื่อหุ้มสมองชั้นกลาง, รอยโรคที่รังสีแก้วตาทั้งสองข้างในกลุ่มอาการทรูโซ เป็นต้น
ลักษณะทางกายวิภาคของหลอดเลือดสมองส่วนหลัง (PCA) คือ แยกจากหลอดเลือดเบซิลาร์ ส่วนต้น (P1–P2) เลี้ยงโครงสร้างส่วนลึก (ทาลามัสส่วนหลังและสมองส่วนกลาง) ส่วนปลาย (P3–P4) เลี้ยงคอร์เทกซ์สมองกลีบท้ายทอย การบาดเจ็บของเซกเมนต์ P4 เป็นสาเหตุหลักของความบกพร่องลานสายตา 1) คอร์เทกซ์ท้ายทอยอยู่ห่างจากระบบหลอดเลือดส่วนกลางและมีโครงสร้างที่เสี่ยงต่อภาวะขาดเลือด
สาเหตุหลักของกลุ่มอาการแอนตันคือโรคหลอดเลือดสมอง การควบคุมปัจจัยเสี่ยงต่อหลอดเลือดสมอง เช่น ความดันโลหิตสูง เบาหวาน ไขมันในเลือดผิดปกติ และการสูบบุหรี่อย่างเหมาะสมเป็นพื้นฐานของการป้องกัน หากมีอาการสูญเสียการมองเห็น กะทันหัน ปวดศีรษะ หรืออัมพาตครึ่งซีก ควรรีบไปพบแพทย์ฉุกเฉินทันที
Q
กลุ่มอาการแอนตันสามารถเกิดขึ้นได้จากสาเหตุอื่นนอกจากโรคหลอดเลือดสมองหรือไม่?
A
กลุ่มอาการแอนตันอาจเกิดจากสาเหตุที่ไม่เกี่ยวกับหลอดเลือดได้หลากหลาย เช่น MELAS (โรคไมโตคอนเดรีย เอนเซ็ฟฟาโลไมโอพาธี) 2) MS (โรคปลอกประสาทเสื่อมแข็ง) โรคสมองอักเสบจากไวรัสเวสต์ไนล์ 3) การบาดเจ็บ และพิษจากคาร์บอนมอนอกไซด์ สาเหตุทั้งหมดนี้มีพื้นฐานทางพยาธิวิทยาร่วมกันคือความผิดปกติของสมองกลีบท้ายทอยทั้งสองข้าง
การวินิจฉัยทางคลินิกทำได้โดยการรวม 4 ปัจจัย ได้แก่ ประวัติการเล่าเรื่องเท็จ การพิสูจน์ทางคลินิกว่าสูญเสียการมองเห็น ผลการตรวจอวัยวะภายในตาปกติ และการยืนยันรอยโรคที่สมองกลีบท้ายทอยด้วยภาพ
CT scan ศีรษะ (NCCT) : มีประโยชน์ในการประเมินฉุกเฉิน ใช้ยืนยันภาวะสมองขาดเลือด (บริเวณความหนาแน่นต่ำ) ตัวอย่างเช่น แสดงเป็นภาวะสมองขาดเลือดที่สมองกลีบขมับและท้ายทอยด้านขวา 1) MRI ศีรษะ :
ในระยะเฉียบพลันมาก (ภายใน 6 ชั่วโมง) DWI มีประโยชน์ แม้ในระยะเฉียบพลันที่ตรวจพบได้ยากด้วย T1, T2, FLAIR ก็สามารถตรวจพบได้ด้วย DWI
ภาพ FLAIR มีความสามารถในการแยกแยะระหว่างเนื้อสมองขาดเลือดและน้ำไขสันหลังได้ดี
ตรวจหาบริเวณสัญญาณสูงในคอร์เทกซ์กลีบท้ายทอยและเนื้อขาวใต้คอร์เทกซ์ในภาพ T2-FLAIR 2) 3)
การตีความผล DWI : สัญญาณ DWI สูงร่วมกับสัญญาณ ADC ปกติ (ไม่ลดลง) บ่งชี้ถึงการเปลี่ยนแปลงจากอาการชัก และแตกต่างจากโรคหลอดเลือดสมองขาดเลือด (ซึ่งมีค่า ADC ลดลง) 2)
VEP (ศักย์ไฟฟ้าที่เกิดจากการมองเห็น )V-EEG (คลื่นไฟฟ้าสมองร่วมกับวิดีโอ) : มีประโยชน์เมื่อสงสัยอาการชักในโรคเช่น MELAS สามารถตรวจจับอาการชักที่เกิดจากสมองกลีบท้ายทอยได้ 2)
โรคที่ควรแยกและการวินิจฉัยแยกโรคมีดังนี้
โรค จุดที่ใช้แยกโรค กลุ่มอาการชาร์ลส์ บอนเน็ต เห็นภาพหลอน รักษาความตระหนักรู้ (ไม่มีภาวะไม่รู้โรค) ภาวะสมองเสื่อม ภาวะไม่รู้โรคทางปัญญา การสร้างเรื่องเท็จจากความจำบกพร่อง กลุ่มอาการเวอร์นิค-คอร์ซาคอฟ ขาดไทอามีน・ความจำทันทีคงอยู่ การแสร้งป่วย VEP แสดงการทำงานของการมองเห็น ส่วนกลางปกติความบกพร่องทางการมองเห็นจากสาเหตุทางจิตใจ ปฏิกิริยารูม่านตา และการเคลื่อนไหวของลูกตาปกติ (เหมือนกับ cortical blindness) จำเป็นต้องได้รับการประเมินทางจิตเวช
การแยกจากความบกพร่องทางการมองเห็นจากสาเหตุทางจิตใจ มีความสำคัญเป็นพิเศษ เนื่องจาก cortical blindness ที่เกิดจากความเสียหายของสมองกลีบท้ายทอยทั้งสองข้างไม่มีความผิดปกติของลูกตาและปฏิกิริยารูม่านตา ยังคงอยู่ จึงมักถูกเข้าใจผิดว่าเป็นโรคทางจิตหรือการแกล้งป่วย
การรักษา Anton syndrome ขึ้นอยู่กับสาเหตุที่สงสัยว่าทำให้เกิดรอยโรคที่สมองกลีบท้ายทอย การรักษาที่สาเหตุเป็นพื้นฐาน
tPA ทางหลอดเลือดดำ (tissue plasminogen activator) : เหมาะสมหากภายใน 4.5 ชั่วโมงหลังเริ่มมีอาการ การละลายลิ่มเลือดช่วยป้องกันการขยายตัวของบริเวณที่ขาดเลือด 1) การรักษาทางหลอดเลือด : ในระยะเฉียบพลันมาก อาจพิจารณาการรักษาด้วยสายสวนหลอดเลือด (การนำลิ่มเลือดออก)กรณีเกิน 4.5 ชั่วโมงหลังเริ่มมีอาการ : เปลี่ยนโฟกัสไปที่การป้องกันโรคหลอดเลือดสมองเพิ่มเติมและการฟื้นฟูสมรรถภาพ 1)
ยาต้านเกล็ดเลือด
แอสไพริน : 75–150 มก./วัน (ระดับ A)
โคลพิโดเกรล : 75 มก./วัน (ระดับ A)
ซิโลสตาโซล : 200 มก./วัน (ระดับ B)
ไทโคลพิดีน : 200 มก./วัน (ระดับ B)
การรักษาป้องกันอื่นๆ
ยาต้านการแข็งตัวของเลือด : เช่น วาร์ฟาริน ใช้ในกรณีที่เกิดจากลิ่มเลือดอุดตันจากหัวใจ (เช่น ภาวะหัวใจห้องบนสั่นพลิ้ว)
การรักษาด้วยสแตติน : การจัดการภาวะไขมันในเลือดผิดปกติและการป้องกันการเกิดโรคหลอดเลือดสมองซ้ำ
การควบคุมปัจจัยเสี่ยง : การทำให้ความดันโลหิตสูง น้ำตาลในเลือดสูง และภาวะไขมันในเลือดผิดปกติกลับสู่ปกติ รวมถึงการเลิกสูบบุหรี่
ที่มาจาก MS : การบำบัดด้วยสเตียรอยด์ แบบพัลส์ (IV methylprednisolone) + การแลกเปลี่ยนพลาสมา มีรายงานผู้ป่วยที่ฟื้นตัวอย่างค่อยเป็นค่อยไปในช่วง 2 ปี โดยเริ่มจากการฟื้นฟูการรับรู้ ตามด้วยการฟื้นฟูการมองเห็น ที่มาจาก MELAS : การปรับยาต้านโรคลมชัก ให้เหมาะสม (ปรับขนาด lorazepam และ levetiracetam เพิ่ม lacosamide) + การบำบัดเสริม (L-arginine, levocarnitine, วิตามิน C, B1, B2, B12) 2) ที่มาจากสมองอักเสบ WNV : มีรายงานผู้ป่วยที่ได้รับ methylprednisolone 1000 มก./วัน เป็นเวลา 7 วัน แต่ไม่ตอบสนอง ยังไม่มีการรักษาที่เป็นมาตรฐาน 3)
Q
ระยะเวลาตั้งแต่เริ่มมีอาการนานเท่าใดจึงมีความสำคัญต่อการรักษา?
A
ในกรณีที่เกิดจากโรคหลอดเลือดสมอง หากมาภายใน 4.5 ชั่วโมงหลังจากเริ่มมีอาการ จะมีข้อบ่งชี้ในการให้ tPA (การละลายลิ่มเลือด) 1) หากเกินเวลานี้ การป้องกันการเกิดซ้ำและการฟื้นฟูสมรรถภาพจะเป็นแกนหลักของการรักษา ยิ่งมีเวลาเหลือมากเท่าใด ขอบเขตของเซลล์ประสาทที่สามารถช่วยเหลือได้ก็ยิ่งกว้างขึ้น ดังนั้นเมื่อมีอาการเกิดขึ้น ควรรีบไปพบแพทย์ที่ห้องฉุกเฉินทันที
ความเสียหายแบบกว้างทั้งสองข้างของสมองกลีบท้ายทอย (visual cortex ปฐมภูมิ V1) ทำให้เกิด hemianopia เหมือนกันทั้งสองข้าง และในที่สุดนำไปสู่ cortical blindness. เยื่อหุ้มสมองกลีบท้ายทอยอยู่ห่างจากระบบหลอดเลือดส่วนกลางและมีโครงสร้างที่เปราะบางต่อการขาดเลือด. ภาวะกล้ามเนื้อตายของส่วนปลายของหลอดเลือดสมองส่วนหลัง (P3–P4) ทำให้เลือดไปเลี้ยงกลีบท้ายทอยหยุดชะงัก. 1)
การประมวลผลข้อมูลการเห็นมีวิถีทางหน้าท้อง (วิถี “อะไร”: บริเวณ V4 การรับรู้รูปร่างและสี) และวิถีทางหลัง (วิถี “ที่ไหน”: บริเวณ V5 ตำแหน่งในอวกาศและการเคลื่อนไหว). เส้นใยใต้เยื่อหุ้มสมองบางส่วนข้าม V1 ไปเชื่อมต่อโดยตรงกับ V4 และ V5 ดังนั้นแม้ V1 จะเสียหายอย่างกว้างขวาง วิถีทางเหล่านี้อาจยังคงทำงาน ทำให้สามารถคงการรับรู้สีและการตรวจจับการเคลื่อนไหวได้ในบางกรณี. 1) นี่คือพื้นฐานทางประสาทวิทยาของปรากฏการณ์ Riddoch (มองเห็นสิ่งที่เคลื่อนไหวได้).
盲視(blindsight)のメカニズムとしては、macaque monkeyを用いた研究でLGBdからV2・V3・V4・V5/MT野・FST・LIPへの直接投射経路が報告されており、この経路が意識下の視覚反応を説明する可能性がある。
病態失認の機序については複数の仮説が存在する。
仮説 内容 根拠 視覚野+連合野の同時損傷 一次視覚野と視覚連合野が同時に障害され、自己状態への洞察が欠如する 後頭葉広汎病変の臨床像 離断症候群(disconnection) 頭頂葉白質病変により視覚野と他領域が断絶する 白質病変を伴う症例での発症 言語中枢との連結異常 障害された視覚野と機能している言語領域の接続が断絶し、言語領域が視覚入力なしに作話的回答を生成する 作話の内容が視覚的詳細を含む点
現在、「言語中枢との連結異常」説が最も支持されている。損傷した視覚野から言語野へのフィードバックが途絶えることで、言語野が「見えている」という虚偽の報告を生成すると考えられている。
Q
なぜ患者は見えていないのに見えていると主張するのか?
A
最も支持されている仮説は「言語中枢との連結異常」説である。後頭葉の損傷により視覚野から言語野へのフィードバック回路が断絶し、言語野は視覚入力なしに「見えている」という作話的な回答を生成するとされる。これは意図的な嘘ではなく、脳の回路損傷に起因する神経学的な現象である。
MELASにおける機序 :小細動脈の内皮・平滑筋細胞に異常ミトコンドリアが蓄積し、毛細血管増殖を来す。てんかん発作が神経血管単位の急速なエネルギー枯渇を引き起こし、Todd麻痺様の病態へと至る。Fryer仮説では「てんかん発作がstroke-like episodeの引き金になる」と提唱されている。2)
WNV脳炎における血液脳関門(BBB)通過機序 :受動的細胞輸送、軸索輸送、炎症誘発性BBB破壊の3つの経路が想定されている。3)
Ziaul ら(2024)の症例報告では、COVID-19患者は虚血性脳卒中リスクが3.6倍に増加し、軽症COVID-19でも脳卒中リスクが約1%に上昇することが報告された。1) 高い炎症反応、過凝固状態、医学的重症度が血栓塞栓症の素因となるとされる。PCAを含む後方循環系の脳卒中においても、パンデミック中に遅延受診が問題となった。
Ewida ら(2021)はMELAS合併アントン-Babinski症候群の症例で、DWI高信号かつADC等信号(虚血性変化とは不一致)という特徴的なMRI所見を報告した。2) この所見は虚血性脳卒中のDWI変化(ADC低下を伴う)と異なり、てんかん発作による可逆的なエネルギー代謝障害と血行動態変化の組合せと解釈される。DWI所見の鑑別はMELASにおける治療方針決定に重要な示唆を与える。
Srichawla(2022)は、神経浸襲型WNV感染症に対してインターフェロンαおよびWNV抗体を含む精製免疫グロブリン製剤が将来の治療候補となりうると報告した。3) 現時点ではメチルプレドニゾロンを含む既存薬への反応は乏しく、確立された治療法は存在しない。WNV感染の80%超は無症候であるが、5%未満が神経浸襲型へと進行するとされ、治療法の確立が急務である。
Ziaul YH, Mittal J, Afroze T, et al. Anton-Babinski Syndrome: A Visual Anosognosia. Cureus. 2024;16(3):e55679.
Ewida A, Ahmed R, Luo A, et al. Mitochondrial Myopathy, Encephalopathy, Lactic acidosis and Stroke-Like Episodes Syndrome Presenting With Anton-Babinski Syndrome and Concurrent Occipital Lobe Seizures. Cureus. 2021;13(1):e12908.
Srichawla BS. Neuroinvasive West Nile Virus (WNV) Encephalitis With Anton Syndrome: Epidemiology and Pathophysiology Review. Cureus. 2022;14(6):e26264.
ถาม AI เกี่ยวกับบทความนี้
คัดลอกข้อความบทความแล้ววางในผู้ช่วย AI ที่คุณต้องการใช้
เปิดผู้ช่วย AI ด้านล่าง แล้ววางข้อความที่คัดลอกลงในช่องแชต