Giai đoạn 1
Thay đổi biểu mô sắc tố võng mạc (RPE) cạnh trung tâm: Xuất hiện các thay đổi sắc tố dạng chấm hoặc mảng trong RPE.
Thị lực và triệu chứng chủ quan: Thường bình thường.

Bệnh loạn dưỡng hắc mạc trung tâm hình vòng (Central Areolar Choroidal Dystrophy; CACD) là một bệnh loạn dưỡng hoàng điểm di truyền gây teo võng mạc-hắc mạc ranh giới rõ ở vùng hoàng điểm. Tần suất mắc bệnh thấp (khoảng 1/100.000 người) và được xếp vào bệnh hiếm.
Bệnh thường khởi phát ở độ tuổi 20–50. Kiểu di truyền chủ yếu là trội nhiễm sắc thể thường (AD), nhưng cũng có báo cáo về thể lặn nhiễm sắc thể thường (AR) và thể lẻ tẻ.
Gen gây bệnh phổ biến nhất là PRPH2 (nhiễm sắc thể 17p13), mã hóa protein peripherin-2. Peripherin-2 cần thiết cho sự hình thành và ổn định đĩa của đoạn ngoài tế bào cảm thụ ánh sáng. Bất hoạt một alen (haploinsufficiency) được cho là cơ chế chính.
CACD có sự tương đồng về kiểu hình với các bệnh do đột biến gen ABCA4 (như bệnh Stargardt) 1), do đó xét nghiệm gen rất quan trọng để chẩn đoán phân biệt. Không có báo cáo về biến chứng toàn thân.
AMD thường khởi phát sau 60 tuổi và thường kèm theo drusen và các thay đổi xuất tiết. CACD khởi phát ở tuổi trẻ đến trung niên, với teo ranh giới rõ và không có drusen. Nếu xét nghiệm gen phát hiện đột biến PRPH2, có thể chẩn đoán CACD.
Triệu chứng chính là ám điểm trung tâm hai bên (khó nhìn phần trung tâm). Giảm thị lực có thể xảy ra sớm, nhưng trong một số trường hợp, thị lực vẫn tương đối tốt cho đến giai đoạn muộn.
Tổn thương hoàng điểm đối xứng hai bên, được phân loại thành 4 giai đoạn. Thần kinh thị giác, mạch máu võng mạc và võng mạc ngoại vi được bảo tồn. Kích thước vùng teo khoảng 2-4 lần đường kính gai thị (DD).
Giai đoạn 1
Thay đổi biểu mô sắc tố võng mạc (RPE) cạnh trung tâm: Xuất hiện các thay đổi sắc tố dạng chấm hoặc mảng trong RPE.
Thị lực và triệu chứng chủ quan: Thường bình thường.
Giai đoạn 2
Teo giảm sắc tố ranh giới không rõ: Vùng teo nhạt xuất hiện bên ngoài trung tâm.
Mở rộng thay đổi RPE: Teo với ranh giới chưa rõ ràng được ghi nhận.
Giai đoạn 3
Teo RPE ranh giới rõ: Vùng teo với ranh giới rõ hình thành bên ngoài trung tâm.
Bảo tồn trung tâm: Ở giai đoạn này, trung tâm (fovea) còn, thị lực tương đối được bảo tồn.
Giai đoạn 4
Teo hoàn toàn bao gồm hố trung tâm: Vùng teo mở rộng bao gồm hố trung tâm và toàn bộ điểm vàng.
Suy giảm thị lực nghiêm trọng: Mất diện rộng các mao mạch hắc mạc, tế bào cảm thụ ánh sáng và RPE gây giảm thị lực trầm trọng.
Tốc độ tiến triển khác nhau rất nhiều giữa các cá nhân. Nhìn chung, diễn tiến chậm, và một số trường hợp mất nhiều thập kỷ để đạt đến giai đoạn 4. Tuy nhiên, tốc độ tiến triển có thể khác nhau tùy theo kiểu gen, và việc đánh giá nhãn khoa định kỳ là rất cần thiết. mfERG được mô tả chi tiết trong phần «Chẩn đoán và Phương pháp Xét nghiệm» là một chỉ số của tiến triển sớm.
Nguyên nhân chính của CACD là đột biến gen PRPH2. PRPH2 mã hóa periferin-2, có chức năng trong việc hình thành và ổn định các đĩa của đoạn ngoài tế bào cảm thụ ánh sáng. Các đột biến ngăn cản duy trì cấu trúc đoạn ngoài bình thường của tế bào cảm thụ ánh sáng.
Vì là di truyền trội trên nhiễm sắc thể thường (AD), xác suất truyền gen đột biến từ cha mẹ sang con là 50%. Nếu có tiền sử gia đình, nên tư vấn di truyền.
Các yếu tố nguy cơ mắc phải hoặc yếu tố lối sống thúc đẩy khởi phát hoặc tiến triển bệnh hiện chưa được xác định rõ ràng.
CACD chủ yếu là di truyền trội trên nhiễm sắc thể thường, và nguy cơ di truyền cho con của bệnh nhân lên tới 50%. Đột biến có thể được xác định bằng xét nghiệm di truyền, cho phép chẩn đoán xác định và sàng lọc gia đình. Ngoài ra, vì nó có thể là mục tiêu của liệu pháp gen trong tương lai, việc ghi nhận đột biến là quan trọng.
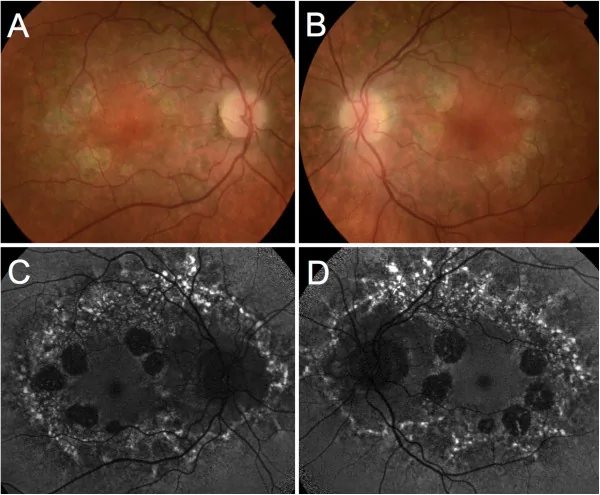
Sử dụng đèn khe và kính soi đáy mắt, xác nhận vùng teo rõ ràng ở hoàng điểm. Đánh giá sự lộ mạch mạch máu hắc mạc hoặc sắc tố.
Kết quả của mỗi xét nghiệm khác nhau tùy theo giai đoạn bệnh. Bảng dưới đây trình bày các kết quả đặc trưng theo từng giai đoạn.
| Xét nghiệm | Kết quả sớm | Kết quả giai đoạn tiến triển |
|---|---|---|
| FAF (Huỳnh quang tự phát đáy mắt) | Tăng huỳnh quang | Mất huỳnh quang (vùng teo) |
| FA (Chụp mạch huỳnh quang) | Tăng huỳnh quang cạnh hố trung tâm | Lấp đầy xuyên thấu ở vùng teo |
| OCT | Dày POS-RPE | Mất lớp ngoài (tế bào cảm quang và RPE) |
Cần phân biệt với các bệnh có teo hoàng điểm tương tự.
| Bệnh cần phân biệt | Điểm phân biệt |
|---|---|
| Thoái hóa hoàng điểm tuổi già (AMD) thể teo | Drusen, ranh giới không đều, khởi phát ở tuổi cao |
| Bệnh Stargardt | Hắc mạc tối, đột biến ABCA4 |
| Loạn dưỡng tế bào nón | Giảm rõ rệt đáp ứng tế bào nón trên ERG, sợ ánh sáng là triệu chứng chính |
Hiện tại chưa có phương pháp điều trị xác định cho CACD. Điều trị nhằm kiểm soát triệu chứng và duy trì chất lượng cuộc sống.
Phục hồi chức năng thị lực kém
Kính lúp và kính chống chói: Kê đơn các dụng cụ hỗ trợ để tận dụng tối đa chức năng thị giác còn lại.
Đào tạo nghề nghiệp và sinh hoạt: Hỗ trợ học các kỹ năng sống hàng ngày thích ứng với khiếm thị.
Tư vấn di truyền
Cung cấp thông tin cho gia đình: Giải thích về di truyền trội trên nhiễm sắc thể thường (nguy cơ di truyền 50%).
Xét nghiệm di truyền: Xác định đột biến rất quan trọng để chẩn đoán xác định và lựa chọn điều trị trong tương lai.
Liệu pháp gen (giai đoạn nghiên cứu)
Ứng cử viên điều trị trong tương lai: Nghiên cứu đang được tiến hành về liệu pháp thay thế gen nhắm vào đột biến PRPH2.
Hiện tại: Chưa thể cung cấp như một phương pháp điều trị đại trà.
Nghiên cứu về liệu pháp gen cho các bệnh võng mạc di truyền liên quan đến PRPH2 đang được đẩy mạnh trên toàn cầu. Tại Vương quốc Anh, một thử nghiệm liệu pháp gen cho chứng loạn dưỡng màng mạch (choroidermia) đã được thực hiện vào năm 2014, và ứng dụng cho các bệnh đột biến PRPH2 cũng đang được nghiên cứu. Tuy nhiên, hiện tại chưa được thiết lập như một phương pháp điều trị tiêu chuẩn và vẫn đang trong giai đoạn nghiên cứu.
Ở vùng teo, các mao mạch màng mạch, biểu mô sắc tố võng mạc và tế bào cảm thụ ánh sáng (hình que và hình nón) biến mất. Số lượng tế bào ở lớp nhân ngoài giảm đáng kể, và màng giới hạn ngoài tiếp xúc trực tiếp với màng Bruch. Các mạch máu màng mạch cỡ vừa và lớn vẫn được bảo tồn trong thời gian dài ngay cả ở giai đoạn tiến triển.
Peripherin-2 khu trú ở rìa của các đĩa đoạn ngoài của tế bào cảm thụ ánh sáng và đóng vai trò thiết yếu trong việc hình thành, ổn định đĩa và duy trì độ cong của rìa.
Khi xảy ra tình trạng thiếu hụt PRPH2 (mất chức năng một bản sao), sự hình thành hình thái bình thường của đoạn ngoài bị suy giảm. Sự phá vỡ cấu trúc của đoạn ngoài tiến triển thành quá trình chết theo chương trình của tế bào cảm thụ ánh sáng, dẫn đến teo thứ phát của biểu mô sắc tố võng mạc và mao mạch màng mạch.
PRPH2 được cho là có chức năng khác nhau ở tế bào hình que và hình nón; trên mô hình chuột knockout PRPH2, người ta báo cáo rằng tế bào hình nón xanh thoái hóa chậm hơn so với các tế bào hình nón khác. Sự khác biệt giữa tế bào hình que và hình nón này được cho là góp phần vào sự đa dạng của kiểu hình lâm sàng của bệnh.
Trên điện võng mạc đa tiêu, sự suy giảm chức năng được phát hiện ngay cả ở vùng cận trung tâm vượt ra ngoài vùng teo có thể nhìn thấy khi khám đáy mắt. Điều này cho thấy các tổn thương CACD lan rộng hơn so với vùng teo nhìn thấy trên lâm sàng.
Các nghiên cứu về liệu pháp thay thế gen và liệu pháp chỉnh sửa gen cho các bệnh võng mạc di truyền liên quan đến đột biến PRPH2 đang được tiến hành trên toàn cầu. Đối với một bệnh liên quan (choroidermia), thử nghiệm lâm sàng liệu pháp gen đầu tiên đã được thực hiện tại Vương quốc Anh vào năm 2014.
Phân tích khả năng gây bệnh của từng đột biến đang được tinh chỉnh cùng với sự tiến bộ của y học gen. Sự phổ biến của giải trình tự toàn bộ exome (WES) đã cải thiện đáng kể độ chính xác chẩn đoán 1), cho phép xác định đột biến ở nhiều bệnh nhân hơn.
PRPH2 được chứng minh có vai trò chức năng khác nhau ở tế bào que và tế bào nón ở cấp độ phân tử. Kiến thức này rất quan trọng để giải thích sự đa dạng kiểu hình (thoái hóa ưu thế ở tế bào que hay tế bào nón) và có thể ảnh hưởng đến việc lựa chọn mục tiêu điều trị trong tương lai.