Stadium 1
Perubahan RPE parafoveal: Perubahan pigmen titik atau bercak pada epitel pigmen retina (RPE).
Penglihatan dan gejala subjektif: Seringkali normal.

Distrofi Koroid Sentral Areolar (Central Areolar Choroidal Dystrophy; CACD) adalah distrofi makula herediter yang menyebabkan atrofi retina-koroid yang jelas batasnya di area makula. Insidensinya rendah (sekitar 1 per 100.000 orang) dan diklasifikasikan sebagai penyakit langka.
Onset paling sering pada usia 20–50 tahun. Pola pewarisan terutama autosomal dominan (AD), namun kasus autosomal resesif (AR) dan sporadis juga dilaporkan.
Gen penyebab yang paling sering adalah PRPH2 (kromosom 17p13), yang mengkode protein periferin-2. Periferin-2 penting untuk pembentukan dan stabilisasi diskus segmen luar fotoreseptor. Haploinsufisiensi (kehilangan fungsi satu alel) dianggap sebagai mekanisme utama.
CACD memiliki kemiripan fenotip dengan penyakit akibat mutasi gen ABCA4 (seperti penyakit Stargardt) 1), sehingga tes genetik penting untuk diagnosis banding. Tidak dilaporkan adanya komplikasi sistemik.
AMD biasanya onset setelah usia 60 tahun dan sering disertai drusen serta perubahan eksudatif. CACD onset lebih muda hingga usia pertengahan, dengan atrofi jelas batas tanpa drusen. Jika ditemukan mutasi PRPH2 pada tes genetik, diagnosis CACD dapat ditegakkan.
Gejala utama adalah skotoma sentral bilateral (sulit melihat bagian tengah). Penurunan tajam penglihatan dapat terjadi sejak dini, namun pada beberapa kasus penglihatan tetap relatif baik hingga stadium lanjut.
Lesi makula simetris bilateral, stadium diklasifikasikan menjadi 4 tahap. Saraf optik, pembuluh darah retina, dan retina perifer tetap utuh. Ukuran area atrofi sekitar 2-4 kali diameter diskus optikus (DD).
Stadium 1
Perubahan RPE parafoveal: Perubahan pigmen titik atau bercak pada epitel pigmen retina (RPE).
Penglihatan dan gejala subjektif: Seringkali normal.
Stadium 2
Atrofi hipopigmentasi batas tidak jelas: Area atrofi pucat muncul di luar fovea.
Perluasan perubahan RPE: Atrofi dengan batas belum jelas terlihat.
Stadium 3
Atrofi RPE batas jelas: Area atrofi dengan batas jelas terbentuk di luar fovea.
Fovea masih utuh: Pada tahap ini, fovea masih ada, penglihatan relatif terjaga.
Stadium 4
Atrofi lengkap yang melibatkan fovea: Area atrofi meluas hingga mencakup fovea dan seluruh makula.
Gangguan penglihatan berat: Hilangnya secara luas kapiler koroid, fotoreseptor, dan RPE menyebabkan penurunan tajam penglihatan.
Kecepatan perkembangan sangat bervariasi antar individu. Umumnya perjalanan penyakit lambat, dan beberapa kasus membutuhkan waktu puluhan tahun untuk mencapai stadium 4. Namun, kecepatan perkembangan dapat berbeda tergantung genotipe, dan evaluasi oftalmologis berkala sangat penting. mfERG yang dijelaskan secara rinci di bagian «Diagnosis dan Metode Pemeriksaan» merupakan indikator perkembangan awal.
Penyebab utama CACD adalah mutasi pada gen PRPH2. PRPH2 mengkode periferin-2, yang berfungsi dalam pembentukan dan stabilisasi cakram segmen luar fotoreseptor. Mutasi menghalangi pemeliharaan struktur segmen luar fotoreseptor yang normal.
Karena merupakan pewarisan autosomal dominan (AD), probabilitas pewarisan gen mutan dari orang tua ke anak adalah 50%. Jika ada riwayat keluarga, konseling genetik dianjurkan.
Faktor risiko didapat atau faktor gaya hidup yang mempercepat onset atau progresi penyakit belum teridentifikasi secara jelas saat ini.
CACD sebagian besar adalah pewarisan autosomal dominan, dan risiko pewarisan pada anak pasien mencapai 50%. Mutasi dapat diidentifikasi melalui tes genetik, memungkinkan diagnosis pasti dan skrining keluarga. Selain itu, karena mungkin menjadi target terapi gen di masa depan, pencatatan mutasi adalah penting.
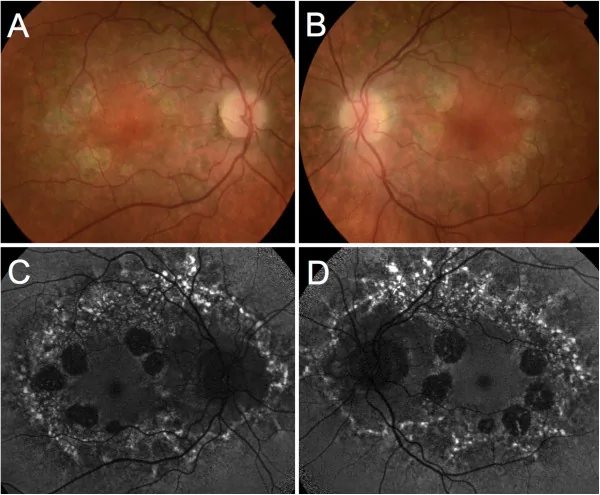
Dengan slit-lamp dan oftalmoskop, konfirmasi area atrofi yang jelas di makula. Evaluasi adanya eksposur pembuluh koroid atau pigmentasi.
Temuan setiap pemeriksaan berbeda tergantung stadium penyakit. Tabel di bawah menunjukkan temuan khas per stadium.
| Pemeriksaan | Temuan Dini | Temuan Lanjut |
|---|---|---|
| FAF (Autofluoresensi Fundus) | Hiperfluoresensi | Hilangnya fluoresensi (area atrofi) |
| FA (Angiografi Fluoresein) | Hiperfluoresensi parafoveal | Pengisian tembus di area atrofi |
| OCT | Penebalan POS-RPE | Hilangnya lapisan luar (fotoreseptor dan RPE) |
Penting untuk membedakan dari penyakit yang menunjukkan atrofi makula serupa.
| Penyakit Banding | Poin Pembeda |
|---|---|
| AMD Atrofi | Drusen, batas tidak teratur, onset usia lanjut |
| Penyakit Stargardt | Koroid gelap, mutasi ABCA4 |
| Distrofi Kerucut | Penurunan respons kerucut ERG yang signifikan, fotofobia sebagai gejala utama |
Saat ini belum ada pengobatan yang pasti untuk CACD. Pengobatan bertujuan untuk mengelola gejala dan mempertahankan kualitas hidup.
Rehabilitasi Low Vision
Kaca pembesar dan kacamata pelindung cahaya: Meresepkan alat bantu untuk memaksimalkan fungsi penglihatan yang tersisa.
Pelatihan pekerjaan dan kehidupan: Membantu mempelajari keterampilan hidup sehari-hari yang sesuai dengan gangguan penglihatan.
Konseling Genetik
Memberikan informasi kepada keluarga: Menjelaskan pewarisan dominan autosomal (risiko pewarisan 50%).
Tes genetik: Identifikasi mutasi penting untuk diagnosis pasti dan pilihan pengobatan di masa depan.
Terapi Gen (Tahap Penelitian)
Kandidat pengobatan masa depan: Penelitian sedang berlangsung mengenai terapi penggantian gen yang menargetkan mutasi PRPH2.
Saat ini: Belum dapat diberikan sebagai pengobatan umum.
Penelitian terapi gen untuk penyakit retina herediter yang melibatkan PRPH2 semakin cepat secara global. Di Inggris, uji coba terapi gen untuk distrofi koroid (koroideremia) telah dilakukan pada tahun 2014, dan penerapannya pada penyakit mutasi PRPH2 juga sedang diteliti. Namun, saat ini belum ditetapkan sebagai terapi standar dan masih dalam tahap penelitian.
Di area atrofi, kapiler koroid, epitel pigmen retina, dan fotoreseptor (batang dan kerucut) menghilang. Jumlah sel di lapisan nukleus luar berkurang drastis, dan membran limitans eksterna langsung bersentuhan dengan membran Bruch. Pembuluh darah koroid berukuran sedang dan besar tetap bertahan lama bahkan pada tahap lanjut.
Periferin-2 terlokalisasi di tepi cakram segmen luar fotoreseptor dan memainkan peran penting dalam pembentukan cakram, stabilisasi, dan mempertahankan kelengkungan tepi.
Ketika terjadi haploinsufisiensi PRPH2 (kehilangan fungsi satu salinan), pembentukan morfologi segmen luar yang normal terganggu. Kerusakan struktural segmen luar berkembang menjadi apoptosis fotoreseptor, yang menyebabkan atrofi sekunder epitel pigmen retina dan kapiler koroid.
PRPH2 diduga memiliki fungsi berbeda pada batang dan kerucut; pada model tikus knockout PRPH2, dilaporkan bahwa kerucut biru mengalami degenerasi lebih lambat daripada kerucut lainnya. Perbedaan antara batang dan kerucut ini dianggap berkontribusi pada keragaman fenotip klinis penyakit.
Pada elektroretinografi multifokal, penurunan fungsi terdeteksi bahkan di area parafoveal yang melampaui area atrofi yang terlihat pada pemeriksaan fundus. Ini menunjukkan bahwa lesi CACD meluas lebih luas daripada atrofi yang terlihat secara klinis.
Penelitian tentang terapi penggantian gen dan terapi penyuntingan gen untuk penyakit retina herediter yang melibatkan mutasi PRPH2 sedang berlangsung secara global. Untuk penyakit terkait (koroideremia), uji klinis terapi gen pertama dilakukan di Inggris pada tahun 2014.
Analisis patogenisitas setiap mutasi semakin diperhalus seiring kemajuan pengobatan genom. Meluasnya penggunaan whole exome sequencing (WES) telah secara signifikan meningkatkan akurasi diagnostik 1), memungkinkan identifikasi mutasi pada lebih banyak pasien.
PRPH2 diketahui memiliki peran fungsional yang berbeda pada sel batang dan kerucut pada tingkat molekuler. Pengetahuan ini penting untuk menjelaskan keragaman fenotipe (apakah degenerasi dominan pada batang atau kerucut), dan berpotensi memengaruhi pemilihan target terapi di masa depan.