المرحلة الأولى
تغيرات في الظهارة الصبغية للشبكية (RPE) حول النقرة: تظهر تغيرات صبغية نقطية أو بقعية في الظهارة الصبغية للشبكية.
الرؤية والأعراض الذاتية: غالبًا ما تكون طبيعية.

ضمور المشيمية والشبكية المركزي الحلقي (CACD) هو ضمور بقعة وراثي يسبب ضمورًا واضحًا في الشبكية والمشيمية في منطقة البقعة. معدل الإصابة منخفض (حوالي 1 لكل 100,000 شخص)، ويصنف كمرض نادر.
غالبًا ما يبدأ المرض بين سن 20 و50 عامًا. النمط الوراثي السائد هو الوراثة الجسدية السائدة (AD)، كما تم الإبلاغ عن حالات وراثة جسدية متنحية (AR) وحالات متفرقة.
الجين المسبب الأكثر شيوعًا هو PRPH2 (الكروموسوم 17p13)، الذي يرمز لبروتين بيريفيرين-2. يعتبر بيريفيرين-2 ضروريًا لتكوين واستقرار أقراص الجزء الخارجي للمستقبلات الضوئية. يُعتقد أن نقص الجرعة (فقدان وظيفة أحد الأليلات) هو الآلية الرئيسية للمرض.
لوحظ تشابه في النمط الظاهري بين CACD والأمراض الناتجة عن طفرات جين ABCA4 (مثل مرض ستارغاردت) 1)، مما يجعل الاختبار الجيني مهمًا للتشخيص التفريقي. لم يتم الإبلاغ عن مضاعفات جهازية.
يبدأ الضمور البقعي المرتبط بالعمر عادة بعد سن 60 عامًا، وغالبًا ما يكون مصحوبًا بالدرزات والتغيرات النضحية. يبدأ CACD في سن مبكرة إلى متوسطة، ويتميز بضمور واضح الحدود دون درزات. يمكن تأكيد تشخيص CACD عن طريق الاختبار الجيني لطفرات PRPH2.
العارض الرئيسي هو العتمة المركزية الثنائية (صعوبة رؤية الجزء المركزي). قد يحدث انخفاض الرؤية مبكرًا، ولكن في بعض الحالات تظل الرؤية جيدة نسبيًا حتى مراحل متقدمة.
تظهر آفات بقعية متناظرة في كلتا العينين، وتصنف المرحلة إلى 4 مراحل. العصب البصري والأوعية الدموية الشبكية والشبكية المحيطية تبقى سليمة. يبلغ حجم المنطقة الضامرة حوالي 2-4 أضعاف قطر القرص البصري (DD).
المرحلة الأولى
تغيرات في الظهارة الصبغية للشبكية (RPE) حول النقرة: تظهر تغيرات صبغية نقطية أو بقعية في الظهارة الصبغية للشبكية.
الرؤية والأعراض الذاتية: غالبًا ما تكون طبيعية.
المرحلة الثانية
ضمور ناقص الصباغ غير واضح الحدود: تظهر منطقة ضمور شاحبة خارج النقرة.
اتساع تغيرات RPE: يُلاحظ ضمور غير واضح الحدود بعد.
المرحلة الثالثة
ضمور RPE واضح الحدود: تتشكل منطقة ضمور واضحة الحدود خارج النقرة.
الحفاظ على النقرة: في هذه المرحلة، تبقى النقرة (fovea) سليمة، وتكون الرؤية محفوظة نسبيًا.
المرحلة الرابعة
ضمور كامل يشمل النقرة: تتوسع منطقة الضمور لتشمل النقرة والبقعة بأكملها.
ضعف بصري شديد: يؤدي الفقدان الواسع للشعيرات الدموية المشيمية والخلايا المستقبلة للضوء والظهارة الصبغية الشبكية إلى انخفاض حاد في الرؤية.
تختلف سرعة التقدم بشكل كبير بين الأفراد. بشكل عام، يكون المسار بطيئًا، وقد تستغرق بعض الحالات عقودًا للوصول إلى المرحلة الرابعة. ومع ذلك، قد يختلف معدل التقدم حسب النمط الجيني، والتقييم الدوري للعين ضروري. يُعد تخطيط كهربية الشبكية متعدد البؤر (mfERG) المذكور بالتفصيل في قسم «التشخيص وطرق الفحص» مؤشرًا على التقدم المبكر.
السبب الرئيسي لـ CACD هو طفرة في جين PRPH2. يرمز PRPH2 لبروتين بيريفيرين-2، الذي يعمل على تكوين واستقرار أقراص الجزء الخارجي للمستقبلات الضوئية. تمنع الطفرات الحفاظ على البنية الطبيعية للجزء الخارجي للمستقبلات الضوئية.
نظرًا لأنه وراثة جسمية سائدة (AD)، فإن احتمال انتقال الجين المتحور من الوالد إلى الطفل هو 50٪. إذا كان هناك تاريخ عائلي للإصابة، يُوصى بالاستشارة الوراثية.
لم يتم تحديد عوامل الخطر المكتسبة أو عوامل نمط الحياة التي تسرع ظهور المرض أو تقدمه بشكل واضح حتى الآن.
CACD هي في الغالب وراثة جسمية سائدة، وخطر انتقالها إلى أطفال المريض يصل إلى 50٪. يمكن تحديد الطفرة عن طريق الاختبار الجيني، مما يتيح التشخيص المؤكد وفحص العائلة. بالإضافة إلى ذلك، نظرًا لأنها قد تكون هدفًا للعلاج الجيني في المستقبل، فإن تسجيل الطفرة مهم.
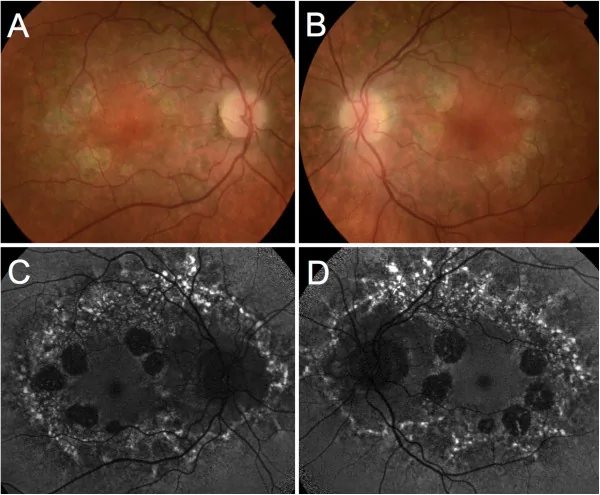
باستخدام المصباح الشقي ومنظار العين، يتم تأكيد وجود منطقة ضمور محددة بوضوح في البقعة. يتم تقييم وجود تعرض الأوعية المشيمية أو التصبغات.
تختلف نتائج كل فحص حسب مرحلة المرض. يوضح الجدول أدناه النتائج المميزة لكل مرحلة.
| الفحص | النتائج المبكرة | النتائج المتقدمة |
|---|---|---|
| FAF (التألق الذاتي لقاع العين) | فرط التألق | فقدان التألق (منطقة الضمور) |
| FA (تصوير الأوعية بالفلوريسين) | فرط التألق المجاور للنقرة | امتلاء شفاف في منطقة الضمور |
| OCT | سماكة POS-RPE | فقدان الطبقة الخارجية (المستقبلات الضوئية و RPE) |
من المهم التفريق بين الأمراض التي تظهر ضمورًا بقعيًا مشابهًا.
| مرض التفريق | نقاط التفريق |
|---|---|
| الضمور البقعي المرتبط بالعمر (AMD) من النوع الضموري | وجود دروزن، حدود غير منتظمة، ظهور في سن متأخر |
| مرض ستارغاردت | المشيمية الداكنة، طفرة ABCA4 |
| ضمور المخاريط | انخفاض شديد في استجابة المخاريط في تخطيط كهربية الشبكية، رهاب الضوء كعرض رئيسي |
لا يوجد حاليًا علاج محدد لـ CACD. يهدف العلاج إلى إدارة الأعراض والحفاظ على جودة الحياة.
إعادة التأهيل لضعف البصر
النظارات المكبرة والنظارات الواقية من الضوء: وصف أدوات مساعدة لتعظيم الاستفادة من الوظيفة البصرية المتبقية.
التدريب المهني والحياتي: المساعدة في اكتساب مهارات الحياة اليومية التي تتكيف مع الإعاقة البصرية.
الاستشارة الوراثية
تقديم المعلومات للعائلة: شرح الوراثة الجسدية السائدة (خطر وراثة 50%).
الاختبار الجيني: تحديد الطفرات مهم للتشخيص النهائي وخيارات العلاج المستقبلية.
العلاج الجيني (مرحلة البحث)
مرشح علاجي مستقبلي: يجري البحث في العلاج ببدائل الجينات المستهدف لطفرات PRPH2.
الوضع الحالي: لا يمكن تقديمه كعلاج عام في الوقت الحالي.
تتسارع الأبحاث عالميًا حول العلاج الجيني لأمراض الشبكية الوراثية التي تشمل PRPH2. في المملكة المتحدة، أُجريت تجربة علاج جيني لضمور المشيمية (كورويدييريميا) في عام 2014، ويُدرس تطبيقه على أمراض طفرات PRPH2. ومع ذلك، لم يُثبت بعد كعلاج قياسي ولا يزال في مرحلة البحث.
في منطقة الضمور، تختفي الشعيرات الدموية المشيمية والظهارة الصباغية للشبكية والخلايا المستقبلة للضوء (العصي والمخاريط). ينخفض عدد الخلايا في الطبقة النووية الخارجية بشكل كبير، وتتصل الغشاء المحدد الخارجي مباشرة بغشاء بروك. تبقى الأوعية المشيمية المتوسطة والكبيرة محفوظة لفترة طويلة حتى في المراحل المتقدمة.
يتمركز بروتين بيريفيرين-2 في حافة أقراص الجزء الخارجي للمستقبلات الضوئية، ويلعب دورًا أساسيًا في تكوين الأقراص واستقرارها والحفاظ على انحناء الحافة.
عند حدوث نقص في جرعة PRPH2 (فقدان وظيفة نسخة واحدة)، يتعطل تكوين الشكل الطبيعي للجزء الخارجي. يؤدي الانهيار الهيكلي للجزء الخارجي إلى موت الخلايا المبرمج للمستقبلات الضوئية، مما يسبب ضمورًا ثانويًا في الظهارة الصباغية للشبكية والشعيرات الدموية المشيمية.
يُقترح أن PRPH2 يؤدي وظائف مختلفة في العصي والمخاريط؛ في نموذج الفأر مع تعطيل PRPH2، يُبلغ أن المخاريط الزرقاء تتنكس بشكل أبطأ من المخاريط الأخرى. يُعتقد أن هذا الاختلاف بين العصي والمخاريط يساهم في تنوع النمط الظاهري السريري للمرض.
في تخطيط كهربية الشبكية متعدد البؤر، يُكتشف انخفاض الوظيفة حتى في المنطقة المجاورة للنقرة التي تتجاوز منطقة الضمور المرئية في فحص قاع العين. يشير هذا إلى أن آفات CACD تمتد على نطاق أوسع من الضمور المرئي سريريًا.
يتم حاليًا إجراء أبحاث عالمية حول العلاج ببدائل الجينات والعلاج التحريري الجيني لأمراض الشبكية الوراثية التي تشمل طفرات PRPH2. في مرض ذي صلة (الكورويديرميا)، أجريت أول تجربة سريرية للعلاج الجيني في المملكة المتحدة في عام 2014.
يتم تحليل الإمراضية لكل طفرة بدقة مع تقدم الطب الجيني. أدى انتشار تحليل الإكسوم الكامل (WES) إلى تحسين دقة التشخيص بشكل كبير 1)، مما يتيح تحديد الطفرات لدى عدد أكبر من المرضى.
يتم توضيح أن PRPH2 له أدوار وظيفية مختلفة في العصي والمخاريط على المستوى الجزيئي. هذه المعرفة مهمة لتفسير تنوع الأنماط الظاهرية (سواء كان التنكس سائدًا في العصي أو المخاريط)، وقد تؤثر على اختيار الأهداف العلاجية في المستقبل.