กลุ่มอาการมิลเลอร์ ฟิชเชอร์ (MFS) เป็นชนิดย่อยของกลุ่มอาการกิลแลง-บาร์เร ซึ่งมีลักษณะสามประการคือ กล้ามเนื้อตาอัมพาต การเคลื่อนไหวไม่ประสานกัน และการหายไปของรีเฟล็กซ์เอ็น
ผู้ป่วย 80-90% มีแอนติบอดีต่อต้าน GQ1b ในซีรัมเป็นบวก ซึ่งเป็นตัวบ่งชี้การวินิจฉัยที่สำคัญ
มักเกิดขึ้นประมาณหนึ่งสัปดาห์หลังการติดเชื้อทางเดินหายใจส่วนบน (76%) หรือการติดเชื้อในระบบทางเดินอาหาร
ส่วนใหญ่เป็นโรคที่จำกัดตัวเอง โดยการเคลื่อนไหวไม่ประสานกันจะดีขึ้นในประมาณ 1 เดือน และกล้ามเนื้อตาภายนอกอัมพาตจะดีขึ้นในประมาณ 3 เดือน
ในกรณีที่ลุกลามเป็น GBS หรือสมองอักเสบก้านสมองบิกเกอร์สตาฟฟ์ แนะนำให้ใช้การรักษาด้วย IVI G หรือการแลกเปลี่ยนพลาสมา
ความชุกทั่วโลกประมาณ 1 ต่อล้านคน และในเอเชียตะวันออกพบ 17-25% ของ GBS ซึ่งสูงกว่าในยุโรป/อเมริกา (5%)
อัตราการกลับเป็นซ้ำอยู่ที่ 11–14% และมีข้อบ่งชี้ถึงความเกี่ยวข้องกับ HLA-DR2
กลุ่มอาการมิลเลอร์ ฟิชเชอร์ (Miller Fisher Syndrome; MFS) เป็นโรคปลายประสาทอักเสบชนิดเฉียบพลันที่เกิดจากภูมิคุ้มกันทำลายตนเอง โดยมีสามอาการหลักคือ กล้ามเนื้อตาภายนอกเป็นอัมพาต การเคลื่อนไหวไม่ประสานกัน และการหายไปของรีเฟล็กซ์เอ็น จัดเป็นชนิดย่อยของกลุ่มอาการกิลแลง-บาร์เร (GBS)
Charles Miller Fisher รายงานรายละเอียดครั้งแรกในปี ค.ศ. 1956 เชื่อกันว่า James Collier ได้นิยามสามอาการหลักไว้แล้วในปี ค.ศ. 19321) MFS อยู่ในสเปกตรัมของกลุ่มอาการแอนติบอดีต่อต้าน GQ1b ร่วมกับ GBS, โรคสมองอักเสบก้านสมองบิกเกอร์สตาฟฟ์ และกล้ามเนื้อตาภายนอกเป็นอัมพาตเฉียบพลัน (ชนิดที่ไม่มีการเคลื่อนไหวไม่ประสานกัน)
ระบาดวิทยา มีดังนี้:
ความชุกทั่วโลก : ประมาณ 1 คนต่อประชากร 1,000,000 คน1) อุบัติการณ์ : 0.09 ต่อ 100,000 คน2) สัดส่วนใน GBS : ประมาณ 5% ในตะวันตก, 17-25% ในเอเชียตะวันออก1) อัตราส่วนเพศ : 2:1 พบในผู้ชายมากกว่าอายุเฉลี่ยที่เริ่มป่วย : 40 ปี สามารถเกิดได้ทุกวัยอัตราการกลับเป็นซ้ำ : 11-14%1)
MFS มักมีโรคดำเนินไปแบบเฟสเดียวและจำกัดตัวเอง
Q
กลุ่มอาการมิลเลอร์ ฟิชเชอร์พบได้น้อยเพียงใด?
A
ความชุกทั่วโลกอยู่ที่ 1 ต่อล้านคน อุบัติการณ์ 0.09 ต่อ 100,000 คน ถือเป็นโรคที่พบได้ยาก1, 2) อย่างไรก็ตาม ในเอเชียตะวันออก กลุ่มอาการนี้คิดเป็น 17-25% ของผู้ป่วย GBS ซึ่งสูงกว่าประมาณ 5% ในยุโรปและอเมริกา1) .
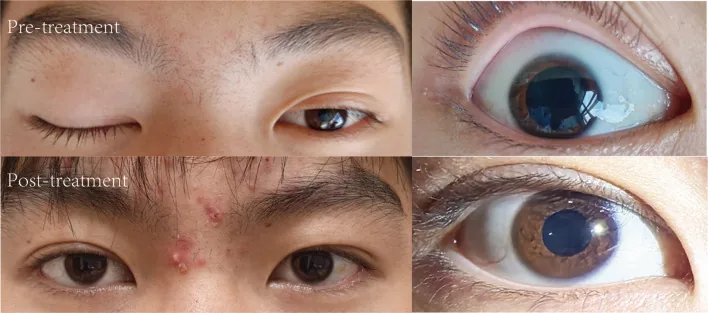
ภาพประกอบกลุ่มอาการมิลเลอร์ ฟิชเชอร์ Juyuan Pan, Ningyu Zheng, Dan Yu et al. Unilateral ophthalmoplegia in anti-GQ1b antibody syndrome: case report and systematic literature review. Frontiers in Immunology. 2025 Oct 10; 16:1669821. Figure 1. PM
CI D: PMC12549634. License: CC BY.
ภาพประกอบแสดงอาการหลักของกลุ่มอาการมิลเลอร์ ฟิชเชอร์
มักเริ่มมีอาการประมาณหนึ่งสัปดาห์หลังการติดเชื้อทางเดินหายใจส่วนบน โดยมีอาการเห็นภาพซ้อน หรือเวียนศีรษะ (เสียการทรงตัว) หลังจากดำเนินไป 1–2 สัปดาห์ มักมีแนวโน้มทุเลาได้เอง
อาการที่ผู้ป่วยรับรู้ได้หลักมีดังนี้:
เห็นภาพซ้อน เดินลำบาก/เวียนศีรษะ : พบใน 32%ความรู้สึกผิดปกติ : พบใน 14%อื่นๆ : หนังตาตก , สติสัมปชัญญะผิดปกติ, แขนขาอ่อนแรง, กลืนลำบาก, อาการของก้านสมอง, กลัวแสง, หน้ามืด, มองเห็นไม่ชัด, ปวดศีรษะ, อัมพาตเส้นประสาทใบหน้า
ต่อไปนี้คืออาการแสดงทางคลินิกที่สำคัญที่เกี่ยวข้องกับสามอาการหลักของ MFS
กล้ามเนื้อตาอัมพาต
กล้ามเนื้อนอกตาอัมพาต : มักเป็นทั้งสองข้างและสมมาตร พบข้างเดียวใน 27–31% ของผู้ป่วย4)
ความผิดปกติของกล้ามเนื้อในตา (ความผิดปกติของรูม่านตา ) : เกิดขึ้นประมาณครึ่งหนึ่งของผู้ป่วย มีอาการม่านตา ขยาย ปฏิกิริยาต่อแสงหายไป และความผิดปกติของการปรับโฟกัส
หนังตาตก
ภาวะเสียการทรงตัว (Ataxia)
ภาวะเสียการทรงตัวของลำตัวและแขนขา : ความรุนแรงแตกต่างกันไป ผู้ป่วย 30% มีภาวะเสียการทรงตัวรุนแรงจนไม่สามารถเดินเองได้ ไม่สามารถเดินต่อเท้าเป็นเส้นตรงได้
ระยะหลังเริ่มมีอาการ : มีแนวโน้มทุเลาลงภายในประมาณ 1 เดือน
การหายไปของรีเฟล็กซ์เอ็น
การหายไปของรีเฟล็กซ์เอ็นส่วนลึก : ถือว่าค่อนข้างจำเพาะต่อกลุ่มอาการนี้ ใน 12-31% ของผู้ป่วย รีเฟล็กซ์อาจยังคงอยู่
ระยะหลังเริ่มมีอาการ : การฟื้นตัวมีแนวโน้มช้ากว่าภาวะเสียการทรงตัวและกล้ามเนื้อตาอัมพาต
ลำดับการฟื้นตัว : ฟื้นตัวตามลำดับ ภาวะเสียการทรงตัว → อัมพาตกล้ามเนื้อตา → การหายไปของรีเฟล็กซ์เอ็นกล้ามเนื้อ1) ภาวะเสียการทรงตัวดีขึ้นในประมาณ 1 เดือน อัมพาตกล้ามเนื้อนอกลูกตา ในประมาณ 3 เดือน และส่วนใหญ่ฟื้นตัวโดยไม่มีภาวะแทรกซ้อนในประมาณ 6 เดือน
กลุ่มอาการ MFS/GBS ซ้อนทับ : 5.6–7.1% ของผู้ป่วย MFS มีอาการอ่อนแรงของแขนขาร่วมด้วย2)
MFS ไม่สมบูรณ์ : ภาวะอัมพาตกล้ามเนื้อตาเฉียบพลันโดยไม่มีภาวะเสียการทรงตัว (acute ophthalmoplegia without ataxia) ถือเป็นรูปแบบหนึ่งของกลุ่มอาการแอนติบอดีต่อ GQ1b5)
Q
อาการของกลุ่มอาการมิลเลอร์ ฟิชเชอร์ ฟื้นตัวตามลำดับใด?
A
การฟื้นตัวเกิดขึ้นตามลำดับ ภาวะเสียการทรงตัว (ประมาณ 1 เดือน) → อัมพาตกล้ามเนื้อตา (ประมาณ 3 เดือน) → การหายไปของรีเฟล็กซ์เอ็นกล้ามเนื้อ1) ผู้ป่วยส่วนใหญ่ฟื้นตัวโดยไม่มีภาวะแทรกซ้อนในประมาณ 6 เดือน
การเลียนแบบโมเลกุล (molecular mimicry) เป็นกลไกหลักของการเกิดโรค ลิโพลิโกแซ็กคาไรด์ของเชื้อก่อโรคมีโครงสร้างคล้ายคลึงกับแกงกลิโอไซด์ GQ1b ของมนุษย์ ทำให้เกิดการสร้างแอนติบอดีต่อต้าน GQ1b ที่ทำปฏิกิริยาข้ามกัน
การติดเชื้อก่อนหน้าและเชื้อก่อโรค :
การติดเชื้อทางเดินหายใจส่วนบน (76%) พบบ่อยที่สุด การติดเชื้อทางเดินอาหารพบใน 25%
ระยะเวลามัธยฐานจากการติดเชื้อถึงการแสดงอาการทางระบบประสาทคือ 8 วัน
Campylobacter jejuni (21%), Haemophilus influenzae (8%) 4) ใน 67% ของกรณี ไม่สามารถระบุเชื้อก่อโรคได้
อื่นๆ: มัยโคพลาสมา, ไซโตเมกาโลไวรัส, ไวรัสเอปสไตน์-บาร์, ไวรัสวาริเซลลา-ซอสเตอร์, เอชไอวี-1
ที่เกี่ยวข้องกับวัคซีน : มีรายงานการเกิดหลังการฉีดวัคซีนโควิด-19 (BNT162b2, ChAdOx1, วัคซีนเชื้อตาย), วัคซีนไข้หวัดใหญ่ และวัคซีนนิวโมคอคคัส5, 6, 7) .
ด้านล่างนี้เป็นสรุปการติดเชื้อและปัจจัยกระตุ้นหลักก่อนหน้านี้
ประเภทของปัจจัยกระตุ้น เชื้อก่อโรคหรือผลิตภัณฑ์ที่เป็นตัวแทน การติดเชื้อแบคทีเรีย C. jejuni, H. influenzae การติดเชื้อไวรัส ไซโตเมกาโลไวรัส, EB V, ไวรัสวาริเซลลา-ซอสเตอร์ วัคซีน วัคซีนโควิด-19, วัคซีนไข้หวัดใหญ่ ภูมิต้านตนเอง/เนื้องอก โรคต่อมไทรอยด์, SLE , เนื้องอกร้าย (มะเร็งปอด, มะเร็งต่อมน้ำเหลืองเบอร์คิตต์ ฯลฯ) 3)
ปัจจัยเสี่ยงทางพันธุกรรม : มีข้อเสนอแนะว่ามีความสัมพันธ์ระหว่าง HLA-DR2 กับกลุ่มอาการมิลเลอร์-ฟิชเชอร์ที่เกิดซ้ำ 4) .
การปรุงอาหารให้สุกทั่วถึงสามารถลดความเสี่ยงของการติดเชื้อแคมไพโลแบคเตอร์ได้ หากมีอาการเห็นภาพซ้อน หรือเวียนศีรษะหลังการติดเชื้อทางเดินหายใจส่วนบน ให้ไปพบแพทย์ทันที
Q
กลุ่มอาการมิลเลอร์-ฟิชเชอร์สามารถเกิดขึ้นหลังเป็นหวัดหรือฉีดวัคซีนได้หรือไม่?
A
ผู้ป่วย MFS 76% มีการติดเชื้อทางเดินหายใจส่วนบนมาก่อน นอกจากนี้ยังมีรายงานหลายกรณีหลังการฉีดวัคซีนโควิด-19 (วัคซีน mRNA และวัคซีนเชื้อตาย) และวัคซีนไข้หวัดใหญ่ 5, 6, 7) อย่างไรก็ตาม มีรายงานว่าการพยากรณ์โรคของ MFS หลังฉีดวัคซีนดีในทุกกรณี 7) .
การวินิจฉัย MFS อาศัยการวินิจฉัยทางคลินิกเป็นหลัก โดยการยืนยันสามอาการหลัก (กล้ามเนื้อตาอัมพาต, การเคลื่อนไหวไม่ประสานกัน, ภาวะไร้รีเฟล็กซ์) และการแยกโรคอื่นออก
แอนติบอดี IgG ต่อ GQ1b ในซีรัม เป็นการตรวจเสริมการวินิจฉัยที่สำคัญที่สุด
การตรวจ ความไว ความจำเพาะ แอนติบอดี IgG ต่อต้าน GQ1b ในซีรั่ม 92% 97%1) แอนติบอดีต่อต้าน GQ1b ในน้ำไขสันหลัง 20% 100%1)
ผู้ป่วย MFS 80-90% มีแอนติบอดีต่อ GQ1b ในซีรัมเป็นบวก
ความไวของการตรวจซีรัมสูงกว่าการตรวจน้ำไขสันหลังใน 3 สัปดาห์แรกหลังเริ่มมีอาการ
ระดับไทเทอร์ของแอนติบอดีสัมพันธ์กับความรุนแรงของกล้ามเนื้อตาอัมพาต
การตรวจน้ำไขสันหลัง : พบการแยกตัวของโปรตีนและเซลล์ (อัลบูมินสูงขึ้นแต่จำนวนเซลล์ปกติ) อย่างไรก็ตาม นี่เป็นลักษณะร่วมของโรคภูมิคุ้มกันทางระบบประสาท
การตรวจภาพทางระบบประสาท (MRI สมอง) : ปกติโดยทั่วไป พบความผิดปกติไม่จำเพาะในซีรีเบลลัม ก้านสมองน้อย หรือสมองส่วนกลาง หรือการเพิ่มความเข้มของก้านสมองได้น้อยครั้ง
การศึกษาการนำกระแสประสาท : ปกติในกรณีส่วนใหญ่
การแยกโรคจากโรคต่อไปนี้มีความสำคัญ
โรคกล้ามเนื้ออ่อนแรงชนิดร้าย (Myasthenia Gravis) : แยกโดยดูว่ามีความผันผวนในแต่ละวันหรือไม่ และการทดสอบเทนซิลอนดีขึ้นหรือไม่กลุ่มอาการเมดิอัลลองจิจูดินัลฟาสซิคูลัส (Medial Longitudinal Fasciculus Syndrome) : แยกโดยดูว่าไม่สมมาตรทั้งสองข้างและไม่มีอาการเสียการทรงตัวของลำตัวโรคสมองจากวิตามินบี1 ขาด (Wernicke Encephalopathy) : ภาวะโภชนาการ การมีหรือไม่มีอาตา และความผิดปกติของความรู้สึกตัวสมองส่วนก้านขาดเลือดและเนื้องอกก้านสมอง : การตรวจ MRI และอาการแสดงทางระบบประสาทเฉพาะที่โรคสมองอักเสบก้านสมองบิกเกอร์สตาฟฟ์ : การมีหรือไม่มีความผิดปกติของสติ ความต่อเนื่องในสเปกตรัมของแอนติบอดีต่อต้าน GQ1bอื่นๆ: โรคโบทูลิซึม, กลุ่มอาการโทโลซา-ฮันต์ , โรคปลอกประสาทเสื่อมแข็ง, โรคสมองและไขสันหลังอักเสบเฉียบพลันแพร่กระจาย, โรคเส้นประสาทจากเบาหวาน, โรคซาร์คอยโดซิส
MFS เป็นโรคที่จำกัดตัวเอง และในกรณีที่การทำงานของระบบหายใจยังคงดี การรักษาแบบประคับประคอง (การรักษาตามอาการ) อาจเพียงพอ ผู้ป่วยส่วนใหญ่หายได้เองและการพยากรณ์โรคดี
ยังไม่มีการรักษาที่มีประสิทธิภาพที่ได้รับการยืนยัน แต่มีการใช้การรักษาด้วยภูมิคุ้มกันดังต่อไปนี้
การรักษาด้วย IVIG
ข้อบ่งใช้ : กรณีรุนแรงและเป็นอันตรายถึงชีวิต (ภาวะกดการหายใจ, กลุ่มอาการ MFS/GBS ร่วม, โรคสมองอักเสบก้านสมองบิกเกอร์สตาฟฟ์) 1)
ขนาดยา : 2 กรัมต่อน้ำหนักตัว 1 กิโลกรัม แบ่งให้ใน 5 วัน (400 มก./กก./วัน × 5 วัน) 3)
ประสิทธิผล : ยังไม่มีการศึกษาแบบสุ่มที่มีกลุ่มควบคุมสำหรับ MFS การศึกษาย้อนหลังพบว่าไม่มีผลกระทบสำคัญต่อผลลัพธ์ แต่มีรายงานว่าช่วยให้การเริ่มฟื้นตัวของกล้ามเนื้อตาอัมพาตเร็วขึ้นเล็กน้อย (จาก 13.5 วันเป็น 12.0 วันหลังเริ่มมีอาการ)
การรักษาด้วยการแลกเปลี่ยนพลาสมา
ข้อบ่งใช้ : กรณีที่ใช้ IVI G ได้ยาก, กรณี GBS ที่ลุกลาม, กรณีโรคสมองอักเสบก้านสมองบิกเกอร์สตาฟฟ์ที่ลุกลาม
ประสิทธิผล : มีรายงานผู้ป่วยที่ประสบความสำเร็จ แต่การศึกษาแบบย้อนหลังไม่พบประโยชน์ที่มีนัยสำคัญ มีการลองใช้ร่วมกับการบำบัดด้วยการดูดซับภูมิคุ้มกันเพื่อกำจัดแอนติบอดีต่อต้าน GQ1b
การใช้ IVMP เพิ่มเติม : มีรายงานผู้ป่วยที่เพิ่มการรักษาด้วย methylprednisolone pulse (IVMP) ในผู้ที่ฟื้นตัวไม่เพียงพอจากการใช้ IVI G เพียงอย่างเดียว8)
โรคที่จำกัดตัวเองได้ มีการพยากรณ์โรคที่ดี มักกลับมาเป็นปกติภายในหกเดือน
ภาวะเสียการทรงตัว: ทุเลาลงในประมาณหนึ่งเดือน
อัมพาตกล้ามเนื้อตาส่วนนอก: ทุเลาลงในประมาณสามเดือน
เวลาเฉลี่ยในการฟื้นตัว: ประมาณ 10 สัปดาห์
อาการตกค้าง: พบได้สูงสุด 1 ใน 3 ของผู้ป่วย
อัตราการกลับเป็นซ้ำ: 3–14% อัตราการเสียชีวิต: ประมาณ 4%
MFS บางส่วนอาจพัฒนาไปเป็น GBS หรือโรคสมองอักเสบก้านสมองแบบบิกเกอร์สตาฟฟ์ หากมีอาการอ่อนแรงของแขนขา รู้สึกตัวผิดปกติ หรือหายใจลำบาก ควรพิจารณาการให้ภูมิคุ้มกันบำบัดอย่างรวดเร็วและจำเป็นต้องดูแลในโรงพยาบาล
Q
กลุ่มอาการมิลเลอร์ ฟิชเชอร์สามารถหายได้เองโดยไม่ต้องรักษาหรือไม่?
A
เป็นโรคที่จำกัดตัวเอง (self-limiting) ซึ่งส่วนใหญ่หายได้เอง IVI G อาจช่วยให้กล้ามเนื้อตาที่เป็นอัมพาตฟื้นตัวเร็วขึ้นเล็กน้อย แต่การศึกษาแบบย้อนหลังไม่พบผลกระทบสำคัญต่อผลลัพธ์ อย่างไรก็ตาม หากลุกลามเป็น GBS หรือสมองส่วนกลางอักเสบแบบ Bickerstaff แนะนำให้ใช้ IVI G หรือการแลกเปลี่ยนพลาสมา 1) .
ลิโพลิโกแซ็กคาไรด์ของเชื้อก่อโรค เช่น C. jejuni และ H. influenzae มีโครงสร้างคล้ายคลึงกับแกงกลิโอไซด์ GQ1b ทำให้หลังการติดเชื้อเกิดการสร้างแอนติบอดี IgG ต่อ GQ1b ที่มีปฏิกิริยาข้ามกัน
ยีน cst-II ของ C. jejuni : ความหลากหลาย Asn51 → แอนติบอดีต่อ GQ1b → อัมพาตกล้ามเนื้อตาและการเคลื่อนไหวผิดปกติ / ความหลากหลาย Thr51 → แอนติบอดีต่อ GM1 และ GD1a → แขนขาอ่อนแรง (ชนิด GBS)
ความเกี่ยวข้องกับวัคซีน COVID-19: โปรตีนหนามของ SARS-CoV-2 จับกับแกงกลิโอไซด์ผ่านกรดเซียลิก → การเลียนแบบโมเลกุล 6)
GQ1b มีการแสดงออกอย่างมากในตำแหน่งต่อไปนี้ และแต่ละตำแหน่งอธิบายอาการทางคลินิกที่แตกต่างกัน
บริเวณพาราโนดและปลายประสาทของเส้นประสาทกล้ามเนื้อตา (III, IV, VI) : มีการแสดงออกมากกว่าเส้นประสาทสมองอื่นๆ กลไกหลักที่แอนติบอดีต่อต้าน GQ1b เกี่ยวข้องกับอัมพาตของกล้ามเนื้อนอกลูกตา เซลล์ขนาดใหญ่ในปมประสาทรากหลัง (นิวรอน Ia) : ความเสียหายของนิวรอน Ia ทำให้เกิดการเสียการทรงตัวและการสูญเสียรีเฟล็กซ์เอ็นเนื่องจากความบกพร่องของข้อมูลรับความรู้สึกปมประสาทซิลิอารี : ทำให้เกิดอัมพาตของกล้ามเนื้อในลูกตา (ความผิดปกติของรูม่านตา และการปรับโฟกัส)เยื่อหุ้มก่อนไซแนปส์ที่รอยต่อประสาทและกล้ามเนื้อ : แอนติบอดีต่อต้าน GQ1b จับกับ NMJ → ปล่อยอะเซทิลโคลีนจำนวนมากที่ขึ้นกับคอมพลีเมนต์ → ในที่สุดขัดขวางการส่งสัญญาณประสาทและกล้ามเนื้อ นอกจากนี้ยังเกิดการทำลายปลายแอกซอน ไซแนปส์รอบข้าง และเซลล์ชวานน์ที่อาศัยคอมพลีเมนต์
GT1a แสดงออกอย่างมากในเส้นประสาทกลอสโซฟาริงเจียลและเวกัส ในกลุ่มอาการกิลแลง-บาร์เรที่ตรวจพบแอนติบอดีต่อ GT1a มีรายงานอัมพาตของเส้นประสาทสมอง (ตาเหล่ 57%, อัมพาตใบหน้า 57%, อัมพาตบัลบาร์ 70%) และ 39% ต้องใช้เครื่องช่วยหายใจ 8) .
กลไกทั้งส่วนปลาย (การขาดเส้นใยนำเข้าจากแกนกล้ามเนื้อ) และส่วนกลาง (แอนติบอดีต่อสมองน้อย) อาจเกี่ยวข้อง
เนื้อหาต่อไปนี้อยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิกในปัจจุบัน และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Liang et al. (2022) ได้ทำการทบทวนขอบเขตของ 10 ราย และสรุปลักษณะทางคลินิกของ MFS หลังวัคซีน COVID-197) .
อายุเฉลี่ย 63.5 ปี เพศชาย 80% ระยะเวลามัธยฐานจากวัคซีนถึงเริ่มมีอาการ 13 วัน การแยกตัวของโปรตีน-เซลล์ในน้ำไขสันหลัง 88.9% แอนติบอดีต่อ ganglioside เป็นบวก 62.5% ทุกกรณีมีการพยากรณ์โรคที่ดี7) .
ใน MFS หลังวัคซีน mRNA (BNT162b2) โปรตีนหนามของ SARS-CoV-2 แสดงความสัมพันธ์กับแกงกลิโอไซด์ผ่านกรดเซียลิก ซึ่งเป็นกลไกทางพยาธิวิทยาที่น่าสนใจ 6) .
เป็นที่ทราบกันว่า 27-31% ของกลุ่มอาการแอนติบอดีต่อต้าน GQ1b แสดงอาการกล้ามเนื้อตาอัมพาตข้างเดียว 4) .
Pan et al. (2025) ได้ทำการทบทวนอย่างเป็นระบบใน 18 ราย โดยมีอายุเฉลี่ย 31 ปี และเพศชายเด่น (13/18) ในเด็ก 44.4% แสดงอาการกล้ามเนื้อตาอ่อนแรงข้างเดียว ในขณะที่ผู้ใหญ่มีเพียง 5.7% ส่วนใหญ่ฟื้นตัวภายใน 3 เดือน4) .
มีรายงานผู้ป่วยที่ได้รับ IVMP เพิ่มเติมในกรณีที่การฟื้นตัวล่าช้าเมื่อใช้ IVI G เพียงอย่างเดียว 8) มีการเสนอว่าอาจมีผลในการเร่งการฟื้นตัว แต่ระดับหลักฐานยังคงเป็นเพียงรายงานผู้ป่วยเท่านั้น
อัตราการกลับเป็นซ้ำอยู่ที่ 11–14% และมีความเกี่ยวข้องกับ HLA-DR21) การกลับเป็นซ้ำอาจรุนแรงน้อยกว่าครั้งแรก (เช่น เฉพาะกล้ามเนื้อตาอัมพาต) และมีรายงานผู้ป่วยที่หายดีภายในหนึ่งเดือนโดยการรักษาแบบประคับประคองเท่านั้น1) .
รายงาน MFS ระหว่างตั้งครรภ์พบได้น้อยมาก มีรายงานการใช้ทั้ง IVI G และพลาสมาเฟเรซิส และไม่มีรายงานภาวะแทรกซ้อนปริกำเนิด 9) .
Ooi ST, Ahmad A, Yaakub A. Recurrent Miller Fisher Syndrome. Cureus. 2022;14(6):e26192.
Bahk J, Yang W, Fishman J. Bilateral vocal cord paralysis in Miller Fisher syndrome/Guillain-Barre overlap syndrome and a review of previous case series. BMJ Case Rep. 2021;14:e240386.
Hakobyan N, Yadav R, Pokhrel A, et al. Miller-Fisher Syndrome Unveiled in the Presence of Cholangiocarcinoma. Cureus. 2023;15(11):e49016.
Pan J, Zheng N, Yu D, Jiang H, Zhou Y. Unilateral ophthalmoplegia in anti-GQ1b antibody syndrome: case report and systematic literature review. Front Immunol. 2025;16:1669821.
Abicic A, Adamec I, Habek M. Miller Fisher syndrome following Pfizer COVID-19 vaccine. Neurol Sci. 2022;43:1495-1497.
Yamakawa M, Nakahara K, Nakanishi T, Nomura T, Ueda M. Miller Fisher Syndrome Following Vaccination against SARS-CoV-2. Intern Med. 2022;61:1067-1069.
Liang H, Cao Y, Zhong W, et al. Miller-Fisher syndrome and Guillain-Barre syndrome overlap syndrome following inactivated COVID-19 vaccine: Case report and scope review. Hum Vaccin Immunother. 2022;18(6):e2125753.
Mitsuhashi S, Suzuki A, Hayashi K, et al. Miller-Fisher Syndrome Following Influenza A Infection. Cureus. 2024;16(3):e56064.
Ángel-Páez JA, Hurtado-Bugna S, Aragón-Mendoza RL, et al. Miller Fisher syndrome treated with plasmapheresis during pregnancy: Case report and review of the literature. Rev Colomb Obstet Ginecol. 2021;72:210-218.