โรคเส้นประสาทสมองอักเสบเป็นโรคที่เกิดจากการอักเสบของเส้นประสาทสมอง ทำให้เกิดการทำลายเส้นประสาทหรือการสูญเสียปลอกไมอีลิน
เมื่อเส้นประสาทสมองหลายเส้นถูกกระทบ จะจัดเป็นโรคเส้นประสาทสมองอักเสบหลายเส้น
สาเหตุมีหลากหลาย รวมถึงการติดเชื้อ (เช่น โรคไลม์ , SARS-CoV-2), ภูมิต้านตนเอง (เช่น ชนิดย่อยของ GBS), เนื้องอก, หลอดเลือด และไม่ทราบสาเหตุ
เมื่อมีภาวะผิดปกติของการเคลื่อนไหวลูกตา การเพิ่มความเข้มของสัญญาณของเส้นประสาทสมองที่ได้รับผลกระทบในการตรวจ MRI ด้วยสารทึบรังสีเป็นลักษณะเฉพาะ
ในโรคเส้นประสาทสมองอักเสบหลายเส้นซึ่งเป็นชนิดย่อยของ GBS การรักษาด้วยอิมมูโนโกลบูลินทางหลอดเลือดดำ (IVI G) มักได้ผลดี
การรักษาให้ความสำคัญกับการระบุสาเหตุและการจัดการโรคพื้นเดิม
ด้วยการวินิจฉัยแต่เนิ่นๆ และการรักษาที่เหมาะสม อาการทางระบบประสาทสามารถดีขึ้นได้ในหลายกรณี แต่บางกรณีอาจยืดเยื้อ
โรคเส้นประสาทสมองอักเสบเป็นคำทั่วไปสำหรับโรคที่เกิดการอักเสบของเส้นประสาทสมอง ทำให้เกิดการทำลายเส้นประสาทหรือการสูญเสียปลอกไมอีลิน อาจมีเพียงเส้นประสาทสมองเส้นเดียวที่ถูกกระทบ หรือหลายเส้นพร้อมกัน กรณีหลังเรียกว่าโรคเส้นประสาทสมองอักเสบหลายเส้น (PNC)
PNC ถูกจัดเป็นชนิดย่อยที่พบได้ยากของกลุ่มอาการกิลแลง-บาร์เร (GBS) ในการจำแนก GBS ที่เสนอโดย Wakerley และคณะในปี 2014 PNC ถูกนิยามว่าเป็นภาวะที่แสดงเฉพาะความผิดปกติของการเคลื่อนไหวลูกตา และอาการของก้านสมองส่วนท้าย โดยไม่มีอาการอ่อนแรงของแขนขาหรือการเสียการทรงตัว 1)
ในการทบทวนวรรณกรรมเกี่ยวกับ PNC อายุมัธยฐานของผู้ป่วย 20 รายที่รายงานคือ 40 ปี และร้อยละ 75 เป็นเพศชาย 3) ภาวะกล้ามเนื้อใบหน้าอ่อนแรงพบร้อยละ 70 และปฏิกิริยาตอบสนองของเอ็นกล้ามเนื้อปกติพบร้อยละ 50 3) เมื่อเส้นประสาทสมองที่เกี่ยวข้องกับการเคลื่อนไหวลูกตา (เส้นประสาทสมองคู่ที่ III, IV, VI) ถูกทำลาย อาการภาพซ้อน และตาเหล่ จะกลายเป็นอาการหลัก
Q
ความแตกต่างระหว่างโรคเส้นประสาทสมองอักเสบและโรคเส้นประสาทสมองหลายเส้นอักเสบคืออะไร?
A
โรคเส้นประสาทสมองอักเสบเป็นคำทั่วไปสำหรับการอักเสบของเส้นประสาทสมอง เมื่อเส้นประสาทสมองเส้นเดียวได้รับความเสียหาย เรียกว่า โรคเส้นประสาทสมองอักเสบ เมื่อเส้นประสาทสมองหลายเส้นได้รับความเสียหายพร้อมกัน เรียกว่า โรคเส้นประสาทสมองหลายเส้นอักเสบ (polyneuritis cranialis) โรคเส้นประสาทสมองหลายเส้นอักเสบถูกจัดเป็นชนิดย่อยที่พบได้ยากของ GBS
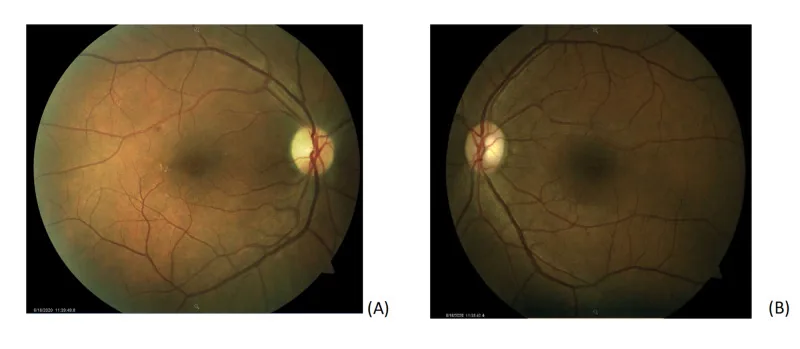
ภาพถ่ายจอประสาทตาแสดงหัวประสาทตาซีดด้านขมับ Rho J, et al. A Case of Non-Arteritic Anterior Ischemic
Optic Neuropathy with COVID-19. Cureus. 2020. Figure 1. PM
CI D: PMC7785499. License: CC BY.
ภาพถ่ายสีจอประสาทตา ของตาทั้งสองข้าง ตาขวา (A) แสดง microaneurysm และสารคัดหลั่งตามแนวเส้นเลือดส่วนบนด้านขมับ รวมถึงหัวประสาทตาซีดด้านขมับ ส่วนตาซ้าย (B) ปกติ ภาพนี้สอดคล้องกับหัวประสาทตาซีดที่กล่าวถึงในหัวข้อ “2. อาการหลักและอาการแสดงทางคลินิก”
อาการที่ผู้ป่วยรู้สึกจากโรคเส้นประสาทสมองอักเสบแตกต่างกันไปตามเส้นประสาทสมองที่ได้รับความเสียหาย อาการหลักมีดังนี้:
ภาพซ้อน (เห็นภาพซ้อน )หนังตาตก ใบหน้าไม่สมมาตรหรือชา : ทำให้เกิดอัมพาตใบหน้าจากความผิดปกติของเส้นประสาทใบหน้า (เส้นประสาทสมองคู่ที่ VII) และความรู้สึกที่ใบหน้าลดลงจากความผิดปกติของเส้นประสาทไทรเจมินัล (เส้นประสาทสมองคู่ที่ V)กลืนลำบากและเสียงเปลี่ยน : เกิดจากความผิดปกติของเส้นประสาทกลอสโซฟาริงเจียล (เส้นประสาทสมองคู่ที่ IX) และเส้นประสาทเวกัส (เส้นประสาทสมองคู่ที่ X)เวียนศีรษะและหูอื้อ : เกิดจากความผิดปกติของเส้นประสาทเวสติบูโลคอเคลีย (เส้นประสาทสมองคู่ที่ VIII)พูดไม่ชัด : เกิดจากความผิดปกติของเส้นประสาทไฮโปกลอสซัล (เส้นประสาทสมองคู่ที่ XII) ทำให้การเคลื่อนไหวของลิ้นผิดปกติปวดศีรษะ : พบได้บ่อยเป็นอาการร่วมของโรคเส้นประสาทสมองอักเสบ
ความผิดปกติของการเคลื่อนไหวของลูกตา
อัมพาตเส้นประสาทสมองคู่ที่ 3 (oculomotor) : ตาเบี่ยงลงและออกด้านนอก, รูม่านตา ขยาย, หนังตาตก
อัมพาตเส้นประสาทสมองคู่ที่ 4 (trochlear) : ทำให้เห็นภาพซ้อน ในแนวตั้งหรือหมุน
อัมพาตเส้นประสาทสมองคู่ที่ 6 (abducens) : ทำให้เห็นภาพซ้อน ในแนวนอนเนื่องจากการจำกัดการกางตา
ความผิดปกติของเส้นประสาทสมองส่วนล่าง
อัมพาตเส้นประสาทสมองคู่ที่ 7 (facial) : ทำให้ใบหน้าไม่สมมาตร, หลับตาไม่สนิท, การรับรสผิดปกติ ประเมินความรุนแรงโดยใช้การจัดระดับของ House-Brackmann 2)
อัมพาตเส้นประสาทสมองคู่ที่ 12 (hypoglossal) : พบการฝ่อของลิ้น, การเบี่ยงเบน, และการกระตุกของมัดกล้ามเนื้อ 1)
อัมพาตของ bulbar (คู่ที่ 9 และ 10) : ทำให้กลืนลำบาก, เสียงแหบ, เพดานอ่อนเบี่ยง
ในภาวะปลายประสาทสมองอักเสบหลายเส้น มักพบการลดลงหรือหายไปของรีเฟล็กซ์เอ็นส่วนลึก 1) 3) หากมีอาการระคายเคืองเยื่อหุ้มสมองร่วมด้วย แสดงถึงการมีเยื่อหุ้มสมองอักเสบเป็นโรคพื้นเดิม
สาเหตุของปลายประสาทสมองอักเสบมีหลากหลาย สาเหตุหลักจำแนกได้ดังนี้
การจำแนก สาเหตุที่พบบ่อย ติดเชื้อ ไวรัส varicella-zoster, EB V, โรค Lyme, วัณโรค, ซิฟิลิส, SARS-CoV-2 ภูมิต้านตนเอง GBS/MFS, ซาร์คอยโดซิส , SLE , โรคเบห์เซ็ต, MOG-AD เนื้องอก เนื้องอกเยื่อหุ้มสมองชั้นใน, เนื้องอกแพร่กระจาย, ยายับยั้งจุดตรวจภูมิคุ้มกัน หลอดเลือด เบาหวาน, โป่งพองของหลอดเลือด ไม่ทราบสาเหตุ โรคเส้นประสาทสมองหลายเส้นไม่ทราบสาเหตุ, เยื่อหุ้มสมองอักเสบหนาตัว
ในสาเหตุจากการติดเชื้อ โรคไลม์ (การติดเชื้อ Borrelia burgdorferi) มีความสำคัญ โรคประสาทจากไลม์เกิดขึ้นในผู้ป่วยโรคไลม์ ที่ไม่ได้รับการรักษา 10-15% โดยมีสามอาการหลักคือ เยื่อหุ้มสมองอักเสบชนิดลิมโฟไซต์, เส้นประสาทสมองอักเสบ, และรากประสาทอักเสบ 4) .
นอกจากนี้ยังมีรายงานเส้นประสาทสมองอักเสบหลังการติดเชื้อ SARS-CoV-2 ในสองกรณีของเส้นประสาทสมองหลายเส้นอักเสบที่เน้นที่เส้นประสาทไฮโปกลอสซัลหลังปอดอักเสบรุนแรงจาก COVID-19 พบว่ามีการปรับปรุงอย่างชัดเจนหลังให้ IVI G 1) กลไกการเกิดโรคน่าจะเป็นทางภูมิคุ้มกันมากกว่าการบุกรุกเส้นประสาทโดยตรง 1) .
ใน PNC ซึ่งเป็นชนิดย่อยของ GBS ตรวจพบแอนติบอดี IgG ต่อต้าน GQ1b ในซีรัมได้ 47% 3) การติดเชื้อก่อนหน้าที่พบบ่อยที่สุดคือ Mycoplasma pneumoniae 3) .
นอกจากนี้ยังมีรายงานกรณีเด็กชายอายุ 16 ปีที่เกิด PNC หลังได้รับวัคซีน COVID-19 (BNT162b2) 2) อย่างไรก็ตาม ความเสี่ยงของภาวะแทรกซ้อนทางระบบประสาทที่เกี่ยวข้องกับวัคซีนนั้นต่ำกว่าการติดเชื้อ COVID-19 เองมาก 2) .
เนื่องจากสาเหตุของเส้นประสาทสมองอักเสบมีความหลากหลาย จึงยังไม่มีมาตรการป้องกันเฉพาะ ในพื้นที่ที่มีโรคไลม์ ระบาด โปรดปฏิบัติตามมาตรการป้องกันเห็บอย่างเคร่งครัด หากมีอาการเช่น เห็นภาพซ้อน ใบหน้าเป็นอัมพาต หรือกลืนลำบากเกิดขึ้นอย่างกะทันหัน ให้ไปพบแพทย์ทันที
Q
COVID-19 กับเส้นประสาทสมองอักเสบมีความสัมพันธ์กันหรือไม่?
A
มีรายงานผู้ป่วยโรคเส้นประสาทสมองอักเสบ (โดยเฉพาะเส้นประสาทสมองอักเสบหลายเส้น) หลังการติดเชื้อ SARS-CoV-2 หลายราย1) 5) กลไกการเกิดโรคเชื่อว่าเกิดจากปฏิกิริยาทางภูมิคุ้มกันหลังการติดเชื้อเป็นหลัก มากกว่าการบุกรุกโดยตรงของไวรัส มีรายงานผู้ป่วยหลังการฉีดวัคซีน COVID-19 เช่นกัน แต่ความเสี่ยงต่ำกว่าการติดเชื้อเอง2)
การวินิจฉัยเส้นประสาทสมองอักเสบต้องอาศัยการตรวจทางคลินิกร่วมกับการตรวจภาพ การตรวจน้ำไขสันหลัง และการตรวจทางไฟฟ้าสรีรวิทยา
การตรวจ MRI ด้วยสารทึบรังสีเป็นการตรวจที่สำคัญที่สุด ในเส้นประสาทสมองอักเสบ การเพิ่มความเข้มของสารทึบรังสีในเส้นประสาทที่ได้รับผลกระทบเป็นลักษณะเฉพาะ การใช้ลำดับ MRI แบบ CI SS (constructive interference in steady state) สามารถแสดงเส้นประสาทสมองได้ชัดเจนยิ่งขึ้น
ประเด็นสำคัญในการถ่ายภาพ MRI มีดังนี้:
ภาพ T1-weighted และ T2-weighted เป็นพื้นฐานสำหรับโรคอักเสบ ให้ใช้วิธี FLAIR และ STIR ร่วมกันสำหรับโรคประสาทตาอักเสบ ภาพ T1-weighted ที่มีการระงับสัญญาณไขมันในแนวระนาบโคโรนัลมีประโยชน์เพื่อประเมินรอยโรคทำลายไมอีลิน การตัดภาพแนวขวางทั้งสมองด้วยวิธี FLAIR มีความสำคัญ
หากสงสัยสาเหตุจากหลอดเลือด ให้เพิ่ม CTA, MRA หรือการฉีดสีหลอดเลือดด้วยสายสวน CT มีประโยชน์ในการคัดกรองฉุกเฉิน
การตรวจน้ำไขสันหลังโดยการเจาะเอวเป็นสิ่งจำเป็นในการระบุโรคพื้นฐาน
การแยกตัวของโปรตีน-เซลล์ (โปรตีนเพิ่มขึ้นแต่จำนวนเซลล์ปกติ): บ่งชี้ชนิดย่อยของ GBS1) 3) การเพิ่มขึ้นของเซลล์ลิมโฟไซต์ : พบในมากกว่า 80% ของผู้ป่วยโรค Lyme ที่มีผลต่อระบบประสาท4) สารสื่อการอักเสบ : มีรายงานการเพิ่มขึ้นของ IL-8 ในน้ำไขสันหลังที่เกี่ยวข้องกับ COVID-195)
การตรวจ ความสำคัญหลัก MRI ด้วยสารทึบแสง การเพิ่มความเข้มของสารทึบแสงในเส้นประสาทสมองที่ได้รับผลกระทบ การตรวจน้ำไขสันหลัง การแยกตัวของโปรตีน-เซลล์ การแยกการติดเชื้อ การศึกษาการนำกระแสประสาท การประเมินการทำลายปลอกไมอีลินและความเสียหายของแอกซอน การตรวจแอนติบอดี การตรวจหาแอนติบอดีต่อแกงกลิโอไซด์
ในการศึกษาความเร็วการนำกระแสประสาท การหายไปของคลื่น F เป็นการค้นพบที่สำคัญในระยะแรกของการทำลายปลอกไมอีลินส่วนต้น2) การตรวจรีเฟล็กซ์กระพริบตาประเมินความผิดปกติของการตอบสนอง R1 และ R23)
การวัดแอนติบอดีต่อแกงกลิโอไซด์ (anti-GM1, anti-GQ1b, anti-GD1a เป็นต้น) มีประโยชน์ในการวินิจฉัยชนิดย่อยของ GBS3) อย่างไรก็ตาม การตรวจไม่พบแอนติบอดีไม่ได้ตัดการวินิจฉัย PNC
ในการค้นหาสาเหตุจากการติดเชื้อ จะตรวจทางซีรั่มวิทยาของโรคลายม์ การตรวจซิฟิลิส แอนติบอดีต่อ AQP4 และแอนติบอดีต่อ MOG ตามความเหมาะสม
การรักษาโรคเส้นประสาทสมองอักเสบขึ้นอยู่กับการรักษาโรคที่เป็นสาเหตุเป็นรายบุคคล
โรคลายม์ (Neuroborreliosis) : การรักษามาตรฐานคือ ceftriaxone ทางหลอดเลือดดำ 14-28 วัน 4) การรับประทาน doxycycline ก็เป็นทางเลือกหนึ่งซิฟิลิส : ให้ penicillin อย่างทั่วร่างกาย หากใช้สเตียรอยด์ ร่วมด้วย ต้องแยกการติดเชื้อออกก่อนไวรัสเริม : แนะนำให้ใช้ acyclovir
การให้อิมมูโนโกลบูลินทางหลอดเลือดดำ (IVI G) : 0.4 กรัม/กก./วัน เป็นเวลา 5 วัน 1) 3) เป็นทางเลือกแรกสำหรับ PNC ที่เป็นชนิดย่อยของ GBSการแลกเปลี่ยนพลาสมา IVI G 3)
การให้สเตียรอยด์ แบบพัลส์ : methylprednisolone 1,000 มก./วัน ทางหลอดเลือดดำเป็นเวลา 3 วัน มีประสิทธิภาพโดยเฉพาะเมื่อมีเส้นประสาทตา อักเสบร่วมด้วยหลังการให้สเตียรอยด์ แบบพัลส์ ให้เริ่มรับประทาน prednisolone 0.5 มก./กก./วัน แล้วลดลง 5-10 มก. ทุก 3-4 วัน
ไม่ให้การรักษาด้วยสเตียรอยด์ ชนิดรับประทานเพียงอย่างเดียว เพราะเพิ่มความเสี่ยงของการกลับเป็นซ้ำของเส้นประสาทตา อักเสบ
ก่อนให้สเตียรอยด์ อย่างทั่วร่างกาย จำเป็นต้องแยกการติดเชื้อ เช่น ไวรัสตับอักเสบบี
การใช้สเตียรอยด์ ทั่วร่างกายอาจทำให้เกิดผลข้างเคียง เช่น แผลในกระเพาะอาหาร กระดูกพรุน น้ำตาลในเลือดสูง ต้อหิน และต้อกระจก ในโรคเส้นประสาทสมองอักเสบจากการติดเชื้อ การกดภูมิคุ้มกันด้วยสเตียรอยด์ อาจทำให้การติดเชื้อแย่ลง ดังนั้นต้องแยกการติดเชื้อออกก่อน สำหรับ IVI G ต้องระวังผลข้างเคียง เช่น ปวดศีรษะ ไข้ และลิ่มเลือดอุดตัน
Q
การรักษาโรคเส้นประสาทสมองอักเสบสามารถคาดหวังการฟื้นตัวได้หรือไม่?
A
ด้วยการระบุสาเหตุและการรักษาที่เหมาะสม ผู้ป่วยส่วนใหญ่จะมีอาการทางระบบประสาทดีขึ้น ในชนิดย่อย PNC ของ GBS มีรายงานจำนวนมากที่แสดงการปรับปรุงอย่างชัดเจนหลัง IVI G1) 3) อย่างไรก็ตาม ในกรณีที่มีความบกพร่องทางการมองเห็น การฟื้นฟูการมองเห็น อาจไม่สมบูรณ์3)
พยาธิสรีรวิทยาของโรคเส้นประสาทสมองอักเสบแตกต่างกันไปตามสาเหตุ แต่กลไกหลักมีดังนี้
การทำลายปลอกไมอีลินคือการทำลายปลอกไมอีลินที่หุ้มแอกซอนของเส้นประสาทที่มีปลอกไมอีลิน เมื่อปลอกไมอีลินถูกทำลาย การนำกระแสประสาทแบบกระโดดจะไม่สามารถเกิดขึ้นได้ ทำให้เกิดความผิดปกติของการนำกระแสประสาท ในชนิดย่อย PNC ของ GBS ชนิดทำลายปลอกไมอีลินเป็นหลัก และทางอิเล็กโทรสรีรวิทยาจะพบการหายไปของคลื่น F การบล็อกการนำ และการยืดระยะเวลาแฝงปลาย2) 5) ในขณะที่ชนิดแอกซอนมีลักษณะเฉพาะคือแอมพลิจูดของศักย์ไฟฟ้ากล้ามเนื้อรวมลดลง5)
ในโรคเส้นประสาทสมองอักเสบหลังการติดเชื้อ การเลียนแบบโมเลกุล (molecular mimicry) เป็นกลไกทางพยาธิวิทยาที่สำคัญ เนื่องจากความคล้ายคลึงกันทางโครงสร้างระหว่างไกลโคลิพิดที่เชื้อก่อโรคติดเชื้อก่อนหน้ามีกับแกงกลิโอไซด์ที่อยู่ในปลอกไมอีลินของเส้นประสาทสมอง จึงเกิดการสร้างแอนติบอดีตนเองที่ทำปฏิกิริยาข้าม3)
แอนติบอดีต่อต้านแกงกลิโอไซด์หลักที่ตรวจพบใน PNC คือ IgG ต่อต้าน GQ1b (47%) รองลงมาคือ IgG ต่อต้าน GT1a และ GD1a3) แอนติบอดีเหล่านี้กำหนดเป้าหมายไปที่ปลอกไมอีลินของเส้นประสาทสมองและทำให้เกิดการทำลายปลอกไมอีลินที่อาศัยคอมพลีเมนต์
กลไกของโรคเส้นประสาทสมองอักเสบหลัง COVID-19 ยังไม่เป็นที่เข้าใจอย่างสมบูรณ์
De Gennaro และคณะ (2021) รายงานผู้ป่วยโรคเส้นประสาทสมองอักเสบหลายเส้นหลังปอดอักเสบรุนแรงจาก COVID-19 จำนวน 2 ราย อาการทางระบบประสาทปรากฏขึ้นประมาณหนึ่งเดือนหลังการติดเชื้อ และการตรวจ PCR สำหรับ SARS-CoV-2 ให้ผลลบ เนื่องจากการปรับปรุงอย่างชัดเจนหลัง IVI G พวกเขาสรุปว่ากลไกทางภูมิคุ้มกันหลังการติดเชื้อเป็นสาเหตุหลัก แทนที่จะเป็นการบุกรุกเส้นประสาทโดยตรง1)
กลไกที่เป็นไปได้มีดังนี้1)
การบุกรุกเส้นประสาทผ่านตัวรับ ACE2 : โปรตีนหนามของ SARS-CoV-2 สามารถจับกับตัวรับ ACE2 ที่แสดงออกในระบบประสาทส่วนกลางและระบบประสาทส่วนปลาย และบุกรุกแบบย้อนกลับจากปลายประสาทปฏิกิริยาที่มีภูมิคุ้มกันเป็นสื่อกลาง : เกิดการตอบสนองทางภูมิคุ้มกันที่ผิดปกติแบบช้า คล้ายกับ GBS และ MFSการกระตุ้นไซโตไคน์แบบต่อเนื่อง : มีรายงานการเพิ่มขึ้นของ IL-8 ในน้ำไขสันหลัง ซึ่งบ่งชี้ถึงการมีส่วนร่วมของไซโตไคน์ที่ก่อให้เกิดการอักเสบ5)
Q
ทำไมเส้นประสาทสมองถึงถูกทำลายหลังการติดเชื้อ?
A
ในโรคปลายประสาทสมองอักเสบหลังการติดเชื้อ กลไกหลักที่คิดว่าเป็นคือการเลียนแบบโมเลกุล ความคล้ายคลึงกันทางโครงสร้างระหว่างไกลโคลิพิดของเชื้อโรคและแกงกลิโอไซด์ของปลอกไมอีลินของเส้นประสาทสมอง ทำให้เกิดการผลิตแอนติบอดีตนเองที่ทำปฏิกิริยาข้ามกัน ซึ่งทำให้เกิดการทำลายไมอีลินของเส้นประสาทสมอง3) การตอบสนองที่ดีต่อการให้ IVI G ก็สนับสนุนกลไกทางภูมิคุ้มกันนี้1)
เนื้อหาต่อไปนี้ยังอยู่ในขั้นตอนการวิจัยหรือการทดลองทางคลินิก และไม่ใช่การรักษามาตรฐานที่สามารถรับได้ในโรงพยาบาลทั่วไป เป็นข้อมูลอ้างอิงสำหรับผู้เชี่ยวชาญเกี่ยวกับการพัฒนาทางการแพทย์ในอนาคต
Manganotti และคณะ (2021) รายงานผู้ป่วย COVID-19 5 รายที่มีภาวะแทรกซ้อน GBS/PNC สี่รายได้รับ IVI G (0.4 กรัม/กก. เป็นเวลา 5 วัน) และอาการทางระบบประสาทดีขึ้น พบการเพิ่มขึ้นของ IL-8 ในน้ำไขสันหลังใน 3 ราย ซึ่งบ่งชี้ถึงโรคเส้นประสาทส่วนปลายที่มีภูมิคุ้มกันเป็นสื่อกลางที่เกี่ยวข้องกับการติดเชื้อ SARS-CoV-25)
Kulsirichawaroj และคณะ (2022) รายงานกรณีหญิงไทยอายุ 16 ปีที่เกิด PNC 3 ชั่วโมงหลังจากได้รับวัคซีน mRNA BNT162b2 ครั้งแรก เธอมีความผิดปกติของเส้นประสาทสมองคู่ที่ V, VII, IX, X ด้านขวา คลื่น F หายไป และมีการเพิ่มความเข้มของเส้นประสาทเฟเชียลด้านขวา หลังจากให้ IVI G อาการทั้งหมดยกเว้นอัมพาตใบหน้าหายไปภายใน 4 สัปดาห์2)
Li และคณะ (2023) รายงานกรณีที่พบได้ยากของชายอายุ 54 ปีที่มี PNC ร่วมกับการมองเห็น บกพร่อง แอนติบอดี IgG ต่อต้าน GM1 และต่อต้าน GD1a ในซีรัมเป็นบวก และอาการทางระบบประสาทดีขึ้นอย่างรวดเร็วหลังจากให้ IVI G การฟื้นฟูการมองเห็น ต้องใช้สเตียรอยด์ เพิ่มเติม แต่หลังจากหนึ่งเดือน การมองเห็น ฟื้นตัวเต็มที่เป็น 6/6 ในทั้งสองตา3) ในการทบทวนวรรณกรรม จาก 32 กรณีของ GBS ร่วมกับประสาทตาอักเสบ การพยากรณ์โรคทางสายตาไม่ดีใน 47% ในขณะที่การพยากรณ์โรคของอาการทางระบบประสาทโดยทั่วไปดี
De Gennaro R, Gastaldo E, Tamborino C, et al. Selective cranial multineuritis in severe COVID-19 pneumonia: two cases and literature review. Neurol Sci. 2021;42(5):1643-1648.
Kulsirichawaroj P, Sanmaneechai O, Wittawatmongkol O, et al. Polyneuritis cranialis associated with BNT162b2 mRNA COVID-19 vaccine in a healthy adolescent. Vaccines. 2022;10(1):134.
Li H, Li Z, Huang B, et al. Co-occurrence of polyneuritis cranialis and visual impairment: a case report and literature review. Neurol Sci. 2023;44(5):1563-1574.
Omotosho YB, Sherchan R, Ying GW, et al. A unique case of Bannwarth syndrome in early disseminated Lyme disease. Cureus. 2021;13(4):e14680.
Manganotti P, Bellavita G, D’Acunto L, et al. Clinical neurophysiology and cerebrospinal liquor analysis to detect Guillain-Barré syndrome and polyneuritis cranialis in COVID-19 patients: a case series. J Med Virol. 2021;93(2):766-774.