조기 발병형
황반병증: 가장 특징적인 소견. 생후 35일부터 나타날 수 있습니다.
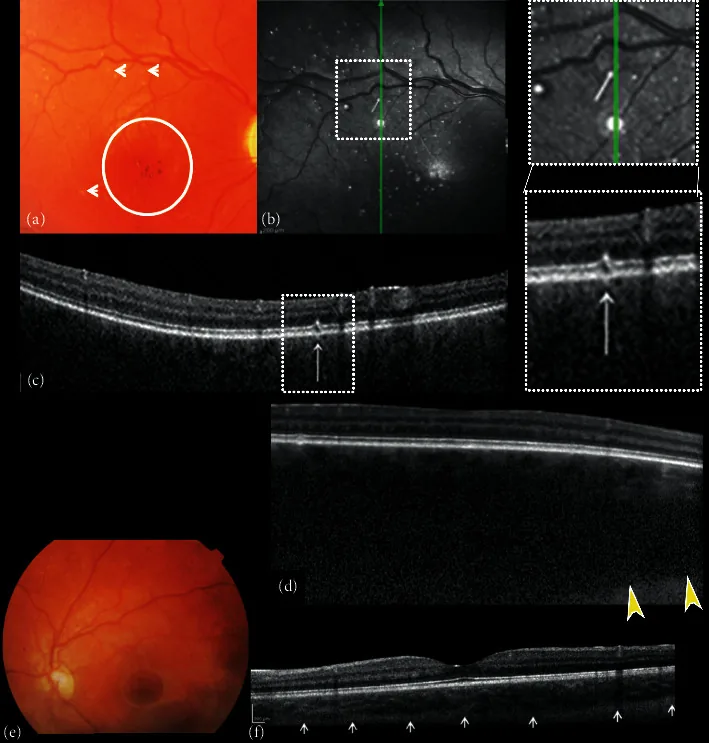
황소눈 모양 황반병증: 중심부 맥락망막 위축과 색소 고리를 보이는 특징적인 패턴입니다.
망막색소변성 유사 변화: 광범위한 망막 변성이 발생합니다.
시신경 위축: 진행된 사례에서 관찰됩니다.
안저 형광조영(FAF) : 중심와 저자발광, 경계부 과자발광 패턴.

코발라민 C 결핍증(cblC형)은 세포 내 비타민 B12(코발라민) 대사의 선천성 대사 오류입니다. 공식 명칭은 메틸말론산뇨증 및 호모시스틴뇨증 cblC형(OMIM #277400)입니다. 전체 cbl 대사 이상의 약 80%를 차지하는 가장 흔한 유형입니다.
유전 양식은 상염색체 열성입니다. 원인은 MMACHC 유전자(1p34.2)의 돌연변이입니다. MMACHC 단백질은 세포 내 코발라민 대사의 초기 단계를 담당하며, 기능 상실로 인해 아데노실코발라민(AdoCbl)과 메틸코발라민(MeCbl)의 합성이 모두 손상됩니다.
추정 발생률은 1:100,000 ~ 1:200,000으로 알려져 있지만 3, 4), 중국 산둥성 조사에서는 1:3,920으로 높은 빈도가 보고되었습니다. 미국에서는 2000년대 초반부터 신생아 선별검사(NBS) 대상이 되었습니다 4).
발병 연령에 따라 조기 발병형(생후 1년 이내, 전체의 86~88%)과 지연 발병형(1세 이후)으로 크게 나뉩니다. 지연 발병형은 160예 이상, 성인 발병(18세 이상)은 30예 이상 보고되었습니다 3).
혈중 C3 프로피오닐카르니틴 상승을 지표로 한 NBS를 통해 조기 발견이 가능합니다. 그러나 지연 발병형이나 경증형에서는 NBS를 통과하는 경우가 있어 4), 선별검사가 정상이더라도 임상적으로 의심되는 경우 혈장 Hcy 및 소변 MMA 추가 검사가 필요합니다.
발병 연령에 따라 임상 양상이 크게 다릅니다.
조기 발병형 안구 증상:
지발형 주요 증상(안외):
조기 발병형과 지발형은 안저 소견이 크게 다릅니다.
조기 발병형
황반병증: 가장 특징적인 소견. 생후 35일부터 나타날 수 있습니다.
황소눈 모양 황반병증: 중심부 맥락망막 위축과 색소 고리를 보이는 특징적인 패턴입니다.
망막색소변성 유사 변화: 광범위한 망막 변성이 발생합니다.
시신경 위축: 진행된 사례에서 관찰됩니다.
안저 형광조영(FAF) : 중심와 저자발광, 경계부 과자발광 패턴.
지연형
안저 정상인 경우가 많음 : 심각한 안소견을 보이지 않는 경우가 많음 3, 4).
척수 MRI 소견 : 후삭의 고신호 병변이 특징적 4).
뇌 MRI 백질 병변 : 일부 지연형에서 관찰됨 3).
고혈압성 망막병증 : 신장 합병증(혈전성 미세혈관병증)을 동반한 중증 환자에서 발생 가능 2).
전신 합병증으로 대사성 산증, 근긴장저하, 소두증, 심근병증(50%) 1), 신혈전성 미세혈관병증(TMA) 2)이 알려져 있음.
지연형에서는 조기발현형과 같은 심각한 황반병증·망막변성은 드물고, 안저 정상인 경우가 많음 3, 4). 그러나 신장 합병증을 동반한 중증 환자에서는 고혈압성 망막병증이 나타날 수 있음 2). 신경 증상은 치료 반응이 좋은 경우가 많지만, 시기능 장애가 잔존한 예도 보고됨 3).
코발라민 C 결핍증은 MMACHC 유전자의 돌연변이에 의한 상염색체 열성 유전 질환입니다. 80개 이상의 돌연변이가 보고되었으며, 돌연변이 유형에 따라 표현형이 크게 다릅니다.
주요 돌연변이의 빈도와 해당 표현형은 아래와 같습니다.
| 돌연변이 | 빈도/계통 | 주요 표현형 |
|---|---|---|
| c.271dupA | 40~61%·유럽계 | 조기 발병·가장 중증 |
| c.394C>T | 약 20% | 후기 발현형 |
| c.609G>A | 48~55%·동아시아계 | 영아기~소아기 |
기타 주요 변이로는:
또한, PRDX1 유전자 변이로 인한 MMACHC의 후성유전적 침묵이 원인이 되는 ‘epi-cblC’도 존재하며, 이차성 cblC 유사 병태를 유발합니다.
대사 이상을 나타내는 검사 소견이 진단의 중심이 됩니다.
| 검사 항목 | 전형적 소견 | 의의 |
|---|---|---|
| 혈장 Hcy | 현저히 상승 | 선별검사 |
| 요중 MMA | 상승 | 대사 차단 확인 |
| 유전자 검사 | MMACHC 돌연변이 | 확진 |
보고된 구체적 수치: 혈장 Hcy 101.51700.5 µmol/L2, 3), 요중 MMA 85802 mmol/mol3, 4). 지발형에서는 혈청 비타민 B12가 정상 범위인 경우가 많다 (448~625 pg/mL)3, 4).
식이성 B12 결핍, 악성 빈혈, 기타 cbl 대사 이상(cblD, cblF 등) 및 MTHFR 결핍증과의 감별이 중요합니다3, 4). Hcy 상승과 MMA 상승의 조합은 cblC에 특징적이며, Hcy 상승만 있고(MMA 정상)는 MTHFR 결핍 등을 시사합니다.
있습니다. 지발형 cblC에서는 혈청 B12가 정상 범위에 있는 경우가 많으며3, 4), B12 정상만으로 배제해서는 안 됩니다. 신경 증상이나 정신 증상이 있는 젊은 환자에서는 혈장 Hcy와 MMA를 반드시 측정하고, 상승되어 있으면 유전자 검사로 MMACHC를 분석해야 합니다.
치료의 주축은 히드록시코발라민(OH-Cbl)의 비경구 투여이며, 베타인, 폴린산, L-카르니틴을 병용하는 다제 병용 요법이 시행됩니다.
비경구 투여가 기본입니다. 투여량 기준: 1 mg/일 또는 0.3 mg/kg/일 근육 주사(IM) 4). 보고된 투여량:
Ailliet 등(2022)은 지발형 성인 환자에서 25 mg/일 피하 주사(SC)를 시행하여 신경 증상의 개선을 얻었습니다3). Goyne 등(2023)의 증례에서는 5 mg/일 IM으로 시작했습니다4). Hjalmarsson 등(2024)의 중증 심부전 합병 증례에서는 30 mg/일 정맥 투여(IV)가 이루어졌습니다1).
호모시스테인의 메티오닌으로의 재메틸화를 촉진합니다. 투여량 기준: 250 mg/kg/일을 3회 분할4). 보고된 투여량: 100 mg/kg/일2), 1 g×3회4), 2~3 g×3회1).
치료 목표는 MMA와 Hcy를 낮추고 대사 지표를 정상화하는 것입니다. 적절한 치료를 통해 Hcy가 현저히 감소합니다:
Akar 등(2024)의 신장 TMA를 동반한 중증 사례에서는 치료 시작 후 Hcy가 1,700.5에서 4.6 µmol/L로 정상화되었습니다2). Hjalmarsson 등(2024)의 심근병증 동반 사례에서는 MMA가 97에서 8.1 mmol/mol, Hcy가 91에서 31.8 µmol/L로 개선되었습니다1).
후발형은 치료 반응이 비교적 좋지만4), 시기능 회복은 제한적일 수 있습니다3). 조기 발현형은 적절한 치료에도 불구하고 10대에 법적 실명에 이르는 경우가 많습니다.
조기 발현형에서는 대사 지표가 개선되어도 황반병증 및 망막 변성의 시기능 예후가 불량한 경우가 많으며, 10대에 법적 실명에 이르는 사례가 보고되었습니다. 후발형에서는 신경 증상에 대한 치료 반응이 비교적 좋지만, 잔존 시기능 장애는 제한적으로만 회복됩니다3). 조기 진단 및 조기 치료 시작이 최상의 예후를 가져올 수 있습니다.
MMACHC 단백질은 리소좀에서 코발라민-합토코린(R) 복합체와 결합하여 코발라민에서 R기를 절단하고 세포 내에서 이용 가능한 공통 코발라민 중간체를 생성합니다. 이 중간체는 이후 두 가지 경로로 분기됩니다.
MMACHC 기능 상실로 두 경로 모두 손상되면:
안구 조직에 미치는 영향으로는 메티오닌 감소로 인한 글루타티온(GSH) 합성 장애가 망막색소상피(RPE)의 산화 스트레스 방어를 저하시켜 황반변성의 원인이 되는 것으로 생각됩니다. 고Hcy에 의한 혈관내피 손상이 망막 및 맥락막 순환을 손상시키는 기전도 추정됩니다.
Hjalmarssон 등(2024)은 심근병증을 동반한 cblC 환자에서 LVAD(좌심실 보조 장치) 이식 후 심장 이식을 시행한 세계 최초의 증례를 보고했습니다1). 고용량 OH-Cbl(30 mg/일 IV), 베타인, 폴린산, L-카르니틴의 대사 치료와 병용하여 대사 지표 개선(MMA 97→8.1, Hcy 91→31.8)과 함께 좋은 결과를 얻었습니다.
심장 이식 후에도 cblC에 대한 대사 치료의 지속이 필수적임이 나타났습니다1).
지발형 및 경증형에서는 신생아 선별검사에서 놓치는 경우가 있음이 보고되었으며4), 신경 증상 또는 정신 증상을 보이는 젊은 성인에서 B12가 정상이더라도 Hcy와 MMA를 측정하는 것의 중요성이 강조됩니다3, 4).
PRDX1 유전자 돌연변이로 인한 MMACHC의 후성유전적 침묵으로 발생하는 ‘epi-cblC’가 보고되었다. 유전자 돌연변이가 없어도 cblC 유사 병태를 나타낼 수 있으므로 진단 알고리즘의 재고가 요구된다.
Ailliet 등(2022)은 지연형 cblC의 가족 선별검사를 통해 무증상 동형접합체를 조기 발견한 경험을 보고하고, 프로밴드 진단을 계기로 한 적극적인 가족 선별검사의 의의를 강조하였다3).