外因性眼内炎
急性術後型:白内障手術後が最多。術後6週以内に発症する。
遅発型(慢性術後型):手術後数週〜数ヶ月以上を経て発症。P. acnes などが原因となる。
外傷性:眼球穿孔創から病原体が直接侵入。成人の発生率0.9〜18%、小児では5〜54%に達する。2)
濾過胞関連・硝子体内注射後:抗VEGF薬投与後の発生が増加傾向にある。

眼内炎(Endophthalmitis)は、硝子体腔や前房を含む眼内液に炎症細胞が大量浸潤した化膿性炎症の総称である。進行が速く、適切な治療が遅れると短期間で不可逆的な視力障害に至る眼科救急の代表疾患である。
発症経路から大きく外因性と内因性の2つに分類される。
外因性眼内炎
急性術後型:白内障手術後が最多。術後6週以内に発症する。
遅発型(慢性術後型):手術後数週〜数ヶ月以上を経て発症。P. acnes などが原因となる。
外傷性:眼球穿孔創から病原体が直接侵入。成人の発生率0.9〜18%、小児では5〜54%に達する。2)
濾過胞関連・硝子体内注射後:抗VEGF薬投与後の発生が増加傾向にある。
内因性眼内炎
細菌性:菌血症の0.04〜0.5%に合併する。1) 肺・肝・心内膜炎など他臓器感染巣からの血行性播種。
真菌性:カンジダ属が多く、免疫抑制患者や長期中心静脈カテーテル留置例に発症しやすい。
K. pneumoniae関連:台湾での12年間データではEEの55.8%を占める。1) 糖尿病・肝膿瘍との関連が深い。
内因性眼内炎(Endogenous Endophthalmitis; EE)は菌血症症例の0.04〜0.5%に発症し1)、高病毒性型 K. pneumoniae(hvKP)による肝膿瘍(PLA)合併例では EE 発生率が3.4〜12.6%に達する。3)
白内障手術後が最も多いが、外傷・抗VEGF薬硝子体内注射・濾過胞関連など多様な外因性経路がある。さらに全身の感染巣から血液を介して眼内に播種する内因性眼内炎も存在し、糖尿病患者や免疫抑制患者では特に注意が必要である。
Endophthalmitis Vitrectomy Study(EVS)における術後眼内炎の症状頻度を以下に示す。
| 症状 | 頻度(EVS) |
|---|---|
| 霧視 | 94.3% |
| 充血 | 82.1% |
| 眼痛 | 74% |
| 眼瞼腫脹 | 34.5% |
EVSのデータでは眼痛は74%に認められるが、25%以上の症例では疼痛がない。術後や注射後に急激な視力低下・充血が生じた場合は、疼痛がなくても眼内炎を積極的に疑って受診する必要がある。
主要な臨床所見の頻度(EVS)を以下に示す。
| 所見 | 頻度(EVS) |
|---|---|
| 前房蓄膿 | 85% |
| 透光体混濁(硝子体炎) | 79% |
| 光覚弁以下の視力 | 26% |
EVS(白内障術後眼内炎)での培養陽性例の菌種分布:
610眼を対象とした多施設研究では、高毒性菌による感染で重度視力低下(LP以下)のオッズ比が4.48、網膜剥離または眼球摘出のオッズ比が1.90であった。4)
予後不良因子:
白内障手術後眼内炎はまれだが重篤である。ESCRSは、術後眼内炎リスクを下げるため、手術終了時の前房内抗菌薬投与を推奨している8)。
受診時視力の評価が治療方針決定で最重要である。EVSの知見から、光覚弁(LP)以下か手動弁(HM)以上かの区別が治療選択の分岐点となる(「標準的な治療法」の項参照)。
前房蓄膿の程度・角膜浮腫・フィブリン析出などを評価する。隅角鏡を用いると隅角内の蓄膿(angle hypopyon)を検出できる。
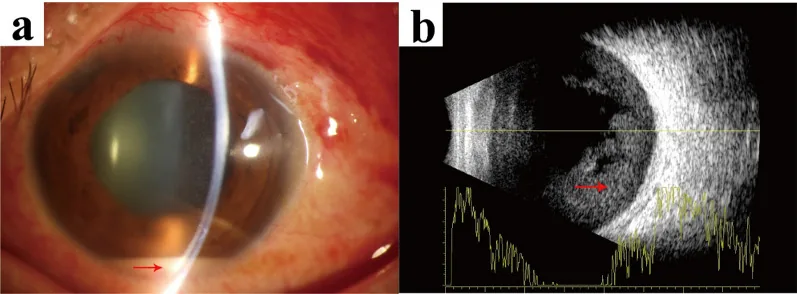
硝子体炎や角膜浮腫で眼底が透見困難な場合に、硝子体内エコーの評価・網膜剥離の有無の確認に必須の検査となる。
術後早期の前房炎症においてTASSとの鑑別が重要である。5)
TASSは手術翌日(12〜24時間以内)に発症し、硝子体炎を伴わない点が眼内炎との主要な鑑別点である。5) TASSはステロイド点眼に反応するが、眼内炎では抗菌薬の早期投与が不可欠であり、両者の見分けは治療方針に直結する。疑わしい場合は硝子体穿刺による検体採取を行う。
EVSの推奨に基づく治療選択(白内障術後・二次眼内レンズ挿入後眼内炎):5)
Tap & Inject
適応:受診時視力が手動弁(HM)以上の症例。
処置:硝子体穿刺(tap)+硝子体内抗菌薬注入(inject)を行う。
EVSでは視力HM以上の群で、即時硝子体切除術とTap&Injectの最終視力に有意差なし。侵襲の少ない治療として第一選択となる。
即時硝子体切除術
適応:受診時視力が光覚弁(LP)以下の症例。
効果:硝子体切除術群で20/40以上の視力を達成した割合が33%、Tap群では11%。5)
即時の硝子体手術により硝子体内の起炎菌・炎症物質を除去する。日本では視力予後の改善を期待して早期硝子体手術を行う施設も多い。
投与量の標準的なプロトコールを以下に示す。
| 薬剤 | 硝子体内投与量 |
|---|---|
| バンコマイシン | 1.0 mg/0.1 mL |
| セフタジジム | 2.25 mg/0.1 mL |
| アムホテリシンB | 5〜10 μg/0.1 mL |
| ボリコナゾール | 50〜100 μg/0.1 mL |
ESCRSガイドライン(2024)では以下を推奨している:8)
全身感染症の管理が最優先となる。IDSA推奨では K. pneumoniae 肝膿瘍(PLA)合併EEに対し、抗菌薬を4〜6週間投与する。1) 眼局所治療(硝子体内抗菌薬注入・硝子体手術)と全身治療を並行して行う。
علاوه بر درمان موضعی چشم با ویترکتومی و تزریق آنتیبیوتیک داخل زجاجیهای، درمان آنتیبیوتیکی سیستمیک برای بیماری زمینهای (مانند آبسه کبدی یا باکتریمی) به مدت ۴ تا ۶ هفته استاندارد است. 1) مدیریت بیماریهای زمینهای مانند دیابت و وضعیت سرکوب ایمنی نیز همزمان انجام میشود و همکاری با متخصص عفونی ضروری است.
در حین جراحی یا تروما، باکتریهای معمول اطراف چشم وارد داخل چشم شده و در حفره زجاجیه و اتاق قدامی که از نظر ایمنی ایزوله هستند، به سرعت تکثیر مییابند. از آنجا که مکانیسمهای دفاعی داخل چشم در برابر استافیلوکوکها ضعیف است، حتی مقدار کمی باکتری نیز میتواند باعث عفونت شود.
باکتریهای بسیار سمی پس از جراحی گلوکوم و ویترکتومی نسبتاً شایعتر هستند، که تصور میشود به دلیل اختلال در سد ملتحمه در این جراحیها باشد که ورود باکتریهای دهانی و محیطی را تسهیل میکند.4)
عوامل بیماریزا از کانونهای عفونت در سایر اندامها (مانند آبسه کبد، پنومونی، اندوکاردیت) از طریق جریان خون به داخل چشم منتشر میشوند. معمولاً عفونت از بخش خلفی چشم از طریق عروق شبکیه شروع شده و به یووه و زجاجیه گسترش مییابد.
عوامل حدت hvKP (کلبسیلا پنومونیه با حدت بالا):
در دیابت، افزایش نفوذپذیری عروق ناشی از هیپرگلیسمی، ورود hvKP به عروق شبکیه را تسهیل میکند 3) و کاهش عملکرد نوتروفیلها، دفاع در برابر عفونت را تضعیف میکند. این یکی از دلایل شیوع بالای EE همراه با PLA در بیماران دیابتی محسوب میشود.
Yap و همکاران (2025) در یک مطالعه چندمرکزی روی 610 چشم گزارش کردند که اندوفتالمیت ناشی از باکتریهای بسیار سمی (باکتریهای دهانی، استرپتوکوک و غیره) در مقایسه با باکتریهای کمسمیت، شانس کاهش شدید بینایی (LP یا کمتر) را 4.48 برابر و شانس جداشدگی شبکیه یا تخلیه چشم را 1.90 برابر افزایش میدهد. 4) میزان کشت مثبت 48.5% (296 از 610 چشم) بود. این یافته نشان میدهد که تخمین عامل عفونی در زمان مراجعه (بر اساس روش جراحی، مکانیسم آسیب و سیر بالینی) به پیشبینی پیشآگهی کمک میکند.
مطالعهای با استفاده از IRIS Registry (2025) گزارش کرد که در ۱۰۴۴ مورد اندوفتالمیت پس از تزریق داخل زجاجیهای داروی ضد VEGF، بین انجام ویترکتومی زودهنگام و تنها تزریق آنتیبیوتیک داخل زجاجیهای تفاوت معنیداری در حدت بینایی نهایی وجود نداشت. 6) این یافته نشان میدهد که در مواردی که حدت بینایی در زمان مراجعه خوب است، روش Tap & Inject ممکن است از تهاجم بیش از حد جلوگیری کند.
Blanch و همکاران (Ophthalmology) در یک مرور سیستماتیک شامل 8497 چشم، زمان انجام بخیه اولیه در آسیبهای باز چشم را مقایسه کرده و تأثیر آن را بر بروز اندوفتالمیت بررسی کردند.7) بخیه زودهنگام برای جلوگیری از ورود عوامل بیماریزا به داخل چشم از نظر کاهش خطر عفونت توصیه میشود.
لو و همکاران (2025) موردی از عفونت سیستمیک و اندوفتالمیت ناشی از جنس Paenibacillus را گزارش کردند و این گونه نادر باکتریایی را که با کشت به سختی قابل شناسایی بود، با استفاده از mNGS (توالییابی نسل بعدی متاژنومیک) شناسایی کردند.2) mNGS به عنوان یک فناوری امیدوارکننده برای یافتن علت اندوفتالمیت کشت-منفی مورد توجه قرار گرفته است.