PSS型(類似Posner-Schlossman症候群)
發病年齡:20~50歲的年輕男性
眼壓:顯著升高至40~60 mmHg(有時超過60 mmHg)
前房發炎:相對輕微(細胞2+或以下)
KP:不帶色素的小至中型灰白色肉芽腫性KP
病程:反覆緩解和復發的發作型
眼壓特徵:緩解期眼壓低於對側眼。隅角開放,無周邊虹膜前粘連。

巨細胞病毒(CMV,人類皰疹病毒5型)是一種屬於皰疹病毒科的DNA病毒。40歲以上成人血清陽性率達80-85%。
在免疫功能低下者中,它已知可引起壞死性視網膜炎(CMV視網膜炎)。近年來,免疫功能正常者中也出現CMV引起的虹膜睫狀體炎和角膜內皮炎,常伴有眼壓升高,並易遷延或復發。葡萄膜炎診療指南將CMV與HSV、VZV一同列為皰疹性前部葡萄膜炎的獨立病因3)。
CMV前部葡萄膜炎在亞洲報告較多,日本、中國和新加坡的病例系列研究領先。高CMV血清陽性率和遺傳易感性可能有關。
大多數報告病例為男性,發病年齡呈雙峰分佈。復發性急性型多見於30-50歲,慢性高眼壓型多見於50-70歲。
Posner-Schlossman症候群(PSS)是一種單眼、復發性虹膜炎伴急性眼壓升高,長期被視為特發性疾病。在PSS患者房水中檢測到CMV的報告相繼出現,導致人們認為它可能與CMV前部葡萄膜炎是同一疾病或存在重疊3)。兩者都具有前房炎症輕微伴眼壓升高等共同特徵。單純的PSS通常預後良好,不合并角膜內皮損傷,但在CMV確認的病例中,內皮細胞損傷可能成為問題。
CMV前部葡萄膜炎比HSV和VZV起病更隱匿,常呈慢性病程。由於缺乏疱疹典型的角膜知覺減退、水皰和皮疹,容易誤診1)。
PSS型(類似Posner-Schlossman症候群)
發病年齡:20~50歲的年輕男性
眼壓:顯著升高至40~60 mmHg(有時超過60 mmHg)
前房發炎:相對輕微(細胞2+或以下)
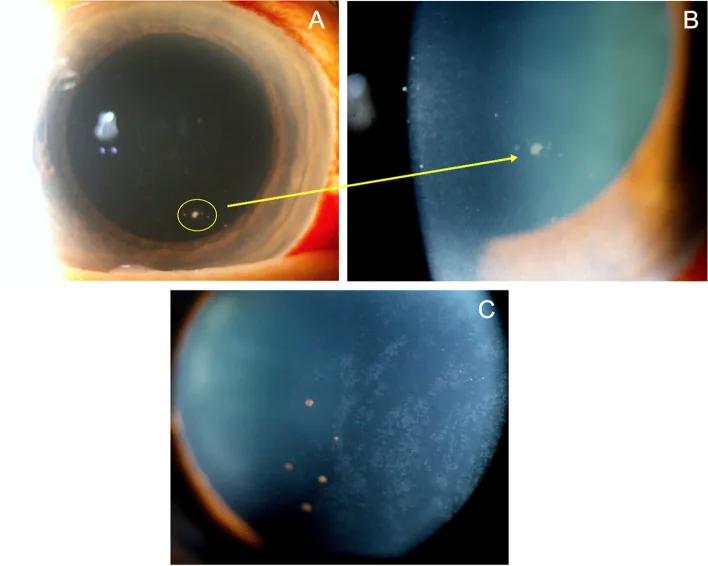
KP:不帶色素的小至中型灰白色肉芽腫性KP
病程:反覆緩解和復發的發作型
眼壓特徵:緩解期眼壓低於對側眼。隅角開放,無周邊虹膜前粘連。
FUS型(Fuchs葡萄膜炎症候群樣)
VZV葡萄膜炎中,角膜感覺減退、帶狀皮疹和扇形虹膜萎縮是鑑別線索,但CMV前葡萄膜炎缺乏這些表現。硬幣狀KP(KP corrals)和線狀KP是CMV角膜內皮炎的特徵性表現。阿昔洛韋或伐昔洛韋治療無效也是積極懷疑CMV的依據。確診必須進行房水定量PCR檢測,定性PCR可能出現偽陽性,因此必須使用定量方法1)。
CMV潛伏感染骨髓系前驅細胞(單核細胞/巨噬細胞前驅)。通過尚未完全闡明的機制,病毒在前眼部的巨噬細胞和樹突狀細胞內再激活,釋放干擾素-γ和干擾素-β,導致前眼部炎症。其他部位的感染也可能誘導循環單核細胞中的CMV再激活。
可能誘發再激活的藥物(有報導):
其他風險因素:
目前尚無針對CMV的市售疫苗。維持全身免疫狀態是一級預防的基礎。
若懷疑感染性前葡萄膜炎且符合以下任一條件,應考慮前房穿刺1):
一項針對全球75名葡萄膜炎專家的德爾菲調查顯示,73.3%的專家對疑似病例始終進行前房穿刺1)。
| 檢查方法 | 敏感度/特異度 | 注意事項 |
|---|---|---|
| 定量RT-PCR(CMV-DNA) | 敏感度71%(急性期) | ≥10³ copies/mL具診斷價值。定性PCR有偽陽性風險,不採用 |
| 抗體指數(AI)檢測 | 敏感度87%(慢性期) | 眼內抗體合成的特異性分析。慢性期有用 |
| 定量PCR+AI聯合 | 敏感度100% | 兩者聯合可最大化診斷準確性 |
| 多重PCR(先進醫療) | 多種病毒全面檢測 | 有助於與HSV/VZV鑑別。被認定為先進醫療3) |
SUN工作組將前房水PCR陽性作為CMV前葡萄膜炎研究分類的必要條件1)。
鑑別診斷:
前房穿刺(房水採集)是在門診局部麻醉下進行的相對短時間的處置。這是確定感染性葡萄膜炎病原病毒的重要檢查,操作得當則併發症風險低。對於CMV前部葡萄膜炎的確診是必不可少的步驟,73.3%的世界專家在疑似病例中始終執行該檢查1)。在沒有確診的情況下開始治療,存在繼續使用對CMV不敏感的acyclovir類藥物的風險。
CMV對acyclovir、valacyclovir、penciclovir不敏感。第一線藥物是ganciclovir或valganciclovir。
局部治療(第一線)
藥物:ganciclovir凝膠 0.15%
用法:每日4次(點眼)
優點:無全身毒性。無需定期血液檢查。
專家共識:85%支持開始局部抗病毒治療1)
70%選擇0.15%更昔洛韋凝膠作為第一線治療1)
全身治療(重症/遷延病例)
藥物:纈更昔洛韋(口服)
誘導劑量:900mg每日兩次,至少2週
維持劑量:450mg每日兩次(炎症消退後)
78%的專家選擇口服纈更昔洛韋作為全身治療1)
注意:必須每2週監測全血細胞計數和血清肌酐
復發處理:減量或停藥後復發率高達80%。復發時從初始劑量重新開始,並更緩慢地逐漸減量(88%的專家支持)1)。
類固醇僅在抗病毒藥物覆蓋下使用(71%支持)1)。無抗病毒藥物單獨使用類固醇有加重角膜內皮細胞損傷的風險。
發作時眼壓可升至40 mmHg以上(有時60 mmHg以上),因此需要迅速進行眼壓管理。
如果藥物控制眼壓不充分,可能需要青光眼手術(如小樑切除術)。若不處理,4年內超過25%的患者需要青光眼手術。在炎症充分控制後,也可進行白內障手術。
無效。CMV對阿昔洛韋、伐昔洛韋、噴昔洛韋不敏感,因此這些藥物無效是CMV感染的重要徵象。更昔洛韋(局部或全身)或纈更昔洛韋是一線藥物;如果懷疑CMV前葡萄膜炎,需要更換抗病毒藥物。
初次感染後,CMV潛伏在骨髓系前驅細胞(單核球/巨噬細胞前驅體)中。病毒在前眼部巨噬細胞和樹突狀細胞中再活化,導致前眼部發炎。也有研究指出,其他部位的感染可能誘導循環血液中單核球的CMV再活化。再活化後,釋放干擾素-γ和干擾素-β,啟動發炎連鎖反應。
CMV直接感染角膜內皮細胞,引起細胞損傷。這導致:
若不治療,內皮細胞密度持續進行性下降,最終有進展為水疱性角膜病變的風險。
多種機制參與眼壓升高:
在PSS型中,發作間歇期通常維持正常或略低的眼壓,但隨著反覆發作,小樑網發生不可逆損傷累積,導致慢性高眼壓和青光眼性視野缺損。
一名66歲免疫功能正常的女性,因復發性高眼壓性前葡萄膜炎進行前房穿刺,房水CMV-DNA檢測為25,675 copies/mL。局部使用更昔洛韋0.15%(每日4次)、口服伐昔洛韋1g(每日2次)合併局部類固醇治療後,炎症消退,眼壓得到控制,最終穩定在12 mmHg 2)。
一項涉及21個國家100名國際葡萄膜炎專家的兩輪德爾菲調查中,75人(75%)完成了調查1)。儘管CMV前葡萄膜炎的診斷和治療在許多領域難以達成共識,但達成了以下重要共識:
然而,對於PCR陰性病例的治療和診斷標準,國際共識仍未建立,需要進一步累積證據1)。