MERRF (โรคลมชักกล้ามเนื้อกระตุกที่มีเส้นใยแดงขาด) เป็นโรคหลายระบบที่หายาก เกิดจากการกลายพันธุ์ของดีเอ็นเอไมโตคอนเดรีย
การกลายพันธุ์ m.8344A>G พบประมาณ 80% ของผู้ป่วยทั้งหมด มีรูปแบบการถ่ายทอดทางมารดา
อาการทางจักษุประสาท ได้แก่ ฝ่อของเส้นประสาทตา ตาเข หนังตาตก จอประสาทตา เสื่อมชนิดมีเม็ดสี และตากระตุก
แม้การมองเห็น ปกติ OCT อาจตรวจพบการบางลงของชั้นเส้นใยประสาทจอตา
อาการทางคลินิกแตกต่างกันมากตามระดับ heteroplasmy (สัดส่วนของ mtDNA ที่กลายพันธุ์)
ในการรักษาโรคลมชัก การใช้ยาเลวิทิราซิแทมร่วมกับโคลนาซีแพมถือว่ามีประสิทธิภาพมากที่สุด และกรดวาลโปรอิกมีข้อห้ามใช้โดยหลักการเนื่องจากความเป็นพิษต่อไมโตคอนเดรีย
ไม่มีการรักษาที่หายขาด จำเป็นต้องติดตามผลระยะยาวโดยสหสาขาวิชาชีพ
กลุ่มอาการ MERRF (Myoclonic Epilepsy with Ragged Red Fibers) เป็นโรคไมโตคอนเดรีย หลายระบบที่หายากซึ่งเกิดจากการกลายพันธุ์ของดีเอ็นเอไมโตคอนเดรีย ใน ICD-10 จัดอยู่ในรหัส E88.4 (ความผิดปกติของการเผาผลาญไมโตคอนเดรีย)
ประมาณ 80% ของผู้ป่วย MERRF เกิดจากการกลายพันธุ์แบบจุด m.8344A>G ในยีน MT-TK5) การกลายพันธุ์นี้ทำให้ tRNA ไลซีนทำงานผิดปกติ ขัดขวางการประกอบโปรตีนที่จำเป็นสำหรับฟอสโฟรีเลชันแบบออกซิเดชัน1) การกลายพันธุ์อื่นๆ ที่เป็นสาเหตุ ได้แก่ m.8356T>C, m.8363G>A และ m.3243A>G5) นอกจากนี้ยังมีรายงานการกลายพันธุ์ใหม่ในยีน MT-TC (m.5820C>A)2) .
ในกรณีที่ถ่ายทอดทางพันธุกรรม มักจะเป็นรูปแบบการถ่ายทอดทางมารดา โรคที่เป็นตัวแทนของโรคกล้ามเนื้อและสมองจากไมโตคอนเดรีย ได้แก่ โรคตากระตุก เรื้อรังแบบลุกลาม (CPEO), MELAS และ MERRF โดย MELAS พบได้บ่อยที่สุด
ความชุกของ MERRF ประมาณน้อยกว่า 1 ใน 100,000 คน อายุเฉลี่ยที่เริ่มมีอาการคือ 45 ปี 5) แต่มีบางกรณีที่เริ่มมีอาการในวัยเด็กตอนต้นด้วยอาการชักจากโรคลมชัก มีรายงานว่า 92.3% ของผู้ที่กลายพันธุ์ m.8344A>G จะเกิดโรคลมชัก 4) .
อาการทางคลินิกแตกต่างกันอย่างมากตามระดับของ heteroplasmy (สัดส่วนของ mtDNA กลายพันธุ์และชนิดปกติในเซลล์เดียวกัน)1) 3) . เมื่อปริมาณการกลายพันธุ์ต่ำ อาจมีรูปแบบที่ไม่รุนแรงโดยไม่มีอาการของระบบประสาทส่วนกลาง มีรายงานครอบครัวหนึ่งที่ไม่แสดงอาการทางคลินิกของระบบประสาทส่วนกลางตลอดสี่ชั่วอายุคน3) .
Q
MERRF ถ่ายทอดทางพันธุกรรมอย่างไร?
A
DNA ไมโทคอนเดรียถ่ายทอดจากแม่เท่านั้น ดังนั้นจึงมีรูปแบบการถ่ายทอดทางมารดา สัดส่วนของ mtDNA ที่กลายพันธุ์ (heteroplasmy) แตกต่างกันไปในแต่ละบุคคลและเนื้อเยื่อ และส่งผลต่อความรุนแรงของอาการทางคลินิก สำหรับรายละเอียดเพิ่มเติม โปรดดูหัวข้อ “สาเหตุและปัจจัยเสี่ยง” (#3-สาเหตุและปัจจัยเสี่ยง)
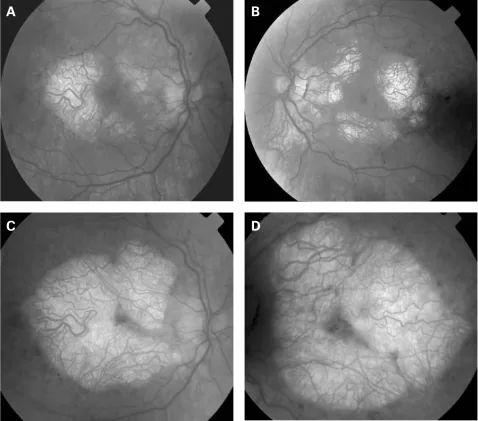
ภาพ MERRF P P Rath, S Jenkins, M Michaelides et al. Characterisation of the macular dystrophy in patients with the A3243G mitochondrial DNA point mutation with fundus autofluorescence. The British Journal of Ophthalmology. 2008 Jan 22; 92(5):623. Figure 2. PM
CI D: PMC2569141. License: CC BY.
ภาพผู้ป่วย MERRF ระหว่างปี 1994 ถึง 2001
ลักษณะสำคัญสี่ประการของ MERRF คือ กล้ามเนื้อกระตุก (myoclonus), ลมชักทั่วไป (generalized epilepsy), การทรงตัวผิดปกติ (ataxia), และเส้นใยกล้ามเนื้อสีแดงหยาบ (ragged red fibers) จากการตรวจชิ้นเนื้อกล้ามเนื้อ ในสาขาจักษุประสาทวิทยา อาการต่อไปนี้เป็นอาการหลักที่ผู้ป่วยมาโรงพยาบาล
การมองเห็น ลดลงฝ่อของเส้นประสาทตา มักเป็นทั้งสองข้างและสมมาตรอาการกล้ามเนื้อกระตุก (Myoclonus) : การหดและคลายตัวของกล้ามเนื้ออย่างรวดเร็วโดยไม่ตั้งใจ มักนาน 1–2 วินาที 5) อาจถูกกระตุ้นโดยแสง 2) .อาการชักจากโรคลมชัก : อาการชักแบบกล้ามเนื้อกระตุกพบมากที่สุด แต่ยังมีรายงานอาการชักแบบเกร็งกระตุกทั้งตัว อาการชักเฉพาะที่ และอาการชักแบบเหม่อ 5) .อาการเสียการทรงตัวจากสมองน้อย (Cerebellar ataxia) : การเคลื่อนไหวไม่ประสานกันและพูดไม่ชัดปรากฏขึ้นแบบค่อยเป็นค่อยไป 4) .การสูญเสียการได้ยินแบบประสาทรับเสียง (Sensorineural hearing loss) : พบร่วมบ่อย.อาการชาปลายมือปลายเท้า : ความผิดปกติทางความรู้สึกที่ปลายแขนขาเนื่องจากโรคเส้นประสาทส่วนปลาย 2) .กล้ามเนื้ออ่อนแรงและเหนื่อยง่าย : เนื่องจากโรคกล้ามเนื้อ 4) .
ผลการตรวจทางประสาทจักษุวิทยาหลักที่เกี่ยวข้องกับ MERRF มี 5 ประการ ได้แก่ ฝ่อ/โรคเส้นประสาทตา กล้ามเนื้อตาอัมพาต หนังตาตก จอประสาทตา เสื่อมชนิดมีเม็ดสี และอาตา
ฝ่อของเส้นประสาทตา
ความถี่ : 39% ของผู้ป่วย MERRF (Hirano และคณะ 13/36 ราย) และ 10% ของผู้ที่มีการกลายพันธุ์ m.8344A>G โดยรวม (Altmann และคณะ 34 ราย) 1)
ผลการตรวจ : จานประสาทตา ซีดทั้งสองข้างและสมมาตร 1) มีรายงานการพบฝ่อของเส้นประสาทตา ใน 6 ใน 7 ราย (85.7%) ของเด็กและผู้ใหญ่ตอนต้นที่ได้รับการยืนยันทางพันธุกรรม
จุดที่น่าสนใจ : ตรวจพบการบางลงของ RNFL และ GCC จุดรับภาพในผู้ป่วยทั้งสามรายที่ไม่มีอาการทางสายตา
กล้ามเนื้อตาอัมพาตและหนังตาตก
กล้ามเนื้อตาอัมพาต : 2 ใน 34 ราย (5.9%) การจำกัดการเคลื่อนไหวของกล้ามเนื้อนอกลูกตา แตกต่างกันไปในรายงาน: 2/2 ราย (Zhu และคณะ), 3 ใน 7 ราย (42.9%, Grönlund และคณะ).
หนังตาตก
จอประสาทตาเสื่อมและอาตา
จอประสาทตา เสื่อมชนิดมีเม็ดสีจอประสาทตา เสื่อม (Grönlund และคณะ).
อาตา
Q
เส้นประสาทตาสามารถผิดปกติได้หรือไม่แม้ว่าการมองเห็นปกติ?
A
แม้ในผู้ป่วยที่ไม่มีอาการทางตา OCT สามารถตรวจพบการบางลงของชั้นใยประสาทจอตาและกลุ่มเซลล์ปมประสาทจอตาบริเวณจุดรับภาพ ซึ่งสะท้อนถึงการสูญเสียเซลล์จอตาที่แฝงอยู่ และแนะนำให้ติดตามผลทางจักษุวิทยาเป็นประจำ
เส้นใยแดงขาดวิ่น : ยืนยันโดยการตัดชิ้นเนื้อกล้ามเนื้อใน 96% ของการกลายพันธุ์ m.8344A>G 1) .ไขมันในเนื้อเยื่อหลายตำแหน่ง : มีช่วง 3–32.4% ตามรายงาน1) มีการชี้ให้เห็นความสัมพันธ์ระหว่าง heteroplasmy สูงกับขนาดของ lipoma1) .โรคกล้ามเนื้อหัวใจ เบาหวาน ภาวะไทรอยด์ต่ำ : เกิดร่วมเป็นส่วนหนึ่งของความผิดปกติหลายอวัยวะ5) .ภาวะเลือดเป็นกรดแลกติก : พบระดับแลกเตตในน้ำไขสันหลังสูงขึ้น2) .ความบกพร่องทางสติปัญญาและภาวะสมองเสื่อม : ปรากฏในรายที่ลุกลาม.
สาเหตุของ MERRF คือการกลายพันธุ์ของดีเอ็นเอไมโทคอนเดรีย (mtDNA)
การกลายพันธุ์ m.8344A>G ในยีน MT-TK : พบบ่อยที่สุด คิดเป็นประมาณ 80% ของผู้ป่วยทั้งหมด5) ทำให้เกิดความผิดปกติของโครงสร้าง tRNA ไลซีน ขัดขวางการสังเคราะห์โปรตีนที่จำเป็นสำหรับฟอสโฟรีเลชันเชิงออกซิเดชัน1) .การกลายพันธุ์ mtDNA อื่นๆ : m.8356T>C, m.8363G>A, m.3243A>G, m.3255G>A, m.5820C>A ในยีน MT-TC และอื่นๆ2) 5) .การถ่ายทอดทางมารดา : เนื่องจาก mtDNA ถ่ายทอดจากมารดาเท่านั้น ในครอบครัวที่มีผู้ป่วย จึงถ่ายทอดเฉพาะสมาชิกในครอบครัวฝ่ายมารดาเท่านั้นเฮเทอโรพลาสมีและผลของเกณฑ์ : เมื่อสัดส่วนของ mtDNA กลายพันธุ์เกินเกณฑ์เฉพาะเนื้อเยื่อ จะเกิดความผิดปกติทางชีวเคมี3) เกณฑ์ในกล้ามเนื้อโครงร่างประมาณว่าอยู่ที่ 60-90% ของการกลายพันธุ์ และหากมี mtDNA ปกติเหลืออยู่ประมาณ 15% การแปลรหัสและการทำงานของ COX จะกลับมาเกือบปกติ3) .ยีนปรับแต่งในนิวเคลียส : มีข้อบ่งชี้ถึงปัจจัยที่มีผลต่อการแยกและการจำลอง mtDNA และควบคุมการกระจายปริมาณการกลายพันธุ์ระหว่างเนื้อเยื่อ3) .
MERRF เป็นโรคทางพันธุกรรม การป้องกันโดยปัจจัยสิ่งแวดล้อมทำได้ยาก หากสงสัยว่ามีรูปแบบการถ่ายทอดทางมารดาในครอบครัว ควรพิจารณาปรึกษาแพทย์ด้านพันธุศาสตร์ การหลีกเลี่ยงสิ่งกระตุ้นแสงและความเครียดที่อาจทำให้เกิดอาการชัก และการติดตามผลแบบสหสาขาวิชาอย่างสม่ำเสมอเป็นสิ่งสำคัญ
สำหรับการวินิจฉัย MERRF ใช้ลักษณะทางคลินิกสี่ประการต่อไปนี้ (สี่ประการคลาสสิก)
กล้ามเนื้อกระตุก
โรคลมชักทั่วร่างกาย
ภาวะเสียการทรงตัว
เส้นใยกล้ามเนื้อสีแดงขาดในการตัดชิ้นเนื้อกล้ามเนื้อ
การตรวจทางพันธุกรรมระดับโมเลกุลมีความจำเป็นสำหรับการวินิจฉัยที่แน่นอน พบการกลายพันธุ์ m.8344A>G ในผู้ป่วยมากกว่า 80% 5) .
สิ่งส่งตรวจ : สกัดดีเอ็นเอจากเลือด ปัสสาวะ และกล้ามเนื้อวิธีการ : การวัดปริมาณเฮเทอโรพลาสมีด้วยวิธี PCR-RFLP 3) ข้อควรระวัง : โดยปกติแล้ว heteroplasmy ในปัสสาวะจะสูงกว่าในเลือด 3)
การย้อม Gomori trichrome แบบดัดแปลงพบเส้นใยสีแดงขาดรุ่งริ่ง พบการย้อม SDH เข้มและเส้นใยที่ขาด COX ในการย้อมคู่ COX-SDH พบเส้นใยที่ขาด COX ประมาณ 5% 2) กล้องจุลทรรศน์อิเล็กตรอนพบการเพิ่มจำนวนและยืดตัวผิดปกติของไมโตคอนเดรียใต้เยื่อหุ้มเซลล์กล้ามเนื้อ 2)
การนำกระแสประสาท : แสดงรูปแบบของโรคเส้นประสาทรับความรู้สึก 2) การตรวจคลื่นไฟฟ้าสมอง (EEG) : พบภาวะไวต่อแสง ศักย์ไฟฟ้าสมองที่เกิดจากการกระตุ้นประสาทสัมผัสร่างกายขนาดใหญ่ (SEP 90μV, ปกติ <10μV) เป็นลักษณะเฉพาะ 2) คลื่นไฟฟ้ากล้ามเนื้อ : การเปลี่ยนแปลงของกล้ามเนื้อในรยางค์ส่วนปลายล่าง2)
MRI สมอง : อาจพบการฝ่อของสมองน้อย การเปลี่ยนแปลงสัญญาณของนิวเคลียสเดนเทต2) โดยปกติมักปกติ1) MR Spectroscopy : มักตรวจพบพีคของแลคเตท 1)
เครื่องตรวจการเชื่อมโยงกันของแสง (OCT ) : สามารถตรวจพบการบางลงของชั้นใยประสาทจอตาและกลุ่มเซลล์ปมประสาทจอตาได้แม้ในผู้ป่วยที่ไม่มีอาการ1) การตรวจอวัยวะภายในลูกตา : จานประสาทตา ซีด 1)
ระดับแลคเตท 19 มก./ดล. (ปกติ 4.2–17.0) และไพรูเวท 1.2 มก./ดล. (ปกติ 0.3–0.9) เพิ่มขึ้นเล็กน้อย 2) .
การทำงานของคอมเพล็กซ์ IV ในกล้ามเนื้อโครงร่างลดลงเหลือ 55–69% ของกลุ่มควบคุม 2) .
MERRF เป็นชนิดหนึ่งของโรคลมชักแบบกล้ามเนื้อกระตุกแบบก้าวหน้า (PME) ซึ่งสำคัญที่จะต้องแยกจากโรคต่อไปนี้
โรค จุดที่ใช้แยก โรคลมชักกล้ามเนื้อกระตุกในวัยรุ่น (JME) ไม่มีการเสื่อมของความรู้ความเข้าใจหรือการเคลื่อนไหวผิดปกติแบบก้าวหน้า พยากรณ์โรคดี โรค Lafora พบ Lafora body เป็นบวกจากการตรวจชิ้นเนื้อผิวหนัง โรคอันเวอร์ริชท์-ลุนด์บอร์ก การกลายพันธุ์ของยีน CSTB การดำเนินโรคช้า โรคลิโปฟัสซิโนซิสชนิดเซอรอยด์ในเซลล์ประสาท จอประสาทตา เสื่อมอย่างชัดเจน การขาดเอนไซม์
ในระยะแรกมักถูกวินิจฉัยผิดเป็น JME และอาการทางระบบร่วม เช่น การเสียการทรงตัวและการเสื่อมของสมอง มีประโยชน์ในการแยก PME1)
ปัจจุบันยังไม่มีการรักษาให้หายขาดสำหรับ MERRF การรักษามุ่งเน้นไปที่การบรรเทาอาการ โดยใช้แนวทางสหสาขาวิชาชีพที่ผสมผสานการจัดการโรคลมชักและการดูแลแบบประคับประคองอย่างครอบคลุม
Levetiracetam ถือว่ามีประสิทธิภาพมากที่สุดสำหรับโรคลมชักชนิดกล้ามเนื้อกระตุก 5) .
การรักษาแบบผสม Levetiracetam + Clonazepam : ในการศึกษาในผู้ป่วย MERRF จำนวน 17 ราย ผู้ป่วยทุกรายจาก 12 รายที่เปลี่ยนจากการรักษาด้วยยาเดี่ยวมาเป็นการรักษาแบบผสมมีอาการดีขึ้น มีรายงานการปรับปรุงการทำงานของสมองและการประสานงานของกล้ามเนื้อด้วย 5) .Clonazepam : ในฐานะยาในกลุ่มเบนโซไดอะซีพีน มีประสิทธิภาพเดี่ยวในการรักษาอาการกล้ามเนื้อกระตุก 5) .Zonisamide : มีข้อบ่งชี้ถึงประสิทธิภาพ 5) .Piracetam : มีประสิทธิภาพในบางกรณี5) . ในกรณีของผู้หญิงญี่ปุ่นอายุ 68 ปี ได้เปลี่ยนใบสั่งยาเป็นสูตรที่ใช้ piracetam และ levetiracetam หลังจากหยุด phenytoin และ carbamazepine และอาการดีขึ้น2) .
ASM ผลต่ออาการกล้ามเนื้อกระตุก ข้อควรระวัง Levetiracetam มีประสิทธิภาพ ทางเลือกแรก โคลนาซีแพม ได้ผล ฤทธิ์กดประสาท โซนิซาไมด์ อาจได้ผล — ไพราซีแทม อาจมีประสิทธิผล — กรดวาลโปรอิก — ห้ามใช้โดยหลักการ (พิษต่อไมโตคอนเดรีย) ฟีนิโทอิน อาการกล้ามเนื้อกระตุกแย่ลง หลีกเลี่ยงการใช้ คาร์บามาซีปีน อาการกล้ามเนื้อกระตุกแย่ลง หลีกเลี่ยงการใช้
กรดวาลโปรอิก (Valproic acid) ลดการทำงานของคอมเพล็กซ์ I และ IV ในสายโซ่หายใจของไมโตคอนเดรีย ดังนั้นโดยหลักการแล้วควรหลีกเลี่ยงการใช้ใน MERRF 5) ฟีนิโทอิน (Phenytoin), คาร์บามาซีปีน (Carbamazepine) และออกซ์คาร์บาซีปีน (Oxcarbazepine) อาจทำให้อาการกล้ามเนื้อกระตุก (myoclonus) แย่ลง 5) ลาโมทริจีน (Lamotrigine) ก็มีรายงานว่าทำให้อาการกล้ามเนื้อกระตุกแย่ลงเช่นกัน 5) การเปลี่ยนยาต้านโรคลมชัก ควรทำภายใต้คำแนะนำของแพทย์ผู้เชี่ยวชาญด้านโรคลมชัก
อาหารเสริมต่อไปนี้ได้รับการแนะนำตามประสบการณ์เพื่อช่วยสนับสนุนการทำงานของไมโตคอนเดรีย แต่ไม่มีหลักฐานที่ชัดเจน 1)
โคเอนไซม์คิวเท็น (ยูบิควินอล) : ช่วยสนับสนุนสายโซ่ขนส่งอิเล็กตรอนแอล-คาร์นิทีน : ช่วยสนับสนุนการเผาผลาญกรดไขมันกรดอัลฟาไลโปอิก : ฤทธิ์ต้านอนุมูลอิสระ1) วิตามินอี : ฤทธิ์ต้านอนุมูลอิสระ1) ครีเอทีนโมโนไฮเดรต : ช่วยในการผลิตพลังงาน1) วิตามินบีรวม : ช่วยในการเผาผลาญของไมโตคอนเดรีย
แนะนำให้ทำกายภาพบำบัดและการออกกำลังกายแบบแอโรบิกเพื่อรักษาความสามารถในการเคลื่อนไหว การประกอบอาชีพบำบัดและการบำบัดทางการพูดก็มีประโยชน์เช่นกัน4) .
จำเป็นต้องมีการติดตามผลเป็นประจำโดยแพทย์เฉพาะทางด้านประสาทวิทยา จักษุวิทยา หทัยวิทยา และต่อมไร้ท่อ 1) แนะนำให้ประเมินทางคลินิก ตรวจเลือด ตรวจคลื่นไฟฟ้าสมอง และติดตามระดับยาในเลือดของยาต้านชักทุก 3 เดือน 5) .
Q
ทำไมจึงไม่สามารถใช้กรดวาลโปรอิกใน MERRF ได้?
A
กรดวาลโปรอิกได้รับการพิสูจน์จากการทดลองว่าลดการทำงานของคอมเพล็กซ์ I และ IV ในสายโซ่การหายใจของไมโทคอนเดรีย ซึ่งอาจทำให้โรคไมโทคอนเดรียเช่น MERRF รุนแรงขึ้น 5) ในการรักษาโรคลมชัก ควรเลือกใช้ยาที่มีความเป็นพิษต่อไมโทคอนเดรียต่ำ เช่น เลเวทิราเซแทม และโคลนาซีแพม
พยาธิกำเนิดของ MERRF เกิดจากความผิดปกติของไมโทคอนเดรียอันเนื่องมาจากการกลายพันธุ์ของดีเอ็นเอไมโทคอนเดรีย
การกลายพันธุ์ m.8344A>G ในยีน MT-TK ทำให้โครงสร้างของ tRNA ไลซีนเปลี่ยนแปลงไป ขัดขวางการสังเคราะห์โปรตีนในไมโตคอนเดรีย (การประกอบคอมเพล็กซ์ฟอสโฟรีเลชันออกซิเดชัน)1) ส่งผลให้การผลิต ATP ลดลง และอวัยวะที่ต้องการพลังงานสูง (สมอง กล้ามเนื้อโครงร่าง กล้ามเนื้อหัวใจ) ได้รับความเสียหายเป็นลำดับแรก3)
การกลายพันธุ์ของดีเอ็นเอไมโตคอนเดรียอยู่ในสถานะเฮเทอโรพลาสมี และเมื่อสัดส่วนของ mtDNA กลายพันธุ์เกินเกณฑ์เฉพาะเนื้อเยื่อ จะเกิดฟีโนไทป์ทางชีวเคมี3)
เกณฑ์ทางพยาธิวิทยาของกล้ามเนื้อโครงร่าง: การกลายพันธุ์ 60–90%3)
mtDNA ชนิดปกติที่เหลืออยู่ประมาณ 15% สามารถฟื้นฟูการแปลรหัสและการทำงานของ COX ให้กลับมาเกือบปกติ3)
ยีนปรับแต่งในนิวเคลียสควบคุมการแยกและการจำลอง mtDNA อย่างจำเพาะเนื้อเยื่อ 3)
เพื่อชดเชยการขาด COX (ความผิดปกติของคอมเพล็กซ์ IV ในสายโซ่หายใจ) ไมโทคอนเดรียที่ผิดปกติจะเพิ่มจำนวนใต้ซาร์โคเลมมา ก่อให้เกิดเส้นใยแดงขาดรุ่งริ่ง (RRF) 2) ภายใต้กล้องจุลทรรศน์อิเล็กตรอน จะพบการเพิ่มจำนวนอย่างเด่นชัดของไมโทคอนเดรียที่ยืดยาวผิดปกติและสารรวมพาราคริสตัลไลน์ 2)
เซลล์ปมประสาทจอประสาทตา มีความต้องการพลังงานสูงและไวต่อความผิดปกติของไมโทคอนเดรีย 1) แม้ในผู้ป่วยที่ไม่มีอาการทางสายตา ยังตรวจพบการบางลงของ RNFL และ GCC ซึ่งบ่งชี้ถึงการสูญเสียเซลล์ประสาทที่แฝงอยู่และกำลังดำเนินไป
ความผิดปกติของไมโทคอนเดรียนำไปสู่การเพิ่มขึ้นของความเครียดออกซิเดชัน ความผิดปกติของระบบภูมิคุ้มกัน และการเปลี่ยนแปลงพลวัตของไมโทคอนเดรีย ซึ่งมีส่วนร่วมในพยาธิกำเนิดของอาการชักจากโรคลมชัก 4)
Baysal และคณะ (2025) รายงานการใช้อุปกรณ์กระตุ้นเส้นประสาทเวกัส (VNS) ด้วยโปรโตคอลการเพิ่มขนาดยาอย่างรวดเร็ว (เพิ่มเป็น 2 mA ภายใน 6 วัน) ในหญิงอายุ 38 ปีที่มีการกลายพันธุ์ m.8344A>G ซึ่งมีภาวะสถานะลมชักที่ดื้อต่อการรักษาอย่างรุนแรง (SRSE)4) หลังจากฝัง VNS 7 วัน อาการกล้ามเนื้อกระตุก (myoclonus) เริ่มดีขึ้น และหลังจาก 21 วัน อาการชักเกร็งกระตุกทั้งตัว (generalized tonic-clonic seizure) หายไป ในระหว่างการติดตามผล 2 ปี ไม่มีการกลับเป็นซ้ำของอาการชักเกร็งกระตุกทั้งตัวหรือสถานะลมชัก และอาการกล้ามเนื้อกระตุกก็ลดลง กลไกการออกฤทธิ์ของ VNS สันนิษฐานว่าเกี่ยวข้องกับการกระตุ้นวิถีประสาทจากนิวเคลียสโซลิทาเรียส (nucleus tractus solitarius) ไปยังโลคัสซีรูเลียส (locus coeruleus) ซึ่งปล่อยนอร์เอพิเนฟริน และนิวเคลียสราฟี (raphe nuclei) ซึ่งปล่อยเซโรโทนิน ผ่านการกระตุ้นเส้นประสาทเวกัสข้างซ้าย รวมถึงการเพิ่มความหนาแน่นของตัวรับ GABA-A4) .
อัตราการหยุด SE ด้วย VNS รายงานในการทบทวนอย่างเป็นระบบที่ 74% (28 จาก 38 ราย) แต่มีการชี้ให้เห็นถึงความเป็นไปได้ของอคติในการรายงาน4) .
Perampanel และ rufinamide ได้รับรายงานว่ามีประสิทธิภาพในโรคลมชักแบบกล้ามเนื้อกระตุกที่ไม่ใช่ไมโตคอนเดรีย และคาดว่าจะนำไปใช้ใน MERRF5) .
การรักษาทางเลือกอื่นๆ ได้แก่ อาหารแอตกินส์ กลูโคคอร์ติคอยด์ แคนนาบิไดออล (CBD) N-อะเซทิลซิสเทอีน การกระตุ้นสมองส่วนลึก และการกระตุ้นแม่เหล็กผ่านกะโหลกศีรษะ (ลดความถี่ชักลง 30-40%)5) .
Kawazoe และคณะ (2022) รายงานหญิงชาวญี่ปุ่นอายุ 68 ปีที่มีการกลายพันธุ์แบบโฮโมพลาสมี m.5820C>A ในยีน MT-TC2) การกลายพันธุ์นี้อยู่ที่ฐานของก้านรับกรดอะมิโนของ tRNA ซิสเทอีน และการวิเคราะห์ในซิลิโกทำนายว่าก่อโรค ในรายนี้พบนิวเคลียร์อินคลูชันที่ให้ผลบวกต่อ p62 ในการตรวจชิ้นเนื้อผิวหนัง ซึ่งชี้ให้เห็นความเชื่อมโยงใหม่ระหว่างโรคไมโตคอนเดรีย และนิวเคลียร์อินคลูชัน2) .
Q
การรักษาด้วยการกระตุ้นเส้นประสาทเวกัสคืออะไร?
A
เป็นการรักษาโดยการพันอิเล็กโทรดรอบเส้นประสาทเวกัสที่คอด้านซ้าย และส่งกระแสไฟฟ้าเป็นระยะจากเครื่องกระตุ้นที่ฝังใต้ผิวหนังบริเวณหน้าอก การรักษานี้ทำงานผ่านก้านสมองเพื่อออกฤทธิ์ต้านการชัก มีรายงานผู้ป่วยที่ได้ผลในภาวะโรคลมชักที่ดื้อต่อการรักษาอย่างรุนแรงใน MERRF4) แต่หลักฐานยังมีจำกัด
Jeeva-Patel T, Freund P, Margolin EA. Lipomatosis and optic neuropathy clinches the diagnosis of myoclonic epilepsy with ragged red fibres (MERRF) syndrome. BMJ Case Rep. 2021;14:e240463.
Kawazoe T, Tobisawa S, Sugaya K, et al. Myoclonic epilepsy with ragged-red fibers with intranuclear inclusions. Intern Med. 2022;61:547-552.
Ripolone M, Zanotti S, Napoli L, et al. MERRF mutation A8344G in a four-generation family without central nervous system involvement: clinical and molecular characterization. J Pers Med. 2023;13:147.
Baysal L, Jobi S, Zimmermann S, Helmers アカントアメーバ角膜炎, Margraf NG. Successful application of vagus nerve stimulation in super refractory status epilepticus associated with MERRF syndrome. Epilepsy Behav Rep. 2025;30:100769.
Finsterer J. A review of the advances in the medical management of epilepsy associated with myoclonic epilepsy with ragged-red fibers (MERRF) syndrome. Cureus. 2025;17(4):e82875.