طريقة التبادل الهوائي
الإجراء: بعد التبادل السائل-الهوائي، يتم تقطير الصبغة على القطب الخلفي.
المزايا: صبغ مركز للقطب الخلفي. تجنب تعرض الصبغة للمنطقة المحيطية.
ملاحظات: يتطلب إتقان العمل تحت الهواء.

جراحة الزجاجية الملونة (chromovitrectomy) هي مصطلح شامل للإجراءات التي تستخدم صبغات حيوية لتصور الأنسجة شبه الشفافة داخل العين مثل الغشاء الداخلي المحدد (ILM)، الجسم الزجاجي، والغشاء فوق الشبكي (ERM) أثناء جراحة الزجاجية عبر الجسم الهدبي (PPV).
الأنسجة الرئيسية التي تتطلب الصبغ أثناء الجراحة هي الثلاثة التالية:
غالبًا ما تُستخدم الصبغات الزرقاء والخضراء. وذلك لأنها توفر تباينًا عاليًا مع اللون البرتقالي المحمر للظهارة الصباغية الشبكية (RPE)، مما يحسن رؤية المنطقة المصبوغة.
هناك ثلاث طرق رئيسية لحقن الصبغة.
الغشاء الداخلي المحدد (ILM) والأغشية أمام الشبكية هي أنسجة شبه شفافة بسمك بضعة ميكرومترات، ويصعب تمييزها تحت المجهر الجراحي بدون صبغ. استخدام الصبغة يوضح حدود الأنسجة، مما يحسن دقة وسلامة التقشير.
المؤشرات الرئيسية لجراحة الزجاجية المصبوغة هي كما يلي:
أثبتت العديد من الدراسات فعالية تقشير الغشاء الداخلي المحدد في جراحة الثقب البقعي.
في تجربة FILMS، أظهرت مجموعة تقشير الغشاء الداخلي المحدد معدل إغلاق تشريحي بنسبة 84% مقابل 48% في مجموعة عدم التقشير، بفارق ذي دلالة إحصائية (P<0.001)3). يعمل الغشاء الداخلي المحدد كسقالة لتكاثر الخلايا، لذا قد يستأنف التكاثر الخلوي إذا لم يتم إزالته2).
أظهر تحليل تلوي شمل 5480 حالة أن تقشير الغشاء الداخلي المحدد يقلل بشكل كبير من إعادة فتح الثقب البقعي2). معدل التكرار منخفض في الجراحة المصحوبة بتقشير الغشاء الداخلي المحدد1). كما درست خمس تجارب عشوائية محكومة مدى التقشير3)، ويجري البحث لتحسين مدى التقشير.
طريقة التبادل الهوائي
الإجراء: بعد التبادل السائل-الهوائي، يتم تقطير الصبغة على القطب الخلفي.
المزايا: صبغ مركز للقطب الخلفي. تجنب تعرض الصبغة للمنطقة المحيطية.
ملاحظات: يتطلب إتقان العمل تحت الهواء.
طريقة الملء السائل
الإجراء: حقن الصبغة تحت ملء BSS.
المزايا: إجراء بسيط وسهل التعلم.
ملاحظة: هناك خطر التخفيف والتعرض الواسع. يمكن استخدام معلق عالي الكثافة للتحكم في ذلك.
تقنية التقشير القياسية بعد الصبغ هي طريقة “القرص والتقشير” 3). يتم إمساك الغشاء الداخلي المحدد (ILM) بملقط دقيق وتقشيره بشكل دائري. وقت الصبغ من 5 إلى 10 ثوانٍ كافٍ 3)، والتعرض المفرط يزيد من خطر السمية.
طريقة استبدال الهواء تسمح بحصر عامل الصبغ في القطب الخلفي، وتجنب التعرض غير الضروري للمناطق المحيطية، مما يجعلها أكثر أمانًا. ومع ذلك، في كلتا الطريقتين، من المهم الحفاظ على وقت الصبغ في حدود 5-10 ثوانٍ وتجنب التعرض المفرط 3).
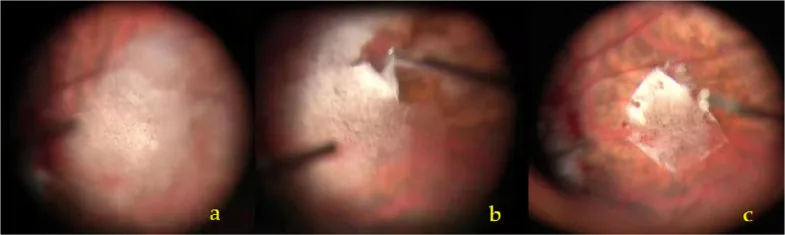
فيما يلي الخصائص الرئيسية لكل عامل صبغ.
| عامل الصبغ | النسيج المستهدف الرئيسي | التركيز المستخدم |
|---|---|---|
| BBG | الغشاء الداخلي المحدد (انتقائي) | 0.025% |
| TA | الجسم الزجاجي والغشاء الداخلي المحدد | معلق 40 ملغ/مل |
| ICG | الغشاء الداخلي المحدد (تقارب عالٍ) | 0.05–0.5% |
| TB | الغشاء فوق الشبكي (تقارب عالٍ) | 0.15% |
ملونات الغشاء الداخلي المحدد
BBG (أزرق بريليانت G): تقارب انتقائي للغشاء الداخلي المحدد3). لا يصبغ الغشاء فوق الشبكي أو الجسم الزجاجي تقريبًا. لا سمية شبكية. يُقترح أيضًا تأثير وقائي عصبي.
ICG (أخضر إندوسيانين): تقارب عالٍ للكولاجين من النوع الرابع واللامينين في الغشاء الداخلي المحدد3). أول ملون استخدم للغشاء الداخلي المحدد3). مخاوف سمية.
صبغة الغشاء فوق الشبكي
TB (أزرق التريبان): تقارب صبغي عالي للغشاء فوق الشبكي. يصبغ الخلايا الدبقية في الغشاء فوق الشبكي بشكل انتقائي. تقارب منخفض للغشاء الداخلي المحدد والجسم الزجاجي. سمية للبطانة القرنية عند التركيز العالي.
تصور الجسم الزجاجي
TA (تريامسينولون أسيتونيد): يترسب في الجسم الزجاجي كبلورات بيضاء، مما يصور الجسم الزجاجي 3). ليس صبغة بل يعمل كبلورات بيضاء على الغشاء الداخلي المحدد للتباين. له أيضًا تأثير مضاد للالتهابات.
معلق مائي بلوري أبيض (40 ملغ/مل)، يُستخدم بحقن 0.1-0.3 مل. يصور الجسم الزجاجي والقشرة الزجاجية الخلفية باللون الأبيض. على عكس الصبغات، يترسب كبلورات بيضاء على الغشاء الداخلي المحدد للحصول على التباين 3). له تأثير مضاد للالتهابات ويساهم في تثبيط الالتهاب داخل العين بعد الجراحة. عمر النصف حوالي 18 يومًا في العيون غير المستأصلة و3 أيام في العيون المستأصلة. تشمل الآثار الجانبية تقدم إعتام عدسة العين وارتفاع ضغط العين. في اليابان، تمت الموافقة على MacuAid (تريامسينولون أسيتونيد 40 ملغ/مل).
صبغة مشتقة من صبغة طعام زرقاء، لها تقارب انتقائي للغشاء الداخلي المحدد 3). لا تصبغ الغشاء فوق الشبكي أو الجسم الزجاجي، لذلك تُستخدم فقط أثناء تقشير الغشاء الداخلي المحدد. التركيز المستخدم هو محلول متساوي التوتر 0.025% (0.25 ملغ/مل). لم تُظهر الدراسات المخبرية والحيوانية سمية شبكية، ويُقترح تأثير وقائي عصبي. تم تطوير TB وBBG بعد ICG، ولهما ملف أمان أفضل 3).
في اليابان، طريقة التحضير تشمل إذابة 0.1 غرام من المسحوق في 400 مل من BSS، ثم التعقيم بالأوتوكلاف عند 115 درجة مئوية لمدة 30 دقيقة. يُقال إن مدة الصلاحية 3 أشهر بعد التحضير.
صبغة عضوية زرقاء، لها تقارب صبغي عالي للغشاء فوق الشبكي. تمر عبر غشاء الخلايا الميتة التالف لتصبغ المكونات الخلوية للغشاء فوق الشبكي، مما يجعلها مناسبة لجراحة تقشير الغشاء فوق الشبكي. تقارب منخفض للغشاء الداخلي المحدد والجسم الزجاجي. التركيز المستخدم هو 0.15%، ويتم تحويله إلى محلول عالي الكثافة (خلط TB مع 10% جلوكوز بنسبة 3:1) لتسهيل التركيز في القطب الخلفي. تم الإبلاغ عن سمية للبطانة القرنية عند التركيز العالي، وله تأثير ماسخ، لذا يجب تجنب استخدامه أثناء الحمل وعند الأطفال.
صبغة خضراء ذات ألفة عالية للكولاجين من النوع الرابع واللامينين المكونين للغشاء الداخلي المحدد (ILM) 3). وهي أول صبغة استخدمت لصبغ ILM 3). كما تم الإبلاغ عن تأثير “تقشير” جزئي لـ ILM (تأثير التقشير الكاذب) 3). ومع ذلك، هناك مخاوف من السمية مثل تلف الشبكية الداخلية والعصب البصري وعيوب المجال البصري 3)، ويوصى حاليًا باستخدامها بتركيز منخفض وأقل وقت تعرض وتقليل الإضاءة 3). يتطلب التخفيف الأولي ماء مقطر (لأن المحلول الملحي يسبب ترسبًا)، ثم يتم ضبط التركيز النهائي باستخدام BSS أو غيره. وافقت إدارة الغذاء والدواء الأمريكية (FDA) على استخدامه عن طريق الوريد فقط، واستخدامه داخل العين هو استخدام خارج العلامة.
تمت الموافقة على TA في اليابان تحت اسم MacuAid. لا توجد منتجات معتمدة رسميًا للاستخدام داخل العين لـ BBG وICG في اليابان، ويتم تحضيرها ذاتيًا أو استخدامها خارج العلامة. كما أن TB غالبًا ما يستخدم خارج العلامة. يجب التحقق من لوائح إدارة الأدوية في المنشأة قبل الاستخدام.
تساهم العوامل التالية في حدوث السمية.
| سبب السمية | الصبغة المعنية | التدبير الوقائي |
|---|---|---|
| ارتفاع أو انخفاض الضغط الأسموزي | ICG (انخفاض الضغط الأسموزي هو المشكلة) | التحضير بمحلول متساوي التوتر |
| السمية الضوئية | ICG | تقليل الإضاءة إلى الحد الأدنى |
| سمية المواد الحافظة | جميع المستحضرات | اختيار مستحضر خالٍ من المواد الحافظة |
| وقت التعرض المفرط | ICG، TB | غسل خلال 5-10 ثوانٍ |
فيما يتعلق بمشكلة الأسمولية، في البيئة منخفضة الأسمولية، قد يحدث تلف في الشبكية بسبب دخول Ca²⁺. من ناحية أخرى، في البيئة عالية الأسمولية، يحدث انكماش في الشبكية. يُعتقد أن أحد أسباب سمية ICG هو الحقن في محلول منخفض الأسمولية 3)، لذا من المهم تحضيره في محلول متساوي الأسمولية.
فيما يتعلق بمشكلة المواد الحافظة، تم الإبلاغ عن أن كلوريد ميريستيل-γ-بيكولينيوم يسبب سمية شديدة، لذا يُفضل اختيار مستحضر خالٍ من المواد الحافظة. البيانات المتعلقة بكحول البنزيل غير واضحة حاليًا.
تشمل النتائج المميزة التي تظهر بعد إزالة ILM ما يلي:
تتضمن سمية ICG عدة عوامل: دخول أيونات الكالسيوم بسبب الحقن في محلول منخفض التوتر، تفاعل الأكسدة الضوئية (السمية الضوئية) نتيجة التعرض للضوء، ومساهمة مكون اليود الموجود فيه 3). لتقليل هذه المخاطر، يُوصى باستخدام تركيز منخفض، وقت تعرض قصير، تقليل الإضاءة، وتحضير المحلول بمحلول متساوي التوتر 3).
يجري البحث عن أصباغ جديدة للتغلب على مشاكل السمية والانتقائية للأصباغ الحالية.
هي تقنية يتم فيها قلب جزء من ILM بدلاً من إزالته بالكامل (كرفرف) لتعزيز إغلاق ثقب البقعة 3). يُنظر في استخدامها للثقوب البقعية الكبيرة أو الحالات المقاومة للعلاج. يساهم تصور ILM بواسطة الصبغة في تحسين دقة هذه التقنية.
لتقييم الأصباغ والتقنيات الجديدة، يُوصى بإطار تقييم تدريجي للابتكار الجراحي مثل إطار IDEAL. التقييم المنهجي للسلامة والفعالية هو تحدٍ مستقبلي.
يمكن أن يقوم البروموفينول الأزرق بتلوين كل من الغشاء الداخلي المحدد (ILM) والغشاء فوق الشبكي (ERM)، وهو عامل تلوين مرشح يُعتقد أنه أقل سمية من ICG. كما أن IFCG (مشتق خالٍ من يوديد الصوديوم) قيد الدراسة بتصميم يزيل مكون اليود الذي يُعتقد أنه يساهم في سمية ICG. كلاهما لا يزال في مرحلة التجارب السريرية حاليًا ولم يصل إلى الاستخدام القياسي.