การตรวจการทำงานของรูม่านตา ประเมินขนาดของรูม่านตา ปฏิกิริยาต่อแสง และปฏิกิริยาต่อการมองใกล้ ใช้เป็นเครื่องมือช่วยวินิจฉัยโรคเส้นประสาทตา และโรคระบบประสาทส่วนกลาง
RAPD (ความบกพร่องของทางนำเข้าสู่รูม่านตา แบบสัมพัทธ์) ตรวจพบได้ด้วยการทดสอบ swinging flashlight และเป็นสัญญาณเชิงวัตถุวิสัยที่สำคัญซึ่งบ่งชี้ถึงการมีโรคของเส้นประสาทตา ข้างเดียวหรือโรคจอประสาทตา ที่กว้างขวาง1) ต้องทำก่อนหยอดยาขยายรูม่านตา ไม่สามารถประเมินได้หลังขยายรูม่านตา
ห้องมืด เปิดตาทั้งสองข้าง ใช้แสงส่องเป็นระยะเวลาเท่ากัน (ประมาณ 1-2 วินาทีต่อข้าง) และความเข้มแสงเท่ากันเป็นเงื่อนไขสำหรับการตรวจหา RAPD ที่แม่นยำ
สามารถวัดปริมาณ RAPD ได้โดยวางฟิลเตอร์ความหนาแน่นเป็นกลางไว้หน้าตาข้างปกติ และยังสามารถประยุกต์ใช้เพื่อประเมินประสิทธิภาพของการรักษาได้
เปรียบเทียบรูม่านตาไม่เท่ากัน ในห้องมืดและห้องสว่างเพื่อแยกความผิดปกติของระบบประสาทซิมพาเทติก (กลุ่มอาการฮอร์เนอร์ ) และความผิดปกติของระบบประสาทพาราซิมพาเทติก (อัมพาตเส้นประสาทกล้ามเนื้อตา)2)
รูม่านตา Argyll Robertson แสดงการสูญเสียรีเฟล็กซ์ต่อแสงแต่คงไว้ซึ่งรีเฟล็กซ์ต่อการมองใกล้ (การแยกของแสงและการมองใกล้) และเป็นลักษณะเฉพาะของโรคซิฟิลิสระบบประสาท การตรวจการทำงานของรูม่านตา เป็นชุดการตรวจที่ประเมินขนาด รูปร่าง ปฏิกิริยาต่อแสง และปฏิกิริยาต่อการมองใกล้ของรูม่านตา ส่วนใหญ่ใช้เป็นเครื่องมือช่วยวินิจฉัยโรคเส้นประสาทตา และโรคระบบประสาทส่วนกลาง และเป็นตัวอย่างทั่วไปของการตรวจที่ง่าย ไม่รุกราน และสามารถทำได้ทันทีที่ข้างเตียงผู้ป่วย
วัตถุประสงค์หลักของการตรวจมีดังนี้:
การตรวจหา RAPD (ความบกพร่องของทางนำเข้าสัมพัทธ์ของรูม่านตา ) : ยืนยันโดยการทดสอบไฟฉายแกว่งข้างเดียวการประเมินรีเฟล็กซ์แสงโดยตรงและโดยอ้อม : สังเกตการหดตัวของรูม่านตา ในตาที่ถูกกระตุ้นและตาตรงข้ามเพื่อแยกความแตกต่างระหว่างความบกพร่องของทางนำเข้าและทางออกการวินิจฉัยแยกสาเหตุของม่านตา ไม่เท่ากัน (anisocoria) : เปรียบเทียบในห้องมืดและสว่างเพื่อแยกกลุ่มอาการฮอร์เนอร์ และอัมพาตเส้นประสาทกล้ามเนื้อตาการประเมินการแยกของแสงกับระยะใกล้ (light-near dissociation) : ใช้เพื่อแยกรูม่านตา อาร์ไกลล์ โรเบิร์ตสันและรูม่านตา อาดีการตรวจรูม่านตา ทางเภสัชวิทยา : ใช้ยาหยอดตาเพื่อยืนยันกลุ่มอาการฮอร์เนอร์ หรือรูม่านตา อาดีและแยกตำแหน่งรอยโรค
ในการประเมินระยะเฉียบพลันของโรคที่คุกคามการมองเห็น เช่น โรคประสาทตาอักเสบ โรคเส้นประสาทตา จากการบาดเจ็บ โรคเส้นประสาทตา ขาดเลือด และในการวินิจฉัยแยกโรคทางจักษุวิทยาและประสาทวิทยา ข้อมูลจากการตรวจนี้มีผลอย่างมากต่อการตัดสินใจทางคลินิก
Q
การตรวจการทำงานของรูม่านตาให้ข้อมูลอะไรบ้าง?
A
การตรวจการทำงานของรูม่านตา สามารถประมาณตำแหน่งของรอยโรคในทางนำเข้า (จอประสาทตา และเส้นประสาทตา ) และทางออก (เส้นประสาทกล้ามเนื้อตา) ของรีเฟล็กซ์แสง โดยเฉพาะอย่างยิ่ง RAPD เป็นสัญญาณวัตถุวิสัยที่สำคัญซึ่งบ่งชี้ถึงโรคเส้นประสาทตา ข้างเดียวหรือโรคจอประสาทตา ที่กว้างขวาง 1) นอกจากนี้ การเปรียบเทียบม่านตา ไม่เท่ากันในห้องสว่างและมืดช่วยให้สามารถแยกความผิดปกติของระบบประสาทซิมพาเทติกและพาราซิมพาเทติกได้ และการรวมกับการตรวจหยอดยาทางเภสัชวิทยาสามารถประมาณตำแหน่งรอยโรค (ก่อนปมประสาทหรือหลังปมประสาท) ได้ในบางกรณี 2)
หาก RAPD เป็นบวก แสดงว่ามีความผิดปกติของเส้นประสาทตา ข้างเดียวหรือโรคจอประสาทตา ที่กว้างขวาง ต่อไปนี้เป็นโรคทั่วไปที่ทำให้ RAPD เป็นบวกและลบ 1) 3)
การจำแนก โรคทั่วไป RAPD บวก (โรคเส้นประสาทตา )โรคประสาทตาอักเสบ , โรคเส้นประสาทตา จากการบาดเจ็บ, โรคเส้นประสาทตา ขาดเลือด (NAION และอื่นๆ), โรคเส้นประสาทตา จากการกดทับRAPD บวก (โรคจอประสาทตา ชนิดกว้าง)จอประสาทตาลอก เป็นบริเวณกว้าง, หลอดเลือดแดงจอประสาทตา ส่วนกลางอุดตัน (CRAO ), AZOOR โรคที่ไม่ทำให้ RAPD เป็นบวก รูที่จุดรับภาพ, โรคเส้นประสาทตา สองข้างแบบสมมาตร, รอยโรคของทางเดินประสาทตา (หลังจุดไขว้)
หาก RAPD เป็นบวกแม้ไม่มีความผิดปกติชัดเจนที่จอตา (โดยเฉพาะจุดรับภาพ) ควรสงสัยโรคเส้นประสาทตา อย่างยิ่ง รูที่จุดรับภาพไม่ทำให้ RAPD เป็นบวก ซึ่งเป็นจุดแยกโรคที่สำคัญ
ในโรคเส้นประสาทตา สองข้างแบบสมมาตร ความบกพร่องของทางนำเข้าของตาทั้งสองข้างจะหักล้างกัน ดังนั้นจึงตรวจไม่พบ RAPD รอยโรคหลังจุดไขว้ (แถบรังสีแก้วตาและคอร์เทกซ์การเห็น) ก็ไม่ทำให้เกิด RAPD เช่นกัน
แนะนำให้ทำการตรวจนี้เป็นการคัดกรองเบื้องต้นสำหรับโรคที่มีความเร่งด่วนสูง (เช่น CRAO , ปลายประสาทตาอักเสบเฉียบพลัน, โรคเส้นประสาทตา จากการบาดเจ็บ)
Q
โรคใดบ้างที่ทำให้ RAPD เป็นบวก?
A
โรคที่ทำให้ RAPD เป็นบวกแบ่งออกเป็นสองกลุ่มใหญ่คือ ความผิดปกติของเส้นประสาทตา และโรคจอประสาทตา ชนิดกว้าง ความผิดปกติของเส้นประสาทตา ได้แก่ ปลายประสาทตาอักเสบ, โรคเส้นประสาทตา จากการบาดเจ็บ, โรคเส้นประสาทตา จากขาดเลือด (เช่น NAION ) และโรคเส้นประสาทตา จากการกดทับ โรคจอประสาทตา ชนิดกว้าง ได้แก่ หลอดเลือดแดงจอประสาทตา ส่วนกลางอุดตัน (CRAO ), จอประสาทตาลอก เป็นบริเวณกว้าง และ AZOOR 1) รูที่จุดรับภาพและโรคเส้นประสาทตา สองข้างแบบสมมาตรไม่ทำให้ RAPD เป็นบวก ต้องจำไว้ว่ารอยโรคหลังจุดไขว้ (แถบรังสีแก้วตาและคอร์เทกซ์การเห็น) ก็ไม่ทำให้เกิด RAPD เช่นกัน
รีเฟล็กซ์รูม่านตา ต่อแสงเกิดขึ้นผ่านเส้นทาง 8 ขั้นตอนดังนี้:
จอประสาทตา (การรับแสง)เซลล์รับแสง และเซลล์ปมประสาทจอตาที่ไวต่อแสง ภายในซึ่งมีเมลาโนพซิน (ipRGC )เส้นประสาทตา (ทางนำเข้า)เส้นประสาทตา ส่งข้อมูลแสงไปยังระบบประสาทส่วนกลางจุดไขว้ประสาทตา : เส้นใยจากด้านจมูกข้ามไปยังด้านตรงข้ามทางเดินประสาทตา (optic tract) : ในส่วนหลัง เส้นใยบางส่วนแยกออกและไปยังสมองส่วนกลาง แทนที่จะไปยัง lateral geniculate bodytegmentum ของสมองส่วนกลาง (นิวเคลียส Edinger-Westphal) : เป็นศูนย์กลางของรีเฟล็กซ์รูม่านตา สั่งให้หดรูม่านตา เส้นประสาทกล้ามเนื้อตา (ทางออก) : เส้นใยประสาทพาราซิมพาเทติกเดินร่วมกับเส้นประสาทกล้ามเนื้อตาปมประสาทซิลิอารี (ciliary ganglion) : เส้นใยหลังปมประสาทจากเส้นประสาทกล้ามเนื้อตาสร้างไซแนปส์กล้ามเนื้อหูรูดรูม่านตา (miosis) : การหดตัวของรูม่านตา เกิดขึ้นภายใต้การควบคุมของเส้นใยหลังปมประสาท
ในมนุษย์ ขนาดของรีเฟล็กซ์รูม่านตา ทางตรงและทางอ้อมเกือบเท่ากัน ดังนั้นแม้เส้นประสาทตา ข้างใดข้างหนึ่งเสียหาย จะไม่เกิด anisocoria เมื่อลืมตาทั้งสองข้าง อย่างไรก็ตาม เมื่อกระตุ้นตาทั้งสองข้างสลับกัน การตอบสนองเมื่อกระตุ้นข้างที่เป็นโรคและข้างปกติจะแตกต่างกัน1)
ความผิดปกติของทางนำเข้า (จอประสาทตา /เส้นประสาทตา ) : เมื่อส่องแสงที่ข้างที่เป็นโรค การหดตัวของรูม่านตา ทั้งสองข้างไม่เพียงพอ ทำให้ RAPD เป็นบวกความผิดปกติของทางออก (เส้นประสาทกล้ามเนื้อตา) : รีเฟล็กซ์ตรงข้างที่เป็นโรคหายไป ในขณะที่รีเฟล็กซ์อ้อมยังคงอยู่ (ความผิดปกติของกล้ามเนื้อหูรูดรูม่านตา ข้างเดียวกัน)
ทางเดินซิมพาเทติกดำเนินไปดังนี้: ไฮโปทาลามัส → ไขสันหลัง (intermediolateral column C8-T2) → ปมประสาทซูพีเรียเซอร์วิคัล → เส้นประสาทซิลิอารียาว → กล้ามเนื้อขยายรูม่านตา ในความผิดปกติของซิมพาเทติก (กลุ่มอาการฮอร์เนอร์ ) กล้ามเนื้อขยายไม่ทำงาน ทำให้การขยายรูม่านตา ในที่มืดบกพร่อง
ipRGC มี melanopsin ซึ่งมีบทบาทสำคัญในการรักษาการหดตัวของรูม่านตา ต่อการกระตุ้นด้วยแสงอย่างต่อเนื่อง มีหน้าที่รับผิดชอบองค์ประกอบที่คงอยู่ของรีเฟล็กซ์รูม่านตา หลังการปรับตัวต่อแสง2)
การทดสอบไฟฉายแกว่ง
การเตรียม : ทำในห้องมืด เปิดตาทั้งสองข้าง (ไม่ปิดตาข้างใดข้างหนึ่ง) ต้องทำก่อนหยอดยาขยายรูม่านตา
ขั้นตอน : ฉายไฟฉายไปที่ตาทีละข้างสลับกันประมาณ 1-2 วินาที ระยะเวลาและความเข้มของแสงต้องเท่ากันสำหรับทั้งสองข้าง
การประเมิน : หากสังเกตเห็นรูม่านตา ขยายเมื่อย้ายแสงไปยังตาอีกข้าง แสดงว่าตาข้างนั้นมี RAPD
ตัวอย่าง (โรคเส้นประสาทตา ข้างซ้าย) : ฉายตาขวา → รูม่านตา ทั้งสองข้างหด ย้ายไปตาซ้าย → รูม่านตา ขยาย กลับไปตาขวา → หด ตาซ้าย → ขยาย วงจรเกิดขึ้นซ้ำ 1)
การวัดปริมาณ RAPD ด้วยฟิลเตอร์ ND
หลักการ : วางฟิลเตอร์ความหนาแน่นเป็นกลาง (ND filter) ไว้หน้าตาข้างปกติ และหาความเข้มข้นของฟิลเตอร์ที่ทำให้ RAPD หายไปเพื่อวัดปริมาณ RAPD
วิธีการ : เพิ่มฟิลเตอร์ทีละขั้นโดยเพิ่มครั้งละ 0.3 หน่วยล็อก (เช่น 0.3, 0.6, 0.9, 1.2 log unit) และทำ swinging flashlight test ซ้ำ
การประยุกต์ใช้ทางคลินิก : ความเข้มข้นของฟิลเตอร์ ND ที่ทำให้ RAPD หายไปเป็นตัวบ่งชี้ขนาดของ RAPD มีประโยชน์สำหรับการประเมินเชิงปริมาณของผลการรักษา 1)
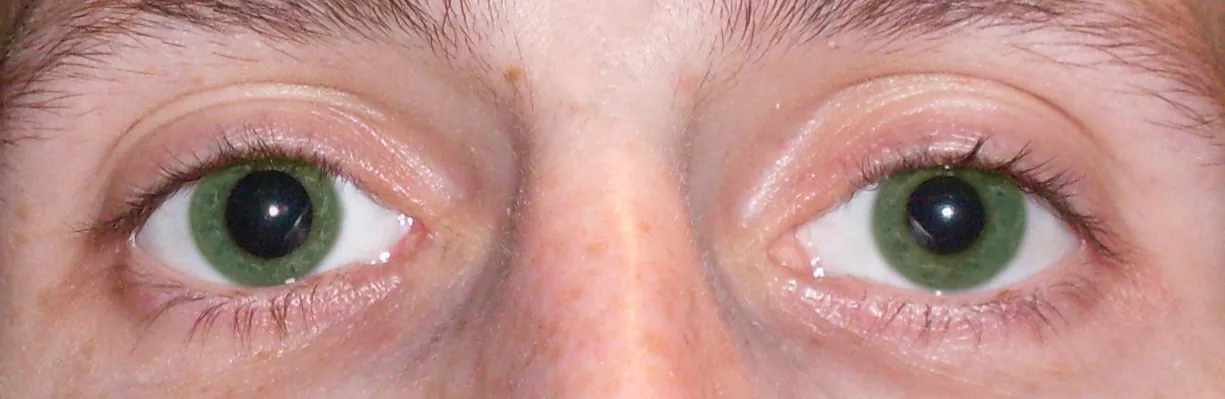
ภาพทางคลินิกของ anisocoria แสดงความไม่เท่ากันของขนาดรูม่านตาระหว่างสองข้าง Russavia. Anisocoria in a 25-year-old male of unknown cause with early facial nerve paralysis. Wikimedia Commons. 2012. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Anisocoria.jpg. License: CC BY 3.0.
ภาพถ่ายภายนอกของดวงตาทั้งสองข้างของชายอายุ 25 ปี แสดง anisocoria โดยขนาด
รูม่านตา ของทั้งสองข้างแตกต่างกันอย่างชัดเจน สอดคล้องกับส่วนข้อความ «การประเมิน Anisocoria (
รูม่านตาไม่เท่ากัน )» ซึ่งกล่าวถึงการแยกความแตกต่างระหว่างความผิดปกติของระบบประสาทซิมพาเทติกและพาราซิมพาเทติกโดยการเปรียบเทียบในห้องมืดและสว่าง
การเปรียบเทียบความแตกต่างของรูม่านตา ในที่มืดและสว่างช่วยแยกความผิดปกติของระบบประสาทซิมพาเทติกและพาราซิมพาเทติก
ความแตกต่างมากขึ้นในที่มืด (รูม่านตา ข้างที่เป็นโรคเล็กกว่า) : บ่งชี้ความผิดปกติของระบบประสาทซิมพาเทติก (Horner syndrome) ในที่มืด รูม่านตา ข้างปกติจะขยายเท่านั้น ทำให้ความแตกต่างเพิ่มขึ้นความแตกต่างมากขึ้นในที่สว่าง (รูม่านตา ข้างที่เป็นโรคใหญ่กว่า) : บ่งชี้ความผิดปกติของระบบประสาทพาราซิมพาเทติก (อัมพาตเส้นประสาทกล้ามเนื้อตา ฯลฯ) ในที่สว่าง รูม่านตา ข้างปกติจะหดเท่านั้น ทำให้ความแตกต่างเพิ่มขึ้นAnisocoria ทางสรีรวิทยา : ภายใน 1 มม. ความแตกต่างคงที่ในที่มืดและสว่าง ปฏิกิริยาต่อแสงยังคงปกติ
ให้ผู้ป่วยจ้องมองเป้าหมายใกล้ (นิ้วหรือสิ่งชี้วัด) และสังเกตปฏิกิริยาใกล้สามอย่าง: การปรับตา, การหุบเข้าหากัน, และการหดตัวของรูม่านตา
การแยกของแสงกับใกล้ (light-near dissociation) : ปฏิกิริยาต่อแสงหายไป แต่ปฏิกิริยาใกล้ยังคงอยู่พบในรูม่านตา Argyll Robertson, รูม่านตา Adie และโรคเส้นประสาทอัตโนมัติจากเบาหวาน
เพื่อระบุตำแหน่งของรอยโรคหรือแยกโรคเฉพาะ ใช้ยาหยอดตาทางเภสัชวิทยา 2) 4) .
Pilocarpine 0.1% : ในรูม่านตา Adie (รอยโรคหลังปมประสาทที่ปมประสาทซิลิอารี) จะเกิดการหดตัวของรูม่านตา ที่เด่นชัดกว่าเนื่องจากการไวเกินจากการเสียประสาท ในตาปกติจะไม่เกิดการหดตัวCocaine 4% : ยับยั้งการนำกลับของ norepinephrine ทำให้รูม่านตา ขยายในตาที่มีประสาทซิมพาเทติกปกติ ในกลุ่มอาการฮอร์เนอร์ รูม่านตา ข้างที่ได้รับผลกระทบจะไม่ขยายหรือขยายไม่เพียงพอHydroxyamphetamine 1% : กระตุ้นการปล่อย norepinephrine จากเซลล์ประสาทหลังปมประสาท ในรอยโรคหลังปมประสาท (รอยโรคของนิวรอนที่สาม) การขยายของรูม่านตา ข้างที่ได้รับผลกระทบจะไม่เพียงพอ ซึ่งแตกต่างจากรูปแบบของรอยโรคก่อนปมประสาท
Q
การทดสอบไฟฉายแกว่ง (Swinging flashlight test) ทำอย่างไร?
A
ในห้องมืดโดยให้ตาทั้งสองข้างเปิด ใช้ไฟฉายส่องตาแต่ละข้างสลับกันประมาณ 1-2 วินาที โดยใช้ระยะเวลาและความเข้มของแสงเท่ากัน การทดสอบนี้ทำก่อนใช้ยาหยอดตาขยายรูม่านตา เสมอ หากพบว่ารูม่านตา ขยายในตาที่ถูกส่องแสง แสดงว่าตานั้นมี RAPD ตัวอย่างในโรคเส้นประสาทตา ข้างซ้าย: เมื่อส่องตาขวา (ตาปกติ) รูม่านตา ทั้งสองข้างหดตัว เมื่อย้ายไปส่องตาซ้าย (ตาที่เป็นโรค) จะเกิดการขยายของรูม่านตา 1) แนะนำให้ทำซ้ำรอบนี้ 2-3 ครั้งเพื่อยืนยัน 6) .
หากไม่มีความผิดปกติของจอตา (โดยเฉพาะจุดรับภาพ) : สงสัยโรคเส้นประสาทตา เป็นหลัก ดำเนินการประเมินโรคประสาทตาอักเสบ , โรคเส้นประสาทตา ขาดเลือด, และโรคเส้นประสาทตาถูกกดทับ หากมีโรคจอตากว้างขวาง : สงสัย CRAO หรือจอตาลอกเป็นบริเวณกว้างหากจอตาปกติแต่ RAPD เป็นสัญญาณวัตถุวิสัยเพียงอย่างเดียว : ให้รวม AZOOR ในการวินิจฉัยแยกโรค
การมีหรือไม่มี RAPD เป็นข้อมูลสำคัญในการติดตามเส้นประสาทตา (การฟื้นตัวจากโรคประสาทตาอักเสบ การประเมินหลังบาดเจ็บ) และการประเมินก่อนผ่าตัด การวัดปริมาณด้วยฟิลเตอร์ ND มีประโยชน์ในการประเมินประสิทธิภาพการรักษาอย่างเป็นรูปธรรม 1) .
ต่อไปนี้คือจุดแยกความผิดปกติของรูม่านตา ที่สำคัญ 2) 3) .
โรค/ภาวะ รูม่านตา ข้างใหญ่รีเฟล็กซ์แสง รีเฟล็กซ์การมองใกล้ อาการอื่นๆ รูม่านตาไม่เท่ากัน ทางสรีรวิทยาแปรผัน ปกติ ปกติ ต่างกัน ≤ 1 มม. กลุ่มอาการฮอร์เนอร์ ตาข้างปกติ (ต่างกันมากขึ้นในที่มืด) ปกติ ปกติ หนังตาตก , รูม่านตา เล็ก, เหงื่อออกน้อยอัมพาตเส้นประสาทกล้ามเนื้อตา ตาข้างที่ได้รับผล (ความแตกต่างเพิ่มขึ้นในห้องสว่าง) รีเฟล็กซ์ตรงหายไป ลดลง ความผิดปกติของการเคลื่อนไหวตา รูม่านตา Adieตาข้างที่ได้รับผล (พบบ่อยในหญิงสาว) ช้า / sector palsy คงอยู่ (ล่าช้า) การแยกแสง-ใกล้, ไวต่อ pilocarpine 0.1% รูม่านตา Argyll-Robertsonไม่มี (รูม่านตา เล็กทั้งสองข้าง) หายไป คงอยู่ ทั้งสองข้าง / ไม่สม่ำเสมอ / ซิฟิลิสระบบประสาท
รูม่านตา Argyll-Robertsonรูม่านตา เล็กและไม่สม่ำเสมอ เป็นลักษณะเฉพาะของโรคซิฟิลิสระบบประสาท 2) รูม่านตา Adie (Holmes-Adie syndrome)รูม่านตา เป็นรูปพัด), การแยกของรีเฟล็กซ์แสง-ปรับใกล้, และการหดตัวของรูม่านตา ที่ไวต่อยาหยด pilocarpine 0.1% มีค่าทางวินิจฉัย 4) อัมพาตเส้นประสาทสมองคู่ที่ 3 : รีเฟล็กซ์ตรงหายไปในตาข้างที่ป่วย, รีเฟล็กซ์อ้อมหายไปเมื่อส่องแสงที่ตาข้างปกติ หากมีอาการผิดปกติของการเคลื่อนไหวลูกตาหรือหนังตาตก ต้องรีบแยกโรคหลอดเลือดโป่งพองของ posterior communicating artery ออก 3)
วิถีนำเข้าประกอบด้วยแอกซอนของเซลล์ปมประสาทจอตา (เส้นประสาทตา ) → ออปติกไคแอสมา → ออปติกแทรกต์ → สมองส่วนกลาง (ส่วนหน้าของนิวเคลียส Edinger-Westphal) ความแตกต่างของการตอบสนองที่เกิดขึ้นตามรูปแบบของความเสียหายมีดังนี้:
การสูญเสียไมอีลิน (optic neuritis) : แอกซอนถูกเก็บรักษาไว้ค่อนข้างดี แต่เกิดการนำสัญญาณช้าลง และพบ RAPD โดยทั่วไป RAPD จะลดลงเมื่อฟื้นตัวความเสียหายของแอกซอน (ischemic/traumatic optic neuropathy) : สัญญาณอ่อนลงและเกิด RAPD การสูญเสียแอกซอนไม่สามารถฟื้นคืนได้ และ RAPD มักคงอยู่โรคจอตากว้างขวาง : เซลล์รับแสง และเซลล์ปมประสาทถูกทำลาย และ RAPD กลายเป็นบวก
วิถีนำออกคือนิวเคลียส Edinger-Westphal → เส้นประสาทสมองคู่ที่ 3 → ปมประสาทซิลิอารี → กล้ามเนื้อหูรูดรูม่านตา ในความเสียหายของวิถีนำออก รีเฟล็กซ์ตรงของตาที่ถูกกระตุ้น (ตาข้างป่วย) หายไป แต่รีเฟล็กซ์อ้อมของตาข้างป่วยเมื่อกระตุ้นตาอีกข้างก็หายไปเช่นกัน ซึ่งเป็นรูปแบบที่แตกต่างจาก RAPD (ความเสียหายของวิถีนำเข้า)
ภาพถ่ายทางคลินิกของม่านตาหด (miosis) ในกลุ่มอาการฮอร์เนอร์ Waster (uploaded by Monopol). Miosis in Horner syndrome, from: Nautiyal A, et al. Painful Horner Syndrome as a Harbinger of Silent Carotid Dissection. PLoS Med. 2005. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Miosis.jpg. License: CC BY 2.5.
ภาพถ่ายภายนอกตาของผู้ป่วย
กลุ่มอาการฮอร์เนอร์ แสดงให้เห็น
ม่านตา หดเนื่องจากความเสียหายของซิมพาเทติกอย่างชัดเจนเมื่อเปรียบเทียบทั้งสองข้าง สอดคล้องกับความบกพร่องของการขยาย
ม่านตา ในที่มืดเนื่องจากความเสียหายของกล้ามเนื้อขยาย
ม่านตา ซึ่งกล่าวถึงในหัวข้อ “ความเสียหายของวิถีซิมพาเทติก (Horner syndrome)”
เส้นทางซิมพาเทติกดำเนินไป: ไฮโปทาลามัส → คอลัมน์อินเตอร์เมดิโอแลเทอรัลของไขสันหลังระดับ C8-T2 → ปมประสาทซูพีเรียเซอร์วิคัล → เส้นประสาทซิลิอารียาว → กล้ามเนื้อขยายม่านตา รอยโรคแบ่งตามนิวรอนลำดับที่ 1, 2 และ 3 และแยกความแตกต่างด้วยการทดสอบหยดไฮดรอกซีแอมเฟตามีน ในรอยโรคนิวรอนลำดับที่ 1 (ส่วนกลาง) และลำดับที่ 2 (ก่อนปมประสาท) จะเกิดม่านตา ขยาย แต่ในรอยโรคนิวรอนลำดับที่ 3 (หลังปมประสาท) จะไม่เกิดม่านตา ขยาย 2)
ipRGC (เซลล์ปมประสาทจอประสาทตา ที่ไวต่อแสง โดยธรรมชาติ) แสดงออกเมลาโนปซินและตอบสนองต่อแสงโดยตรง เซลล์เหล่านี้มีหน้าที่รับผิดชอบองค์ประกอบคงอยู่ของรีเฟล็กซ์ม่านตา ต่อแสง (รีเฟล็กซ์แสงโดยธรรมชาติ) และเกี่ยวข้องกับการหดตัวของม่านตา อย่างต่อเนื่องหลังการกระตุ้นด้วยแสงจ้า ipRGC มักถูกสงวนไว้ค่อนข้างดีในโรคจอประสาทตา ต่างๆ ซึ่งมีส่วนทำให้รีเฟล็กซ์ม่านตา ยังคงอยู่แม้ในกรณีที่เซลล์รูปกรวย และรูปแท่งเสื่อมอย่างรุนแรง 2)
รอยโรคหลังออปติกไคแอสมา (เรเดียชันออปติกาและคอร์เทกซ์การเห็น) ไม่ทำให้เกิด RAPD เนื่องจากอยู่นอกเส้นทางรีเฟล็กซ์ม่านตา ลักษณะนี้มีความสำคัญในการแยกแยะว่าสาเหตุของการมองเห็น ลดลงอยู่ในทางเดินภาพส่วนหน้า (จอประสาทตา หรือเส้นประสาทตา ) หรือส่วนหลัง
ข้อควรระวังหลักในการตรวจมีดังนี้:
ทำในห้องมืด : ความมืดเพียงพอช่วยเพิ่มความแม่นยำในการตรวจหา RAPD เปิดตาทั้งสองข้าง : อย่าปิดตาข้างใดข้างหนึ่งความเข้มแสงเท่ากัน : รักษาความเข้มของไฟฉายให้คงที่ระยะเวลากระตุ้นเท่ากัน : ทำให้ระยะเวลาการส่องแสงเท่ากันในแต่ละตา (สลับกันประมาณ 1-2 วินาที)ทำก่อนขยายม่านตา : ไม่สามารถประเมินได้หลังหยอดยาขยายม่านตา
เครื่องวัดขนาดรูม่านตา อัตโนมัติแบบพกพาและแบบตั้งโต๊ะ (pupillometer) ช่วยให้ประเมิน RAPD ได้อย่างเป็นกลางและเชิงปริมาณ มีการพัฒนาอุปกรณ์ที่ขจัดความแปรผันระหว่างผู้ตรวจ และสามารถวัดได้อย่างแม่นยำในหน่วย 0.01 log unit 5) เนื่องจากสามารถบันทึกการเปลี่ยนแปลงของเส้นผ่านศูนย์กลางรูม่านตา ตามเวลา (ระยะแฝง, แอมพลิจูดการหดตัว, ความเร็วการขยายกลับ) จึงถือเป็นเทคโนโลยีเสริมสำหรับการประเมินตามอัตวิสัยของการทดสอบไฟฉายแกว่ง
โดยใช้การกระตุ้นด้วยแสงสี (แสงสีแดงและสีน้ำเงิน) สามารถประเมินการทำงานของเซลล์รูปกรวย เซลล์รูปแท่ง และเซลล์ ipRGC (เซลล์เมลาโนพซิน) ได้อย่างเลือกสรร กำลังมีการวิจัยเพื่อประเมินระดับความเสียหายของเซลล์แต่ละชนิดแยกกันในจอประสาทตา เสื่อมตามอายุ โรคต้อหิน และจอประสาทตาเสื่อมจากเบาหวาน 2) ซึ่งอาจให้ข้อมูลที่ไม่สามารถได้รับจากรีเฟล็กซ์รูม่านตา ต่อแสงขาวปกติ
กำลังมีการพัฒนาเครื่องวัดขนาดรูม่านตา แบบพกพาที่ใช้กล้องสมาร์ทโฟนและไฟ LED คาดว่าจะนำไปใช้ในต้นทุนต่ำและการแพทย์ทางไกล และถือเป็นเครื่องมือประเมิน RAPD ที่มีแนวโน้มดีในสภาพแวดล้อมที่ไม่มีอุปกรณ์จักษุวิทยาเฉพาะทาง เช่น ห้องฉุกเฉิน สูติศาสตร์ และ ICU 5) อย่างไรก็ตาม การตรวจสอบความแม่นยำและความสามารถในการทำซ้ำยังคงดำเนินอยู่
งานวิจัยเกี่ยวกับความสัมพันธ์ระหว่างความเสียหายทางโครงสร้าง (RNFL บางลงในการตรวจ OCT ) และการทำงานของรูม่านตา (RAPD และการวัดขนาดรูม่านตา แบบสี) ในโรคเส้นประสาทตา จากต้อหิน กำลังสะสมมากขึ้น ความรู้เกี่ยวกับระดับความเสียหายของ iPRGC ในต้อหิน อาจให้ตัวชี้วัดใหม่สำหรับการติดตามการทำงานของต้อหิน 2)
Broadway DC. How to test for a relative afferent pupillary defect (RAPD ). Community Eye Health. 2012;25(79-80):58-59.
Wilhelm H. Disorders of the pupil. Handb Clin Neurol. 2011;102:427-466.
Kawasaki A. Diagnostic approach to pupillary abnormalities. Continuum (Minneap Minn). 2014;20(4):1008-1022.
Bremner FD. Pupil evaluation as a test for autonomic disorders. Clin Auton Res. 2009;19(2):88-101.
Miki A, Iijima A, Takagi M, et al. Pupillography of relative afferent pupillary defects. Jpn J Ophthalmol. 2006;50(3):249-253.
Thompson HS , Corbett JJ, Cox TA. How to measure the relative afferent pupillary defect. Surv Ophthalmol. 1981;26(1):39-42.