瞳孔機能検査は瞳孔 の大きさ・対光反応・近見反応を評価し、視神経 ・中枢神経疾患の診断補助に用いられる
RAPD (相対的瞳孔求心路障害 )はswinging flashlight testで検出され、一側の視神経 や広範な網膜 疾患の存在を示す重要な他覚所見である1) 散瞳 点眼前に必ず実施する。散瞳 後は評価できない暗室・両眼開放・等時間照射(約1〜2秒ずつ)・同一光量が正確なRAPD 検出の条件となる
NDフィルターを健眼前に置くことでRAPD を定量化でき、治療効果の判定にも応用できる
瞳孔不同 は暗室・明室での変化を比較し、交感神経障害(ホルネル症候群 )と副交感神経障害(動眼神経麻痺 )を鑑別する2) Argyll-Robertson瞳孔 は対光反射消失・近見反応保存(光・近見解離)を示し、神経梅毒に特徴的である
瞳孔機能検査は、瞳孔 の大きさ・形・対光反応・近見反応を評価する一連の検査である。主に視神経 ・中枢神経疾患の診断補助として使用され、簡便・非侵襲・即座に実施可能なベッドサイド検査の代表格である。
主な検査目的は以下のとおりである。
RAPD (相対的瞳孔求心路障害 )の検出直接・間接対光反射の評価 :刺激眼と対側眼の縮瞳を観察し、求心路・遠心路障害を鑑別する瞳孔不同 (anisocoria)の原因鑑別ホルネル症候群 ・動眼神経麻痺 を分ける光・近見解離(light-near dissociation)の評価 :Argyll-Robertson瞳孔 ・Adie瞳孔 の鑑別に用いる薬理学的瞳孔 検査 :ホルネル症候群 やAdie瞳孔 の確認・障害部位の鑑別に薬液点眼を利用する
視神経炎 ・外傷性視神経症 ・虚血性視神経症 など視機能を脅かす疾患の急性期評価や、眼科・神経内科の鑑別診断において本検査の情報は臨床判断を大きく左右する。
Q
瞳孔機能検査はどのような情報がわかる検査ですか?
A
瞳孔機能検査では、対光反射の求心路(網膜 ・視神経 )と遠心路(動眼神経)の障害部位を推定できる。特にRAPD は一側の視神経 障害や広範な網膜 疾患の存在を示す他覚所見として重要である1) 。また瞳孔不同 の明室・暗室比較により交感神経・副交感神経障害の鑑別が可能であり、薬理学的点眼検査を組み合わせることで障害部位(節前・節後)まで推定できる場合がある2) 。
RAPD が陽性の場合、一側の視神経 に何らかの障害、あるいは広範な網膜 疾患が存在する。以下にRAPD 陽性・陰性となる代表的な疾患を示す1) 3) 。
眼底(特に黄斑部 )に明らかな異常がないにもかかわらずRAPD が陽性の場合は、視神経 疾患を積極的に疑う。黄斑円孔 ではRAPD は陽性とならない点は重要な鑑別ポイントである。
両側性・対称的な視神経 疾患では両眼の求心路障害が相殺されるためRAPD が検出されない。視交叉 後(視放線 ・視覚野)の病変もRAPD を生じない。
緊急性の高い疾患(CRAO ・急性視神経炎 ・外傷性視神経症 など)の早期スクリーニングとしても本検査の実施が推奨される。
Q
RAPDが陽性になる疾患にはどのようなものがありますか?
対光反射は以下の8段階の経路で成立する。
網膜 (光受容)視細胞 とmelanopsin含有固有光感受性網膜神経節細胞 (ipRGC )で受容される視神経 (求心路)網膜神経節細胞 の軸索が視神経 を形成し、光情報を中枢へ伝達する視交叉 視索 :後半部で一部の繊維が分離し、外側膝状体 ではなく中脳へ向かう中脳被蓋(Edinger-Westphal核) :対光反射の中枢として瞳孔 縮小命令を出力する動眼神経(遠心路) :副交感神経線維が動眼神経に伴行する毛様体 神経節瞳孔 括約筋(縮瞳)
ヒトでは直接対光反射と間接対光反射の大きさはほぼ同じである。したがって一側の視神経 が障害されていても、両眼開放下では瞳孔不同 は生じない。しかし左右眼を交互に刺激した場合、患側刺激時と健側刺激時の反応は異なってくる1) 。
求心路障害(網膜 ・視神経 ) :患側照射時に両眼の縮瞳が不十分となりRAPD 陽性となる遠心路障害(動眼神経) :患側の直接反射が消失し間接反射は保存される(同側の瞳孔 括約筋障害)
交感神経路は視床下部→脊髄(C8〜T2中間外側柱)→上頚神経節→長毛様体 神経→瞳孔 散大筋の経路をたどる。交感神経障害(ホルネル症候群 )では散大筋が機能しないため暗室での散瞳 が障害される。
ipRGC にはmelanopsinが含まれており、持続的な光刺激に対する瞳孔 収縮の維持に重要な役割を担う。明順応後の対光反射の持続成分を担う2) 。
Swinging Flashlight Test
準備 :暗室で実施。両眼は開放(片眼を遮蔽しない)。散瞳 点眼前に必ず行う
手順 :ペンライトを各眼に約1〜2秒ずつ交互に照射する。照射時間・光量は両眼で等しくする
判定 :ペンライトを移動させた際に散瞳 がみられた眼にRAPD が存在すると判定する
例(左眼視神経 障害) :右眼照射→両眼縮瞳。左眼移動→散瞳 。右眼→縮瞳。左眼→散瞳 のサイクルが繰り返される1)
NDフィルターによるRAPD定量
原理 :健眼の前にneutral density filter(NDフィルター)を置き、RAPD が消失するフィルター濃度でRAPD を定量化する
方法 :0.3 log unit刻み(0.3、0.6、0.9、1.2 log unitなど)でフィルターを段階的に追加し、swinging flashlight testを繰り返す
臨床応用 :RAPD が消失するNDフィルターの濃度がRAPD の大きさの指標となる。治療経過の定量的評価に有用である1)
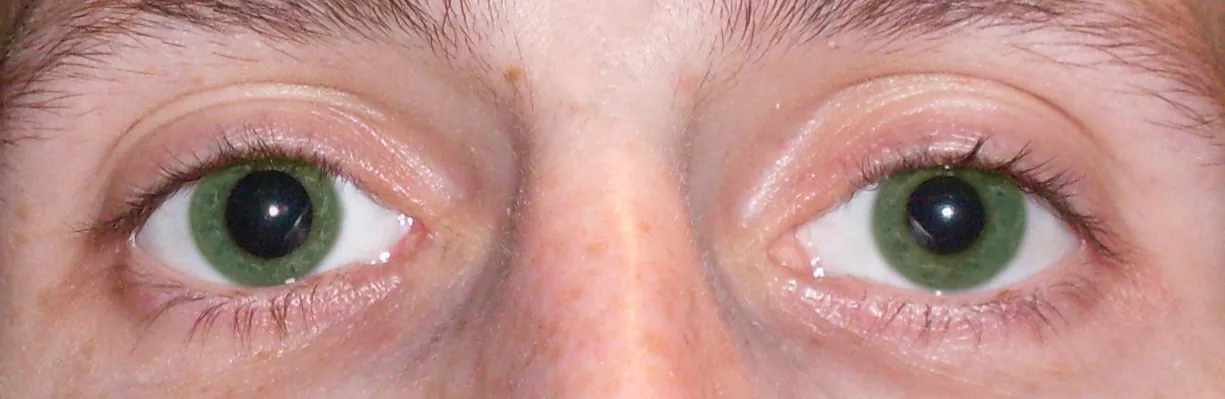
瞳孔不同(anisocoria)の臨床写真。左右の瞳孔径の不均等を示す。 Russavia. Anisocoria in a 25-year-old male of unknown cause with early facial nerve paralysis. Wikimedia Commons. 2012. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Anisocoria.jpg. License: CC BY 3.0.
25歳男性の両眼外観写真で、左右の
瞳孔 径が明らかに異なる
瞳孔不同 を示す。本文「
瞳孔不同 (Anisocoria)の評価」の項で扱う暗室・明室比較による交感神経障害と副交感神経障害の鑑別に対応する。
暗室と明室での瞳孔 差を比較することで、交感神経障害と副交感神経障害を鑑別する。
暗室で不同大(患側が小さい) :交感神経障害(ホルネル症候群 )を示唆。暗室では健眼のみ散大するため差が拡大する明室で不同大(患側が大きい) :副交感神経障害(動眼神経麻痺 等)を示唆。明室では健眼のみ縮小するため差が拡大する生理的瞳孔不同 :1 mm以内。暗室・明室での差が一定で対光反射は正常に保たれる
近見視標(指または指標)に注視させ、調節・輻輳・縮瞳の三大近見反応を観察する
光・近見解離(light-near dissociation) :対光反射が消失しているが近見反応は保存されている状態Argyll-Robertson瞳孔 ・Adie瞳孔 ・糖尿病性自律神経障害などで認められる
障害部位の確定や特定疾患の鑑別に薬物点眼を用いる2) 4) 。
0.1%ピロカルピン点眼 :Adie瞳孔 (毛様体 神経節の節後線維障害)ではdenervation supersensitivityにより健眼よりも顕著に縮瞳する。正常眼では縮瞳は生じない4%コカイン点眼 :ノルエピネフリン再取り込みを阻害し、交感神経が正常な眼では散瞳 する。ホルネル症候群 では患側が散瞳 しないか散瞳 が不十分となる1%ヒドロキシアンフェタミン点眼 :節後ニューロンのノルエピネフリン放出を促進する。節後障害(3次ニューロン障害)では患側での散瞳 が不十分となり、節前障害とは異なるパターンを示す
Q
Swinging flashlight testはどのように行うのですか?
A
暗室で両眼を開放したまま、ペンライトを各眼に約1〜2秒ずつ等時間・等光量で交互に照射する。散瞳 点眼を使用する前に必ず実施する。照射した眼で散瞳 がみられればその眼にRAPD が存在すると判定する。左眼視神経 障害を例にとると、右眼(健眼)照射で両眼が縮瞳し、左眼(患眼)に移動すると散瞳 が生じる1) 。このサイクルを2〜3回繰り返して確認することが推奨される6) 。
眼底(特に黄斑部 )に異常がない場合 :視神経 障害を積極的に疑う。視神経炎 ・虚血性視神経症 ・圧迫性視神経症 などの評価を進める広範な網膜 疾患が存在する場合 :CRAO ・広範な網膜剥離 などを疑う眼底に所見が乏しいがRAPD が唯一の他覚所見である場合 :AZOOR を鑑別に挙げる
視神経 の経過観察(視神経炎 の回復・外傷後の評価)や術前評価においてRAPD の有無は重要な情報となる。NDフィルターによる定量化は治療効果の客観的評価に有用である1) 。
以下に主要な瞳孔異常 の鑑別点を示す2) 3) 。
疾患・病態 大きい瞳孔 対光反射 近見反応 その他所見 生理的瞳孔不同 変動 正常 正常 差は1 mm以内 ホルネル症候群 健眼(暗室で差拡大) 正常 正常 眼瞼下垂 ・逆睫毛・無汗症動眼神経麻痺 患眼(明室で差拡大) 直接反射消失 低下 眼球運動障害 Adie瞳孔 患眼(若年女性に多い) 緩慢・sector palsy 保存(遅延) light-near解離、0.1%ピロカルピン過敏 Argyll-Robertson瞳孔 なし(両側小瞳孔 ) 消失 保存 両側性・不整形・神経梅毒
Argyll-Robertson瞳孔 :光反射消失・近見反応保存・両側性・小さく不整形の瞳孔 が特徴。神経梅毒に特徴的な所見である2) Adie瞳孔 (Holmes-Adie syndrome) :毛様体 神経節の節後線維障害による。sector palsy(扇形の瞳孔 括約筋麻痺)・light-near解離・0.1%ピロカルピン点眼への過敏性縮瞳が診断的価値を持つ4) 動眼神経麻痺 眼球運動障害 ・眼瞼下垂 を伴う場合は後交通動脈瘤を急速に除外する必要がある3)
求心路は網膜神経節細胞 の軸索(視神経 )→視交叉 →視索→中脳(Edinger-Westphal核前部)の経路で成立する。障害様式により生じる反応の違いは以下のとおりである。
脱髄(視神経炎 ) :軸索は比較的保存されるが伝導遅延が生じ、RAPD が認められる。回復とともにRAPD は減弱することが多い軸索障害(虚血性・外傷性視神経症 ) :信号そのものが減弱しRAPD が生じる。軸索喪失は不可逆的であり、RAPD は残存しやすい広範な網膜 疾患 :光受容体・神経節細胞が障害され、RAPD 陽性となる
遠心路はEdinger-Westphal核→動眼神経→毛様体 神経節→瞳孔 括約筋の経路である。遠心路障害では刺激眼(患眼)の直接反射が消失するが、対側眼を刺激した際の間接反射も患眼では消失する。これはRAPD (求心路障害)とは異なるパターンとなる。
ホルネル症候群における縮瞳(miosis)の臨床写真。 Waster (uploaded by Monopol). Miosis in Horner syndrome, from: Nautiyal A, et al. Painful Horner Syndrome as a Harbinger of Silent Carotid Dissection. PLoS Med. 2005. Figure 1. Source ID: commons.wikimedia.org/wiki/File:Miosis.jpg. License: CC BY 2.5.
ホルネル症候群 患者の外眼部写真で、交感神経障害による縮瞳が両眼比較で明瞭に確認できる。本文「交感神経路の障害(
ホルネル症候群 )」の項で扱う
散瞳 筋障害による暗室
散瞳 不全に対応する。
交感神経路は視床下部→脊髄C8〜T2中間外側柱→上頚神経節→長毛様体 神経→瞳孔 散大筋の経路をたどる。障害部位は1次・2次・3次ニューロンに分類され、ヒドロキシアンフェタミン点眼試験で鑑別する。1次ニューロン(中枢性)・2次ニューロン(節前)障害では散瞳 が生じるが、3次ニューロン(節後)障害では散瞳 が生じない2) 。
ipRGC (固有光感受性網膜神経節細胞 )はmelanopsinを発現し、光に対して直接応答する。瞳孔 対光反射の持続成分(intrinsic光反射)を担っており、強光刺激後の持続的な縮瞳に関与する。ipRGC はさまざまな網膜 疾患でも比較的保存されることがあり、錐体・杆体が高度に変性した症例でも対光反射が残存することの一因となる2) 。
視交叉 後(視放線 ・視覚野)の病変は対光反射経路から外れるため、RAPD は生じない。この特性は視力 低下の原因が前視路(網膜 ・視神経 )にあるか後視路にあるかを鑑別する上で重要な情報となる。
検査の主要な注意事項を以下に示す。
暗室で実施 :十分な暗さが必要でRAPD 検出精度が向上する両眼開放 :片眼を遮蔽しないペンライトは同一光量 :フラッシュライトの強度を一定に維持する等時間刺激 :各眼への照射時間を等しくする(約1〜2秒ずつ交互)散瞳 前に実施散瞳 点眼後では評価できない
携帯型・卓上型の自動瞳孔 計(pupillometer)は客観的・定量的なRAPD 評価を可能にする。検者間変動を排除し、0.01 log unit単位での精密な定量が可能な機器が開発されている5) 。瞳孔 径の経時変化(latency・constriction amplitude・redilation velocity)を記録できるため、swinging flashlight testの主観的判断を補完する技術として注目されている。
色光刺激(赤色光・青色光)を使い分けることで、錐体・杆体・ipRGC (melanopsin細胞)それぞれの機能を選択的に評価できる。加齢黄斑変性 ・緑内障 ・糖尿病網膜症 における各細胞タイプの障害の程度を分離して評価する研究が進んでいる2) 。通常の白色光対光反射では評価できない情報を提供する可能性がある。
スマートフォンのカメラとLED照明を用いた携帯型瞳孔 計の開発が進んでいる。低コスト・遠隔医療への応用が期待されており、救急・産科・ICUなど眼科専門機器のない環境でのRAPD 評価ツールとして有望とされる5) 。ただし精度や再現性の検証はなお進行中である。
緑内障 性視神経 障害における構造的障害(OCT -RNFL 菲薄化)と瞳孔 機能(RAPD ・chromatic pupillometry)の相関研究が蓄積されつつある。iPRGC が緑内障 でどの程度障害されるかの知見は、緑内障 の機能的モニタリングに新たな指標を提供する可能性がある2) 。
Broadway DC. How to test for a relative afferent pupillary defect (RAPD ). Community Eye Health. 2012;25(79-80):58-59.
Wilhelm H. Disorders of the pupil. Handb Clin Neurol. 2011;102:427-466.
Kawasaki A. Diagnostic approach to pupillary abnormalities. Continuum (Minneap Minn). 2014;20(4):1008-1022.
Bremner FD. Pupil evaluation as a test for autonomic disorders. Clin Auton Res. 2009;19(2):88-101.
Miki A, Iijima A, Takagi M, et al. Pupillography of relative afferent pupillary defects. Jpn J Ophthalmol. 2006;50(3):249-253.
Thompson HS , Corbett JJ, Cox TA. How to measure the relative afferent pupillary defect. Surv Ophthalmol. 1981;26(1):39-42.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください