Léger
Condition : Pas de compression du nerf optique ni de trouble visuel
Prise en charge : Traitement conservateur uniquement
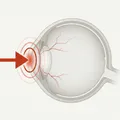
L’emphysème orbitaire est une accumulation anormale d’air dans l’orbite ou les paupières. C’est une affection généralement bénigne et relativement rare, qui se résorbe spontanément en 7 à 10 jours sans séquelles dans la majorité des cas.
La fracture de la paroi orbitaire en est la cause la plus fréquente. La spécificité de l’emphysème orbitaire pour une fracture orbitaire est de 99,6 %, avec une valeur prédictive positive de 98,4 %. La corrélation est particulièrement forte avec les fractures de la paroi médiale, où jusqu’à 75 % des cas présentent un emphysème orbitaire associé 7).
L’emphysème palpébral survient principalement après un traumatisme et se résorbe généralement en quelques jours. L’emphysème orbitaire se résorbe spontanément en quelques jours.
La plupart des cas se résolvent spontanément en 7 à 10 jours sans traitement spécifique ni séquelles. Cependant, en cas d’emphysème orbitaire sous tension avec mécanisme de valve unidirectionnelle, une évolution vers un syndrome compartimental orbitaire est possible, nécessitant une prise en charge urgente en présence de symptômes de neuropathie optique.
Selon la classification de Roelofs, elle est divisée en trois stades2).
Léger
Condition : Pas de compression du nerf optique ni de trouble visuel
Prise en charge : Traitement conservateur uniquement
Modéré
Condition : Signes précoces de compression du nerf optique, trouble visuel léger, augmentation de la pression intraoculaire, exophtalmie modérée
Prise en charge : Ponction à l’aiguille pour décompression ± canthotomie latérale et section du ligament
Sévère
Condition : Compression marquée du nerf optique, trouble visuel sévère, augmentation de la pression intraoculaire, exophtalmie prononcée
Prise en charge : Décompression orbitaire en urgence
Oui. Dans le rapport de Cutting et al. (2021), un cas a été documenté où un RAPD est apparu et une dysfonction du nerf optique s’est produite malgré une pression intraoculaire de 12 mmHg (dans la plage normale)6). Il est important de ne pas juger la sécurité uniquement sur la valeur de la pression intraoculaire, mais d’évaluer globalement le RAPD, l’acuité visuelle et l’exophtalmie.
L’emphysème orbitaire peut survenir pour diverses raisons. La lame papyracée (lamina papyracea) qui sépare les sinus paranasaux de l’orbite a une épaisseur d’environ 0,3 mm et s’amincit davantage avec l’âge, l’ostéoporose et la sinusite chronique, ce qui peut entraîner une fracture ou une diastase même avec une force relativement légère1).
Une comparaison des principales causes et étiologies est présentée ci-dessous.
| Catégorie de cause | Étiologie typique |
|---|---|
| Traumatique | Fracture de la paroi orbitaire (notamment la paroi médiale), lacérations palpébrales et conjonctivales |
| Comportemental/physiologique | Se moucher, éternuer, manœuvre de Valsalva |
| Iatrogène | FESS, rhinoplastie, blépharoplastie, drain thoracique |
| Autres | Barotraumatisme, infection, rupture œsophagienne, idiopathique |
La pression intranasale peut atteindre plus de 70 mmHg en se mouchant et 176 mmHg lors d’un éternuement bouche et nez fermés 4), ce qui peut provoquer une séparation ou une fracture de la lame papyracée.
Les causes iatrogènes incluent la chirurgie endoscopique fonctionnelle des sinus (FESS) 3), la rhinoplastie 1), la blépharoplastie 4), ainsi que des cas rapportés d’air atteignant l’orbite via le médiastin et le cou après insertion d’un drain thoracique en raison d’une fistule bronchopleurale 9).
C’est possible. La pression intranasale lors du mouchage peut atteindre plus de 70 mmHg, et si la lame papyracée est amincie par l’âge ou une sinusite chronique, elle peut se disjoindre ou se fracturer4)6). Même sans antécédent de fracture orbitaire, un cas a été rapporté chez un patient atteint de rhinite allergique qui, en se mouchant fortement le lendemain d’un traumatisme, a aggravé un emphysème orbitaire2).
La première étape consiste à rechercher une crépitation à la palpation des paupières et de l’orbite. Ce signe est considéré comme spécifique de l’emphysème orbitaire. Il est impératif de recueillir les antécédents de traumatisme, de sinusite, de mouchage, d’éternuement ou de chirurgie récente.
Les caractéristiques de chaque examen d’imagerie sont présentées ci-dessous.
| Examen | Caractéristiques | Points d’attention |
|---|---|---|
| Radiographie standard | Évocateur par le « signe du sourcil noir » | Taux de faux négatifs de 50 %, difficile de détecter les microfractures |
| TDM | Méthode diagnostique la plus déterminante | Les deux fenêtres (parties molles et osseuses) sont nécessaires |
| POCUS | Alternative à la TDM, sans irradiation | Nécessite un équipement spécialisé |
Le traitement est choisi par étapes en fonction de la sévérité.
La plupart des cas se résolvent spontanément sans traitement ni intervention chirurgicale. Les conseils suivants et un traitement symptomatique sont recommandés.
Connecter une aiguille à une seringue contenant une solution saline et aspirer l’air intra-orbitaire. Cela permet de surveiller la libération de bulles d’air, évitant ainsi les lésions tissulaires dues à l’aspiration 2)6).
Cutting et al. (2021) ont rapporté un cas d’emphysème orbitaire non traumatique récurrent ayant conduit à un syndrome du compartiment orbitaire. Ils ont ponctionné près du caroncule lacrymale avec une canule 16G et aspiré 7 mL d’air, ce qui a immédiatement résolu la proptose et la diplopie 6).
Chew et al. (2025) ont réalisé une canthotomie latérale sans cantholyse chez un patient présentant un syndrome de compartiment orbitaire avec une pression intraoculaire de 48 mmHg due à un emphysème orbitaire sous tension. En association avec l’acétazolamide systémique, la pression intraoculaire a diminué à 28 mmHg et une récupération complète a été observée après 5 jours5).
La classification de Hunts (stades I à IV) détermine la prise en charge en fonction de la baisse de l’acuité visuelle, de l’élévation de la pression intraoculaire et de la présence d’une occlusion de l’artère centrale de la rétine2).
Il s’agit d’une procédure consistant à connecter une seringue remplie de solution saline et une aiguille (cannule), puis à aspirer l’air accumulé dans l’orbite. La libération des bulles d’air peut être visualisée en temps réel, ce qui permet de prévenir les lésions tissulaires par aspiration. Dans le rapport de Cutting et al. (2021), une canule de calibre 16 a été insérée près de la caroncule lacrymale, et l’aspiration de 7 mL d’air a immédiatement fait disparaître l’exophtalmie et la diplopie6).
Le mécanisme fondamental de l’emphysème orbitaire est un « mécanisme de valve unidirectionnelle » par lequel l’air pénètre dans l’orbite mais ne peut pas en sortir et s’accumule2)5).
La voie d’entrée d’air la plus fréquente est l’entrée depuis les sinus paranasaux via une lame papyracée fracturée ou diastasée. Le tissu adipeux orbitaire lésé agit comme une valve, empêchant l’air de s’échapper de l’orbite.
L’augmentation de la pression intra-orbitaire entraîne les troubles visuels suivants.
Dans l’expérience cadavérique de Heerfordt, une pression interne de 40 à 50 mmHg était nécessaire pour rompre le septum orbitaire lors de l’injection d’air dans l’orbite, la résistance étant la plus forte chez les jeunes sujets 2). L’emphysème orbito-palpébral (état dans lequel le septum orbitaire se rompt et l’air se propage vers les paupières antérieures) peut réduire la pression intra-orbitaire et constituer un signe négatif du syndrome du compartiment orbitaire 2).
Le volume moyen de l’orbite adulte est d’environ 30 mL, un espace conique limité, et l’extensibilité limitée du septum et du tarse le rend vulnérable à l’augmentation de volume 5).
Un déplacement d’air à distance peut également se produire. En raison de la continuité anatomique des plans fasciaux profonds du visage, du cou et du thorax, des cas ont été rapportés où l’air atteint l’orbite via une fistule bronchopleurale → médiastin → cou → fissure orbitaire inférieure 9).
Kanwat et al. (2024) ont publié le premier rapport d’utilisation de la POCUS pour le diagnostic et le suivi en temps réel d’un emphysème périorbitaire survenu après une FESS chez un enfant de 8 ans, dans une situation où la TDM peropératoire n’était pas disponible 3). Le traitement conservateur (pommade Néosporine, bandage compressif) a conduit à une résolution complète en 36 heures.
La POCUS, sans exposition aux rayonnements et réutilisable, attire l’attention comme outil diagnostique alternatif, en particulier chez les enfants et dans les situations d’urgence où la TDM n’est pas disponible.
Boustany et al. (2023) ont rapporté le cas d’une femme de 63 ans ayant présenté une diplopie verticale binoculaire transitoire après une rhinoplastie. Après 2 heures de positionnement en décubitus latéral gauche, l’air extraconique de 4 mm × 3 mm dans la partie supérieure de l’orbite a été dirigé vers le site d’entrée, et la diplopie a disparu 1).
Cette technique est une application des principes de la manœuvre d’Epley pour le vertige paroxystique positionnel bénin et de la manœuvre de Durant pour l’embolie gazeuse, et a été rapportée de manière limitée comme une approche non invasive pour l’emphysème extraconique léger.
AlSubaie et al. (2022) ont rapporté de bons résultats anatomiques et fonctionnels à un an postopératoire chez deux patients ayant subi une reconstruction de fracture blow-out du plancher orbitaire (BOF) à l’aide d’un implant en polyméthacrylate de méthyle (PMMA) modelable 8). Ses caractéristiques incluent un faible coût, la possibilité d’être modelé peropératoire et l’absence de fixation après durcissement, mais les résultats à long terme sont inconnus.