안축장 오차
가장 큰 오차 원인: 안축장은 가장 중요한 매개변수로, 인공수정체 도수를 약 2.5~3배 변화시킵니다.
압박 오차: 접촉식 A-scan에서는 각막 압박으로 인해 안축장이 짧게 측정됩니다.
장안에서의 과대 평가: 광학식에서는 안구 전체에 일률적인 굴절률을 적용하므로, 안축장 25mm 초과인 눈에서는 과대 평가가 발생합니다.

생체계측(biometry)은 생물학에 수학을 적용하는 측정법의 총칭입니다. 안과 영역에서는 백내장 수술 시 인공수정체(IOL) 도수 계산을 위해 눈의 각 부분 치수를 정밀하게 측정하는 것을 말합니다.
눈의 굴절력은 주로 각막, 수정체, 안내 투광체 및 안축장(AL)에 의해 결정됩니다. 백내장 수술에서는 혼탁한 자연 수정체를 제거하고 인공수정체로 교체하므로, 수술 후 목표 굴절을 얻으려면 사전에 인공수정체 도수를 정확히 계산해야 합니다.
1949년 Harold Ridley가 처음으로 인공수정체 이식을 시행했을 때, 환자는 약 20D의 굴절 오차(refractive surprise)가 발생했습니다. 이후 1960년대 후반에 버전스 공식을 이용한 인공수정체 도수 추정이 이루어져 현대 계산법의 출발점이 되었습니다. 1970년대에는 초음파 A모드법이 확립되었고, 이후 계산식은 더욱 정교화되었습니다.
안축장, 각막 굴절력(K값), 전방 깊이(ACD), 수정체 두께(LT), 각막 직경(백색 윤부 직경: WTW)을 측정합니다. 이러한 매개변수로부터 유효 수정체 위치(ELP)를 예측하고 필요한 인공수정체 도수를 산출합니다.
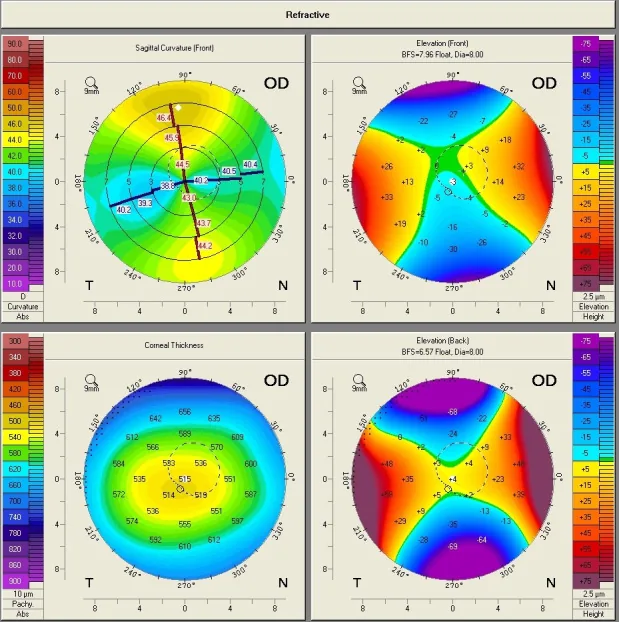
생체계측 자체는 검사법이며 질환이 아닙니다. 측정 정밀도가 불충분한 경우 수술 후 굴절 오차(refractive surprise)가 발생하며, 환자는 다음과 같은 증상을 호소합니다.
수술 후 굴절 오차의 주요 발생 원인은 세 가지입니다.
안축장 오차
가장 큰 오차 원인: 안축장은 가장 중요한 매개변수로, 인공수정체 도수를 약 2.5~3배 변화시킵니다.
압박 오차: 접촉식 A-scan에서는 각막 압박으로 인해 안축장이 짧게 측정됩니다.
장안에서의 과대 평가: 광학식에서는 안구 전체에 일률적인 굴절률을 적용하므로, 안축장 25mm 초과인 눈에서는 과대 평가가 발생합니다.
각막 굴절력 오차
두 번째 오차 원인: K값 1D의 오차가 거의 1:1로 인공수정체 도수 오차에 반영됩니다.
측정 범위 문제: 각막곡률계는 직경 3.2mm 영역을 측정하므로 중심 각막의 실제 굴절력과 차이가 있을 수 있습니다.
굴절교정수술 후 눈: 전후면 곡률비의 변화로 인해 각막 굴절력이 과대평가됩니다.
ELP 예측 오차
유효 수정체 위치 예측 오차: 수술 전에 인공수정체가 낭 내에서 어느 위치에 자리잡을지 정확히 예측하는 것은 어렵습니다.
계산식 의존성: ELP 예측 정확도는 각 세대 계산식 간 차이의 주요 원인입니다.
ESCRS 가이드라인은 수술 전 측정의 정확성, 적절한 계산식 선택, 인공수정체 위치 예측을 굴절 오차 감소의 중요 포인트로 강조합니다. 안축장 및 각막 곡률의 측정 정확도는 생체측정의 발전으로 향상되었지만, 인공수정체 위치 예측 정확도는 사용하는 계산식에 크게 의존합니다1).
수술 후 굴절 오차를 증가시키는 위험 요인은 다음과 같습니다.
진한 백내장이나 고정이 어려운 눈에서는 광학식 측정이 어려울 수 있습니다. 이 경우 침지식 A-scan 등의 초음파 생체측정법을 고려합니다1). 접촉식에서는 각막 압박으로 인한 단축 오차에 주의합니다.
| 파라미터 | 약어 | 의의 |
|---|---|---|
| 안축장 | AL | 가장 중요. 정상 평균 24mm |
| 각막 굴절력 | K | 두 번째로 중요. 1:1로 인공수정체 도수에 영향 |
| 전방 깊이 | ACD | ELP 예측에 필요 |
| 수정체 두께 | LT | 신세대 공식의 추가 변수 |
| 각막윤부 백색 직경 | WTW | ELP 예측 및 안내렌즈 크기 결정에 사용 |
광학식 생체계측은 부분결맞음간섭법(PCI)을 이용한 비접촉 측정법으로, 초기 장비(IOL Master) 이후 표준적인 방법입니다. 접촉식 A-초음파법에 비해 각막 압박에 의한 안축장 단축을 피할 수 있고, 측정자 의존성도 적습니다3). 새로운 형태의 스위프트 소스 OCT는 기존 PCI보다 더 많은 백내장안에서 측정 가능합니다3).
AAO 백내장 PPP는 광학식 생체계측이 황반이 후포도종의 경사벽에 위치하는 경우에도 ‘굴절성 안축장’을 측정하므로 표준 초음파 A-모드법보다 정확하다고 기술합니다. 또한 안내 실리콘 오일이 있는 경우에도 광학식이 더 사용하기 쉽다고 알려져 있습니다3).
광학식 생체계측의 한계로는 모든 눈에 일률적인 굴절률을 적용하는 점이 있습니다. 고도 근시안에서는 유리체 젤의 부피 비율로 인해 실제 안축장이 과대평가되어 표준 계산식에서는 안내렌즈 도수가 과소평가됩니다. 안축장이 25mm를 초과하는 눈에서는 Wang-Koch 조정을 적용할 수 있습니다(단, Barrett Universal II나 Hill-RBF 등 신세대 공식에는 적용 불필요)3).
초음파 A-모드법은 기계적 진동파를 사용하며, 펄스가 각막에서 망막까지 이동하는 시간을 측정합니다. 음속은 매질에 따라 다르며(수정체·각막 약 1641m/s, 방수·유리체 1532m/s), 정상 유수정체안의 평균은 1555m/s입니다. 접촉법(압평법)은 각막을 압박하므로 안축장이 인위적으로 단축되기 쉽고, 측정 정밀도는 검사자의 숙련도에 크게 의존합니다3). 침지법(immersion)은 프로브가 각막에 직접 닿지 않아 압박 오차를 피할 수 있지만, 정렬 제어가 어렵습니다.
각막 굴절력 측정에는 수동 각막곡률계, 자동 각막곡률계, 컴퓨터 비디오 각막지형도, 샤임플러그 카메라(펜타캠 등), 전안부 OCT가 사용됩니다3).
표준 각막곡률계는 중심 각막이 완전한 구면이라는 가정에 기초하여, 전면 곡률로부터 후면 곡률을 추정합니다(전후면 곡률비 고정). 이 가정은 굴절교정수술 후 눈에서는 성립하지 않습니다. 정상안에서 평균 각막 전면 곡률 반경은 7.5mm(약 44.44D), 후면은 전면보다 평균 1.2mm 작습니다.
안내렌즈 도수 계산식은 이론식, 회귀식, 그리고 이 둘의 혼합식으로 크게 나뉘며, ‘세대’로 분류됩니다.
현재 가장 중요한 변수는 **유효 렌즈 위치(ELP)**의 예측이며, 각 계산식의 세대적 진화의 핵심은 ELP 예측 정확도 향상에 있습니다.
각 주요 계산식의 변수는 아래와 같습니다. 안축장과 각막 굴절력 외에도 각 식이 사용하는 추가 변수에 차이가 있습니다3).
| 계산식 | 추가 변수 | 특징 |
|---|---|---|
| Barrett Universal II | ACD, LT, WTW | 이론적 광선 추적 + 데이터 기반 |
| Haigis | ACD | 3변수 다중 회귀 분석 |
| Hill-RBF | ACD, LT, WTW | AI 기반 패턴 인식 |
| Hoffer Q | 없음 | 개인화된 전방 깊이 상수 최적화 |
| Holladay 1 | 없음 | Surgeon factor로 ACD 도출 |
| Holladay 2 | ACD, LT, 나이, WTW, 수술 전 굴절력 | 비선형 회귀로 Holladay 1 업데이트 |
| Kane | ACD, 성별, LT, 각막 두께 | 이론 광학 + 회귀 + AI |
| SRK/T | 없음 | 이론 광학과 회귀 분석의 융합 |
SRK 공식(Sanders·Retzlaff·Kraff)은 현재 권장되지 않지만, 변수 간의 관계 이해에 유용합니다(P = A − 0.9K − 2.5AL).
국내에서는 3세대 SRK/T 공식이 널리 사용되지만, 안축장 및 전안부 형태에 따라 여러 계산 결과를 비교하는 것이 바람직합니다. 백내장 수술 희망자의 약 15%에서 안축장과 각막 굴절력이 균형을 이루지 못한 안구가 관찰됩니다.
신세대 공식(Barrett Universal II, Kane, Hill-RBF 등)은 이론 광학, 회귀, AI 기법을 결합하여 기존 공식에서 오차가 컸던 단안·장안에서도 정확도 향상을 목표로 개발되었습니다4).
단일 구세대 공식에만 의존하면 안축장의 양 끝에서 굴절 오차가 증가하기 쉽습니다. 여러 공식의 비교와 증례 특성에 따른 선택이 중요합니다4, 6).
신세대 공식 간 평균 절대 오차(MAE)의 차이는 대개 작습니다6). 그러나 안축장 범위에 따라 정확도가 다르므로 다음과 같은 선택을 고려합니다.
단안축안(22mm 이하)
Hoffer Q 공식과 Holladay 2 공식은 단안축안에서 비교되어 온 대표적인 공식입니다.
ACD < 2.5mm: ELP 예측 오차가 커지기 쉬우므로 여러 공식을 비교합니다6).
장안축안(24.5mm 이상)
24.5~26.0mm: 3세대 공식과 신세대 공식의 결과를 비교합니다.
26.0mm 이상: 장안축안에서는 공식별 계통 오차에 주의합니다. 필요에 따라 Wang-Koch 안축장 조정을 고려합니다6).
신세대 공식(Olsen, EVO, Kane, Hill-RBF, Barrett II)은 광범위한 안축장에서 평가되었습니다6).
안내렌즈 제조사가 제공하는 렌즈 상수(A 상수)는 어디까지나 권장값이며, 실제 사용하는 생체측정법과의 일관성이 보장되는 것은 아닙니다. 술자의 실제 수술 후 굴절 결과에 기반한 상수 최적화 또는 여러 술자의 데이터를 집적한 온라인 데이터베이스(예: ULIB: User Group for Laser Interference Biometry)의 활용이 유용합니다3).
광학식 생체측정기를 사용하는 경우 광학식 전용 안내렌즈 상수를 사용합니다. IOLMaster 사용 시 신호대잡음비(SNR) ≥5인 측정값을 채택합니다.
각막곡률계로 측정한 각막 난시가 직난시 2D 이상, 도난시 1.5D 이상인 경우 난시 교정용 안내렌즈 적응을 고려합니다. 2016년 체계적 문헌고찰 및 메타분석에서 난시 교정용 안내렌즈는 각막 이완 절개와 병용한 경우를 포함하여 비난시 교정용 안내렌즈보다 잔여 난시가 적은 것으로 나타났습니다3).
계산에는 제조사 제공 온라인 계산기 또는 광학식 생체측정기 내장 Haigis-T식, Barrett Toric식 사용이 권장됩니다. 이들은 측정값을 직접 불러올 수 있어 입력 오류 위험이 낮습니다. 수술 전 각막 난시 1D 이상인 증례는 백내장 수술 환자의 약 1/3에서 확인되며, 토릭 안내렌즈의 잠재적 적응증이 많습니다.
주요 토릭 계산식으로는 Barrett Toric식(각막 후면 난시를 경험적으로 고려), Kane Toric식(AI, 회귀, 이론 광학의 복합 알고리즘), EVO 2.0 Toric식(이론적 각막 후면 난시와 두꺼운 렌즈 모델 통합)이 있습니다. Kane Toric식은 다른 식과 비교하여 평균 절대 예측 오차가 유의하게 낮다는 보고가 있습니다.
토릭 안내렌즈의 축 회전에 주의해야 합니다. 1도 회전 시 약 3%의 난시 교정 효과가 감소하고, 30도 회전 시 교정 효과가 소실됩니다.
굴절교정수술(LASIK, PRK, RK)은 각막 전후면의 곡률비를 변화시킵니다. 각막곡률계는 전면 곡률만으로 후면을 추정하기 때문에 수술 후 눈에서는 각막 굴절력을 과대평가합니다. 또한 많은 안내렌즈 계산식은 ELP를 안축장과 각막 굴절력으로부터 예측하지만, 교정수술 후에는 이 관계가 변화하여 계산식에도 오차가 발생합니다(굴절교정수술 후 눈의 대응 참조).
현대 계산식의 대부분은 Fyodorov의 이론식에 기반합니다:
P = (1336/[AL−ELP]) − (1336/[1336/{1000/([1000/DPostRx] − V) + K} − ELP])
이 식에서 수술 전에 측정할 수 없는 유일한 변수는 ELP이며, 후속식(Holladay, Hoffer Q, SRK/T, Haigis 등)은 모두 ELP 추정의 정확도 향상을 목표로 합니다.
무수정체안: 초음파 속도가 1532m/s가 되며, 두 개의 수정체 스파이크가 소실되고 단일 스파이크로 대체됩니다. 모양체고랑 고정 시 계산상 ACD 값을 0.25mm 감합니다.
위수정체안: 인공수정체 내 초음파 속도는 안내렌즈 재질에 따라 다릅니다(PMMA: 보정계수 +0.45, 실리콘: −0.56 또는 −0.41, 아크릴: +0.30). 위수정체안에서 안축장 재측정에는 광학식이 권장됩니다.
후부 유리체절제술 후·실리콘오일 충전안: 가장 흔한 두 종류의 실리콘오일은 음속이 다릅니다(1050m/s와 980m/s). 광학식 측정이 초음파법보다 정확하며, 또한 안내 실리콘은 양볼록 안내렌즈 이식 시 마이너스 렌즈로 기능하므로 안내렌즈 도수를 3~5D 조정해야 합니다.
굴절교정수술 후 눈에는 주로 세 가지 오차가 발생합니다.
각 방법의 LVC 후 및 RK 후 적용 가능성은 아래와 같습니다.
| 방법 | LVC 후 | RK 후 |
|---|---|---|
| 임상 병력법 | ○ | × |
| 콘택트렌즈 과교정법 | ○ | ○ |
| 중앙 링 토포그래피법 | × | ○ |
각막 전후면의 직접 측정 장비로는 Pentacam(회전식 샤임플러그 카메라, TrueNetPower 맵 및 Holladay Report 등가 K값 산출, 임상 병력 데이터가 없는 경우 대체법), 전안부 OCT(각막 전후면 굴절력 직접 측정, 광선 추적 소프트웨어 OKULIX와 병용 가능), Orbscan(슬릿 스캐닝 + 플라시도 디스크, 각막 혼탁으로 인한 후면 측정 인공물 주의)을 사용할 수 있다7).
과거 데이터에 의존하지 않는 방법으로도 3068%의 증례가 목표 등가구면도수 ±0.5D 이내에 들어가며, 과거 데이터를 필요로 하는 방법이 더 이상 골드스탠다드가 아닙니다6). 여러 방법을 조합한 경우 가장 정확도가 높으며, MedAE 0.310.35D, ±0.5D 이내 비율 66~68%가 보고되었습니다7).
각 수술 기왕력별 예측 정확도는 다음과 같습니다7):
| 수술 기왕력 | ±0.5D 이내 비율 |
|---|---|
| 근시 LASIK/PRK 후 | 0~85% |
| 원시 LASIK/PRK 후 | 38.1~71.9% |
| RK 후 | 29~87.5% |
방사상 각막절개술(RK) 후 눈에서는 ASCRS 포스트RK 안내렌즈 계산기가 유용합니다. 임상 병력법은 RK에서 단계적 중심 각막 편평화(원시화 드리프트)가 발생하기 쉬워 부정확한 경우가 많습니다3). RK 후 눈에서는 다음 사항에 추가로 주의해야 합니다7):
Zeng 등(2022년)은 RK 후 PRK 또는 LASIK을 시행한 환자 2예를 보고했습니다5). 각막 전후면 곡률반경비(B/F비)가 증가한 증례(Case 1, RK+PRK)에서는 Barrett True-K(no history, post-RK)가 가장 정확했으며(실제 사용 IOL과의 차이가 1D 이내), B/F비가 감소한 증례(Case 2, RK+LASIK)에서는 Shammas, Haigis-L, Barrett True-K(no history, post-LASIK/PRK)가 정확도가 좋았습니다.
Zeng 등은 이 소견으로부터 중복 굴절교정수술 후 눈에서는 B/F비(정상안에서는 약 84%)가 안내렌즈 계산식 선택의 중요한 지표가 될 가능성을 시사했습니다5).
소아안, 특히 영유아안은 안축장이 짧아 오차가 증폭됩니다. 또한 안구 성장에 따른 근시화 이동(myopic shift)을 고려한 저교정 전략(undercorrection)이 필요합니다2).
소아안은 다음 점에서 성인안과 근본적으로 다릅니다.
Rathod 등(2025년)의 체계적 문헌고찰에서는 소아 안내렌즈 계산에서 다음이 밝혀졌습니다2).
안내렌즈 계산 정확도에 관한 여러 연구를 통합하면, 신세대 공식(Barrett Universal II, Kane)은 구세대 공식(SRK/T 등)에 비해 특히 2세 이상, 안축장 >21mm인 소아에서 높은 정확도를 보였습니다. 한편, 안축장 <22mm인 눈에서는 Holladay 2, SRK/T, Hoffer Q가 유용하다는 보고도 많아 통일된 견해는 얻어지지 않았습니다2).
AL 및 K 측정은 소아에서 가장 영향력 있는 매개변수입니다. 접촉식 A-scan은 각막 압박으로 인해 안축장을 평균 0.24~0.32mm 짧게 측정하므로, 가능하다면 침지식 A-scan이 권장됩니다 2). WTW 직경이 9mm 미만인 눈에 인공수정체 삽입은 후유착, 속발녹내장 등의 위험으로 인해 피하는 것이 권장됩니다 2).
소아에 대한 저교정 전략의 대표적인 제안값은 다음과 같습니다 (Khokhar 등의 프로토콜).
이는 안구 성장에 따른 근시화 이동을 예상한 설정으로, 성인 시기에 정시에 가깝게 만드는 것을 목표로 합니다 2).
Trivedi 등의 소아 안축장 측정에 관한 무작위 연구에서 접촉식 측정값은 침지식에 비해 평균 0.24~0.32mm 짧았습니다. 소아 안구는 각막 및 공막 강성이 낮아 압박 오차가 발생하기 쉬우므로 침지법이 권장됩니다 2).
현재로서는 통일된 견해가 없습니다. 2세 이상, AL >21mm인 소아에서는 Barrett Universal II 및 Kane 공식의 정확도가 높다고 알려져 있으며, AL <22mm인 단안에서는 Holladay 2, SRK/T, Hoffer Q가 유용하다는 보고가 많습니다 2). 근시화 이동의 개인차가 크기 때문에 저교정 전략과 장기 추적 관찰을 병행하는 것이 중요합니다.
Hill-RBF법(인공지능 기반 패턴 인식)은 실측 데이터로부터 안내렌즈 도수를 추정하는 알고리즘으로, 해부학적 매개변수에 의존하지 않고 작동합니다. Rastogi 등(99안, 4~18세 소아)의 연구에서 Hill-RBF법은 Barrett Universal II, SRK/T, Holladay 1, Hoffer Q 공식과 동등한 예측 정확도를 보였으며, 소아 안과에서 유력한 선택지로 주목받고 있습니다2).
향후 AI 기반 공식은 각 집단의 정상 생체측정 데이터를 활용하여 소아를 포함한 특수안에서도 현재 공식을 능가하는 정확도가 기대됩니다2).
Suzuki 등(2025년)은 안축장 30.0mm 이상의 극단적 축성 근시 80안을 대상으로 AI 기반 안내렌즈 계산 공식의 정확도를 후향적으로 평가했습니다8). Kane 공식과 Hill-RBF 공식은 기존 SRK/T 공식에 비해 유의하게 낮은 평균절대오차(MAE)를 보였습니다. ±0.5D 이내 비율은 SRK/T 26.3%, Barrett Universal II 45.0%, Hill-RBF 55.0%, Kane 65.0%로 AI 기반 공식의 우월성이 입증되었습니다. 안축장 32mm 이상의 하위 그룹에서는 Hill-RBF의 MAE가 0.49D, Kane의 MAE가 0.44D로 가장 우수했습니다8).
2021년에 발표된 AI 계산 공식으로, 기계 학습을 사용하여 각막 후면 곡률 반경과 이론적 렌즈 위치를 예측합니다. 새로운 안내렌즈 모델에 대한 재학습이 필요하지 않은 점이 특징이며, 토릭 안내렌즈나 굴절 교정 수술 후에도 적용 가능하다고 알려져 있습니다. 증거 축적이 기다려집니다.
완전히 공개된 알고리즘을 가지며, 기기에 의존하지 않는 토릭 계산 기능을 통합한 공식입니다6). 알고리즘 투명성 측면에서 독특한 위치에 있습니다.
OCT 데이터에 기반한 광선 추적(Anterion-OKULIX)은 근시 LVC 후안에서 Barrett True K no-history 공식과 비교하여 산술적 예측 오차가 유의하게 낮았다는 보고가 있습니다(−0.13D vs −0.32D)7). 광선 추적법은 각막 전체 표면 형상 데이터를 직접 이용하므로 굴절 교정 수술 후안에 적용 시 이론적 우위가 기대됩니다.
눈 전체에 균일한 굴절률을 사용하는 기존 방법과 달리, 각 세그먼트(방수, 수정체, 유리체)에 개별 굴절률을 적용하는 ‘세그먼트식 안축장 측정’이 연구되고 있습니다. 짧은 눈에서는 최대 0.29mm 크게, 긴 눈에서는 0.50mm 작게 표시되는 것으로 보고되며, 긴 눈과 짧은 눈의 하위 그룹에서 Haigis를 제외한 많은 계산식에서 MAE(평균 절대 오차)의 유의한 개선이 보고되었습니다. 현재 ARGOS(Suntec사)가 세그먼트 방식을 구현하고 있습니다.
한쪽 안내렌즈를 영구적으로 낭내에 두고, 다른 쪽을 일시적으로 모양체구에 두는 ‘Piggyback 안내렌즈’ 접근법이 제안되었습니다. 일시적 안내렌즈는 환자가 성인이 된 후 제거하여 수술 후 굴절을 조정할 수 있습니다2). 실용화를 위한 추가 장기 데이터가 필요합니다.
Optiwave refractive analyzer 등을 이용한 수술 중 파면 수차 측정은 성인의 일반 백내장 수술에서 기존 생체측정과 동등한 수술 후 결과를 얻을 수 있다는 보고가 있습니다. 소아에 대한 적용 가능성은 현재 불명확하며, 추가 연구가 필요합니다2).