中等度

前房洗浄術(Anterior Chamber Washout)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 前房洗浄術とは
Section titled “1. 前房洗浄術とは”前房洗浄術(Anterior Chamber Washout)は、前房内に病的に貯留した物質を灌流液で洗い流す手技である。洗浄の対象となる病的物質には血液・膿・炎症メディエーター・化学物質・粘弾性物質(OVD)などが含まれる。前房洗浄術は独立した疾患ではなく、各種前眼部疾患や術後合併症に対して実施される治療手技として位置づけられる。
前房は約0.2 mLの密閉空間であり、線維柱帯からの房水流出経路のみが実質的な排出路である。病的物質が急速に蓄積する眼内炎・前房出血・化学熱傷などでは自然排出に限界があり、早期の機械的除去が角膜内皮・虹彩・水晶体などの眼内組織保護に直結する。
前房洗浄術の主な適応疾患と目的を示す。
| 適応疾患 | 洗浄の目的 |
|---|---|
| 眼内炎 | 原因菌・起炎物質の除去・角膜内皮および眼内組織の保護 |
| 出血緑内障(前房出血) | 前房出血除去・眼圧コントロール・再出血防止 |
| 乳児の前房出血 | 視覚遮断弱視の発症防止 |
| 再発性出血緑内障(角膜血染症) | 角膜血染の防止・眼圧下降 |
| 化学(アルカリ)熱傷 | 前房内化学物質の除去・炎症の軽減 |
上記5疾患に加え、以下でも前房洗浄が施行される。
- 白内障術後OVD残留高眼圧:術後一過性高眼圧の原因となる粘弾性物質を除去する。
- 白内障術後眼内炎・TASS:感染性眼内炎と非感染性の毒素性前眼部症候群(TASS)は早期鑑別が重要で、前房内炎症物質の除去が必要な症例では前房洗浄を検討する。
- UGH症候群:IOL偏位による虹彩擦過・色素散布・慢性前房出血に対して補助的に施行される。
- MIGS術後・トラベクロトミー術後の前房出血:術後出血が遷延する際に適応となる。
術中前房内抗菌薬投与は術後眼内炎リスクを低下させることがメタアナリシスで示されており1)、前房洗浄の予防的観点からも術中抗菌薬投与の重要性が認識されている。
2. 前房洗浄が必要となる症状と臨床所見
Section titled “2. 前房洗浄が必要となる症状と臨床所見”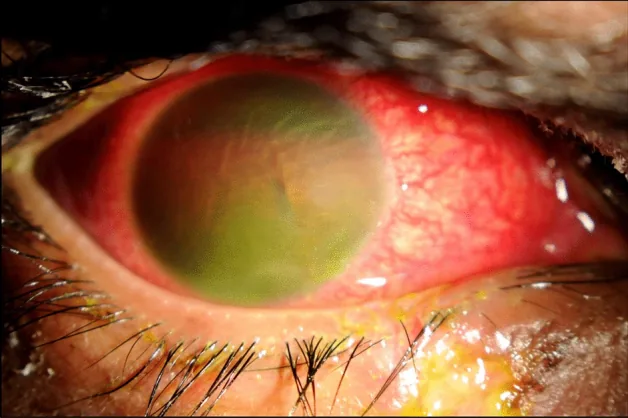
前房洗浄を要する病態ごとに生じる主な自覚症状を以下に示す。
- 眼内炎(感染性):術後数日以内の急激な視力低下・眼痛・充血・眼脂増加。症状の急速な進行が特徴である。
- TASS(非感染性前眼部炎症):術後1〜2日以内の視力低下・充血。感染性眼内炎より早期に発症し、眼痛は比較的軽度なことが多い8)。
- 前房出血:視力低下・眼痛・充血・羞明。出血量に比例して視力低下が増強する。
- 化学熱傷:強い眼痛・充血・視力低下。アルカリ熱傷は前房への浸透が速い。
- OVD残留:白内障術後数時間以内の眼痛・頭痛(眼圧上昇に伴う症状が主体)。
細隙灯顕微鏡検査により前房内を観察し、洗浄の要否と緊急度を判断する。
重度
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”前房洗浄が必要となる各病態のリスク要因を以下に示す。
眼内炎(術後感染性)
Section titled “眼内炎(術後感染性)”白内障術後眼内炎の主なリスク因子は以下の通りである2)7)。
- 術中因子:後嚢破損・硝子体脱出(術後眼内炎リスクが有意に上昇)
- 眼付属器の感染:活動性眼瞼炎・涙嚢炎・涙道閉塞
- 全身因子:免疫不全状態・糖尿病
- 手術因子:手術経験・手術時間の延長・下方切開(眼瞼分泌物の混入リスクが高い)
- 起因菌:最多は表皮ブドウ球菌(coagulase-negative Staphylococcus)であり、全体の約60〜70%を占める7)
TASS(毒素性前眼部症候群)
Section titled “TASS(毒素性前眼部症候群)”非感染性の前眼部炎症であり、主な原因は以下の通りである8)。
- 器械・チューブの不完全な洗浄(酵素洗剤の残留)
- 灌流液への不純物の混入
- 変質した粘弾性物質の使用
- 眼内使用が認可されていない薬剤の誤使用
- 鈍的外傷:最多原因。眼球への圧縮力が虹彩・毛様体の血管を破綻させる。
- 医原性:白内障手術・MIGS術後・UGH症候群。IOLが嚢外固定や非対称固定になると支持部が虹彩を擦過し、虹彩色素が線維柱帯に詰まり色素性緑内障を生じる。虹彩障害が著しいと虹彩毛様体炎と前房出血を伴う(UGH症候群)。
- 自然発生性:虹彩新生血管(糖尿病網膜症・網膜静脈閉塞症)・眼腫瘍・血液疾患(鎌状赤血球症など)。
- 前房出血と高眼圧の遷延が主因。
- 鎌状赤血球症を有する患者では前房内の低酸素環境で赤血球が鎌状化し、少量の出血でも重篤な眼圧上昇を生じやすい。早期の洗浄介入が重要である。
- アルカリ(石灰・強アルカリ洗剤など)は脂肪可溶性のため角膜全層を通過して前房内に浸透し、前房内のpHを急激に変動させる。酸熱傷は角膜実質内でタンパク凝固層を形成するため前房への浸透は限られるが、強酸では前房内へ到達しうる。
4. 診断と検査方法
Section titled “4. 診断と検査方法”前房洗浄術の適応を判断するために以下の検査を組み合わせて実施する。
- 細隙灯顕微鏡検査:前房内の蓄膿・出血・フィブリン・OVD残留を評価する。前房蓄膿の高さ・色調・程度を記録する。
- 眼圧測定:OVD残留は術後数時間以内の急激な眼圧上昇を呈することが多い。前房出血では赤血球による線維柱帯閉塞で眼圧が上昇する。
- 視力検査:初診時および経過観察中に視力の推移を記録する。
- 眼底検査:眼内炎では硝子体混濁の有無が重要であり、前房洗浄単独か硝子体切除術を追加するかの判断に直結する。
- 超音波検査(Bモード):眼底透見不能時に網膜剥離・硝子体混濁の程度を評価する。穿孔性眼外傷が疑われる場合は超音波生体顕微鏡(UBM)は禁忌とする。
- 前房水採取・細菌培養:眼内炎疑いでは27G針でサイドポートから前房水0.2 mLを採取し、細菌培養・薬剤感受性試験に提出する。
- 鎌状赤血球スクリーニング:前房出血患者でリスク群(アフリカ系・地中海系)に対して実施する。
前房洗浄の手術適応基準
Section titled “前房洗浄の手術適応基準”| 病態 | 手術適応基準 |
|---|---|
| 前房出血(健常者) | 50 mmHg以上が5日間持続、または35 mmHg以上が7日間持続 |
| 前房出血(鎌状赤血球症) | 25 mmHg以上が24時間以上持続 |
| 前房出血(角膜血染) | 角膜血染の徴候を認めた時点で緊急施行 |
| 前房出血(乳児・小児) | 全前房出血による視覚遮断が弱視リスクとなる場合 |
| 眼内炎(前房限局型) | 前房蓄膿あり・硝子体混濁が軽度 → 前房洗浄+抗菌薬前房内注入 |
| 眼内炎(硝子体混濁型) | 硝子体混濁が強い場合 → 緊急硝子体切除術を優先 |
5. 標準的な治療法
Section titled “5. 標準的な治療法”前房洗浄術の手技は病態の重症度と施設の状況に応じて選択される。
A. 外来処置法(2箇所穿刺法)
Section titled “A. 外来処置法(2箇所穿刺法)”軽症例や迅速な対応が必要な場合に外来処置として実施される方法である。
- 消毒は内眼手術に準じて行う(ポビドンヨードによる術野消毒)。
- 点眼麻酔で対応可能な場合が多い。
- 角膜に2箇所の穿刺を行う。
- 一方から25G鈍針を装着した注射器でBSS(人工房水)等を注入する。
- 対側の穿刺部近傍を綿棒で軽く押し開いて前房水を排液する。
- 1箇所穿刺のみでは灌流と排液のバランスが保てないため、必ず2箇所の穿刺が必要である。
B. 手術室での前房洗浄(I/A装置使用)
Section titled “B. 手術室での前房洗浄(I/A装置使用)”確実な洗浄を行う場合は手術室にて白内障手術の灌流・吸引(I/A)装置を使用する。
- 眼内炎が疑われる場合はサイドポートから27G針で前房水0.2 mLを採取し細菌培養に提出する4)。
- I/Aチップをサイドポートから挿入し、前房内を吸引・洗浄する。
- フックでIOLを偏位させ、嚢内および支持部周囲も十分に洗浄する。
- 必要に応じて粘弾性物質を前房に注入し、フィブリン膜を硝子体鑷子・前嚢鑷子で除去する。
- 虹彩後癒着が存在する場合は虹彩リトラクターが有用である。
- 抗菌薬などを灌流液に適切な濃度で混入することで、洗浄と薬剤投与を同時に完了できる。
- BSSで前房を再形成し、眼圧をやや高めに調整して終了する。
C. 眼内炎に対する前房洗浄と抗菌薬注入
Section titled “C. 眼内炎に対する前房洗浄と抗菌薬注入”前房内に炎症が限局し硝子体混濁が軽度の場合に適応となる。前房洗浄と同時に以下の抗菌薬を前房内・硝子体内に注入する。
- バンコマイシン:1 mg/0.1 mL(グラム陽性菌カバー)
- セフタジジム:2.25 mg/0.1 mL(グラム陰性菌カバー)
硝子体腔内に混濁が広がっている場合は緊急硝子体切除術を施行する。EVS(Endophthalmitis Vitrectomy Study)では、初期視力が手動弁(HM)以上の急性術後眼内炎において、tap and inject と即座の硝子体切除は同等の視力予後を示した。ただし初期視力が光覚弁(LP)以下では即座の硝子体切除が有意に優れていた3)。
D. 前房出血に対する前房洗浄
Section titled “D. 前房出血に対する前房洗浄”- 角膜サイドポートからシムコ針を用いて前房灌流を行う。
- 出血塊が大きい・硬化している場合は鑷子で摘出するか、硝子体カッターで切除・吸引する。
- 手術時期:受傷後4日目頃が適切である。再出血のリスクが低下し、出血塊が眼組織から分離している時期に相当する9, 11)。
E. TASSに対する前房洗浄
Section titled “E. TASSに対する前房洗浄”TASSは術後1〜2日以内に発症する非感染性前眼部炎症であり、感染性眼内炎との鑑別が重要である。発症時期・眼痛の程度・前房液の培養結果を総合的に判断する8)。前房洗浄と積極的なステロイド点眼で炎症が速やかに軽減する症例が多い。
F. 術式比較
Section titled “F. 術式比較”| 項目 | 外来2箇所穿刺法 | 手術室I/A装置法 |
|---|---|---|
| 麻酔 | 点眼麻酔 | 点眼〜局所麻酔 |
| 洗浄効率 | 低〜中 | 高 |
| 嚢内洗浄 | 困難 | 可能 |
| 適応病態 | 軽症・緊急対応 | 中等度〜重症 |
G. 術後管理
Section titled “G. 術後管理”- 抗菌薬点眼:レボフロキサシン等のフルオロキノロン系点眼薬を使用する。
- ステロイド点眼:ベタメタゾン(リンデロン0.1%等)で炎症を抑制する。
- 眼圧モニタリング:術後の眼圧変動を注意深く観察する。
- 安静・頭部挙上:前房出血洗浄後は頭部を30〜45度挙上し、再出血を予防する10)。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”前房内環境と病的物質の貯留
Section titled “前房内環境と病的物質の貯留”前房は線維柱帯・シュレム管からの房水流出経路が実質的な唯一の排出路である。血液・膿・粘弾性物質・化学物質がこの空間に貯留すると、排出機構が物理的・化学的に閉塞され、眼圧上昇と組織障害の連鎖が生じる。
眼内炎の進行機序
Section titled “眼内炎の進行機序”細菌が前房内で急速に増殖することで以下の連鎖が生じる。
- 細菌由来トキシン・炎症メディエーターが放出される。
- 角膜内皮細胞のポンプ機能が障害されて角膜浮腫が進行する。
- 虹彩・毛様体への炎症波及が後眼部へと拡大する。
- 早期の起炎物質除去が角膜内皮・虹彩・硝子体など眼内組織の保護に直結する。
前房出血による眼圧上昇の機序
Section titled “前房出血による眼圧上昇の機序”前房出血に伴う眼圧上昇は複数の機序で生じる11)。
- 赤血球による線維柱帯閉塞:大量の赤血球が線維柱帯を物理的に閉塞する。
- 溶血性緑内障:溶血したヘモグロビンを含むマクロファージが線維柱帯を閉塞する。
- Ghost cell緑内障:変性赤血球(ghost cell)が変形能を失い線維柱帯を閉塞する。
角膜血染の機序
Section titled “角膜血染の機序”高眼圧が持続し前房出血が遷延すると、角膜内皮のポンプ機能が障害される。ヘモグロビン分解産物(ヘミン・ビリルビン等)が角膜実質に徐々に沈着し、角膜が黄褐色〜茶色に混濁する。一度発症した角膜血染に対しては有効な治療法がなく、吸収を待つのみとなる。そのため予防的観点から、眼圧上昇を伴う遷延性前房出血では早期に前房洗浄を行い角膜血染症の発症を防ぐことが重要である。
OVD残留による眼圧上昇
Section titled “OVD残留による眼圧上昇”粘弾性物質(ヒアルロン酸ナトリウム等)は術中に前房・嚢内に使用されるが、術後に十分除去されない場合、その粘性により線維柱帯を物理的に閉塞し術後一過性高眼圧を引き起こす12)。高分子量・高粘度のOVDほど眼圧上昇のリスクが高い。
化学熱傷の前房内影響
Section titled “化学熱傷の前房内影響”アルカリは脂肪可溶性であるため角膜全層を通過し、前房内のpHを上昇させる。pHの変動が角膜内皮・虹彩実質・水晶体上皮を障害する。アルカリは眼内の脂質膜を溶解して組織壊死を引き起こすため、前房内のアルカリを早急に希釈・除去することが組織障害の軽減に重要となる。
UGH症候群の病態
Section titled “UGH症候群の病態”眼内レンズが嚢外固定または非対称固定になった際に、支持部が虹彩に直接接触・擦過する。虹彩色素が線維柱帯に詰まり色素性緑内障を生じる。虹彩障害が著しいと虹彩毛様体炎と前房出血を伴い(ぶどう膜炎・緑内障・前房出血症候群)、保存的治療で改善しない場合にはIOL交換・摘出が必要となる。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”術中予防的前房内抗菌薬投与
Section titled “術中予防的前房内抗菌薬投与”術後眼内炎の予防として、術中の前房内セフロキシム(1 mg/0.1 mL)投与の有効性が大規模多施設研究で示されている。前房内セフロキシム投与群では眼内炎リスクがオッズ比0.26(95%CI: 0.15〜0.45)と有意に低下した1)。前房洗浄は術後眼内炎の治療手技であるが、予防的介入として術中抗菌薬の前房内投与が普及しつつある。
ポビドンヨード灌流による術中前房内細菌汚染の低減
Section titled “ポビドンヨード灌流による術中前房内細菌汚染の低減”術中に0.25%ポビドンヨード液を用いて眼表面を反復灌流する島田法では、手術終了時の前房内細菌汚染率が低下した(p=0.0017)との報告がある6)。従来の術野消毒に加えた術中灌流が術後眼内炎予防に寄与する可能性がある。
術後眼内炎の全身抗菌薬療法の再評価
Section titled “術後眼内炎の全身抗菌薬療法の再評価”近年のシステマチックレビューでは、術後眼内炎に対する全身抗菌薬の硝子体内移行が限られることが指摘されており5)、全身投与の位置づけは見直しが進んでいる。前房内・硝子体内局所投与が治療の根幹を担い、全身投与はあくまで補助的な役割にとどまるとされつつある。
8. 参考文献
Section titled “8. 参考文献”- Bowen RC, Zhou AX, Bondalapati S, et al. Comparative analysis of the safety and efficacy of intracameral cefuroxime, moxifloxacin and vancomycin on endophthalmitis prophylaxis during cataract surgery: a systematic review and meta-analysis. Br J Ophthalmol. 2018;102(10):1261-1268. doi:10.1136/bjophthalmol-2017-311702. PMID: 29703736.
- Miller KM, Oetting TA, Tweeten JP, et al. Cataract in the Adult Eye Preferred Practice Pattern. Ophthalmology. 2022;129(1):P1-P126. doi:10.1016/j.ophtha.2021.10.006. PMID: 34780842.
- Endophthalmitis Vitrectomy Study Group. Results of the Endophthalmitis Vitrectomy Study. A randomized trial of immediate vitrectomy and of intravenous antibiotics for the treatment of postoperative bacterial endophthalmitis. Arch Ophthalmol. 1995;113(12):1479-1496.
- Wallin T, Parker J, Jin Y, Dubielzig R, Bhattacharya S. Cohort study of 27 cases of endophthalmitis at a single institution. J Cataract Refract Surg. 2005;31(4):735-741.
- Brockhaus L, Goldblum D, Eggenschwiler L, Zimmerli S, Marzolf A, Garweg JG. Revisiting systemic treatment in bacterial endophthalmitis: a systematic review and meta-analysis. Clin Microbiol Infect. 2019;25(10):1234-1241. doi:10.1016/j.cmi.2019.03.005. PMID: 30877061.
- Shimada H, Nakashizuka H. Cataract surgery by intraoperative surface irrigation with 0.25% povidone-iodine. J Clin Med. 2021;10(16):3611. doi:10.3390/jcm10163611. PMID: 34441906.
- Durand ML. Bacterial and fungal endophthalmitis. Clin Microbiol Rev. 2017;30(3):597-613. doi:10.1128/CMR.00113-16. PMID: 28580921; PMCID: PMC5473062.
- Cutler Peck CM, Brubaker J, Woods SE, Chan E, Mettu P, Cousins SW. Toxic anterior segment syndrome: common causes. J Cataract Refract Surg. 2010;36(7):1073-1080. doi:10.1016/j.jcrs.2010.04.025. PMID: 20622677.
- Deutsch TA, Goldberg MF. Surgical management of traumatic hyphema. Ophthalmic Surg. 1983;14(2):137-141.
- Crouch ER Jr, Frenkel M. Aminocaproic acid in the treatment of traumatic hyphema. Am J Ophthalmol. 1976;81(3):355-360.
- Bansal S, Gunasekeran DV, Ang B, Lee J, Khandelwal R, Sullivan P, Agrawal R. Controversies in the pathophysiology and management of hyphema. Surv Ophthalmol. 2016;61(3):297-308.
- Malvankar-Mehta MS, Fu A, Subramanian Y, Hutnik CML. Impact of ophthalmic viscosurgical devices in cataract surgery. J Ophthalmol. 2020;2020:7801093. doi:10.1155/2020/7801093. PMID: 33133677; PMCID: PMC7593745.
