保存的対応(第一選択)

レーシック難民・過矯正への対応
1. レーシック難民・過矯正への対応とは
Section titled “1. レーシック難民・過矯正への対応とは”LASIK(laser in situ keratomileusis)術後に期待された視力改善が得られない、または視覚の質的低下(QOV低下)を生じた患者群は「レーシック難民」と俗称される。この用語は学術的な定義ではなく、他施設で救済を求める患者の実態を表す日本固有の表現である。
過矯正(overcorrection)は、近視矯正LASIKの術後に遠視方向へ矯正過剰となった状態を指す。近業(読書・PC作業)における眼精疲労・頭痛・近見困難が主な問題となる。老視年齢では遠方視力は良好でも中間・近方視力の障害が顕著となり、患者のQOLに大きく影響する。
屈折矯正手術のガイドライン(第8版)では、以下の基本方針を定めている1)。
- 術後屈折度は将来を含めて過矯正にならないことを目標とする
- 近視矯正量は原則6D、十分なインフォームドコンセントのもとに10Dまで
- 残存角膜厚250μm以上を確保する
- 3D以内の近視に対して、老視年齢での近方視力低下のデメリットを術前に十分説明する
QOV低下の原因は過矯正だけではない。高次収差の増加(ハロー・グレア・スターバースト)、ドライアイ(角膜知覚神経切断による涙液減少)、不正乱視(偏心切削・フラップ皺)、DLK(diffuse lamellar keratitis)なども重要な原因となる。ドライアイは術後3〜6か月で多くの症例が改善するが、一部では長期化する。
2. 主な症状と臨床所見
Section titled “2. 主な症状と臨床所見”過矯正による症状:
高次収差・光学的品質の低下:
ドライアイ関連症状:
- 乾燥感・異物感・灼熱感
- 角膜知覚神経切断による涙液分泌減少(術後3〜6か月で多くは回復)
- 角膜トポグラフィ: 近視矯正LASIK後の中央部過度平坦化(過矯正)
- 拡張症進行時: 前面急峻化 + 後面急峻化 + 菲薄化のうち2基準以上の充足3)
- BAD-D(Belin-Ambrósio拡張症スコア)> 2.6: 拡張症異常と判定3)
- PTA(percent tissue altered)≥ 40%: 術前正常角膜でも拡張症リスク有意増加7)
- AS-OCT: フラップ厚・残存実質厚の客観的評価
- 増強手術後の上皮迷入: 鼻下方の前方高低差増加・角膜肥厚・不正乱視の急速進行6)
3. 原因とリスク要因
Section titled “3. 原因とリスク要因”過矯正の原因
Section titled “過矯正の原因”- ノモグラム設定の誤差: エキシマレーザーの過剰切除
- 潜伏性過矯正: 若年者の調節性仮性近視成分を含めた矯正
- 加齢による遠視シフト: 特に3D以内の近視患者が老視年齢に達した場合1)
- 角膜創傷治癒反応のばらつき: 個体差による切削効果の変動
QOV低下の原因
Section titled “QOV低下の原因”- 光学帯径 < 暗所瞳孔径 → 球面収差増加。7mm光学帯では3.50Dの矯正でほぼ高次収差の増加なし
- 偏心切削 → コマ収差
- ドライアイ: 角膜知覚神経切断による涙液分泌減少
- DLK(diffuse lamellar keratitis): フラップ下の非感染性層間炎症
角膜拡張症のリスク因子
Section titled “角膜拡張症のリスク因子”拡張症はQOV低下の中でも特に管理が重要な合併症である3)。
- 若年(角膜リモデリングが活発)
- 高い自覚的屈折等価球面度数
- 角膜厚の減少
- 薄い残余角膜実質床(RSB)厚
- 異常な術前トポグラフィ(潜伏性円錐角膜)
- 全体として、PRKおよびSMILEはLASIKと比較して拡張症リスクが低い3)
4. 診断と検査方法
Section titled “4. 診断と検査方法”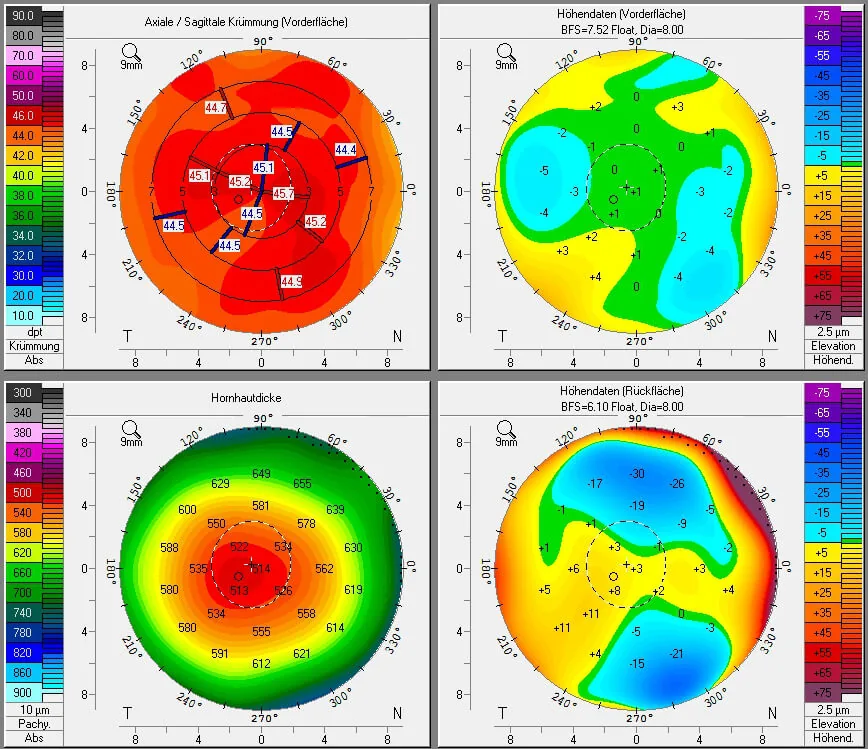
過矯正の診断
Section titled “過矯正の診断”- 自覚的・他覚的屈折検査で術後遠視化を確認
- 調節麻痺下屈折検査(サイプレジン点眼): 潜伏性遠視の正確な定量
- 2色(赤緑)テスト: 赤地の文字が濃く見える場合、網膜前方焦点(過矯正)を示唆
- 角膜トポグラフィ: 中央部の過度平坦化パターン
拡張症スクリーニング指標
Section titled “拡張症スクリーニング指標”| 指標 | 基準値 | 特徴 |
|---|---|---|
| BAD-D | <1.6正常、1.6〜2.6疑い、>2.6異常 | 前後面高低差+角膜厚の統合評価3) |
| PTA | <40%低リスク | (フラップ厚+切削深)/術前中心角膜厚7) |
| KISA% | 60〜100%で潜伏性KC | 中心K+I-S+SRAX |
| Randlemanスコア | 0〜2点低リスク、4点以上高リスク | 年齢+角膜厚+トポパターン+RSB+矯正量 |
ムネリン公式 t = S²D / 3(t: 切除深[μm]、S: 光学帯径[mm]、D: 等価球面度数)で切除深を算出し、RSB = CCT − 切除深 − フラップ厚 として残余角膜実質厚を確認する。最低250μmの確保が必須である1)。
AS-OCTによる評価
Section titled “AS-OCTによる評価”- フラップ厚・残存実質厚の客観的測定
- 上皮厚マッピング: 上皮ドーナツパターン(突出部の上皮菲薄化+周囲の上皮肥厚)は拡張症を示唆
- CLワーページの鑑別: 上皮肥厚+正常角膜厚で拡張症と区別
5. 標準的な治療法
Section titled “5. 標準的な治療法”過矯正への対応は、保存的矯正から段階的に介入する。
追加手術(慎重な適応判断)
増強手術(Enhancement)
Section titled “増強手術(Enhancement)”フラップリフト後にエキシマレーザーを追加照射する増強手術は、屈折状態が非進行性であること・残存角膜厚が十分であることを確認した上で行う1)。Li & Guは増強手術後第1日目から急速に進行した上皮迷入を報告しており、角膜トポグラフィで鼻下方象限の前方高低差増加と同部位の角膜肥厚が確認された。不正斜乱視は第1日の0.6Dから第5日には2.0Dに増大した6)。
TG-LASIK(トポグラフィガイド下LASIK)
Section titled “TG-LASIK(トポグラフィガイド下LASIK)”TG-LASIKは角膜トポグラフィデータに基づくカスタム切削により高次収差を低減する術式である。Rushらの前向き研究ではPhorcides解析を用いたTG-LASIKにおいて、PROWL質問票による全体的視覚満足度指数が術前4.07から術後5.00(最高値)に改善し、全患者が最高満足度を報告した5)。夜間視力・グレア・ハロー・ドライアイ症状のすべてで術後の有意な改善が認められた5)。
- ドライアイ: 人工涙液点眼(頻回)、3%ジクアホソルナトリウム点眼液1日6回、レバミピド点眼
- DLK: ステロイド点眼(早期から高頻度点眼)。grade 1〜2は点眼のみで多くが改善
水晶体系手術
Section titled “水晶体系手術”SMILE(KLEx)の位置づけ
Section titled “SMILE(KLEx)の位置づけ”SMILE(KLEx: keratorefractive lenticule extraction)はフラップを作製しないため、フラップ関連合併症(フラップ皺・上皮迷入・フリーキャップ)を回避できる2)。KLExではキャップが前方ボーマン膜側の構造を温存し、生体力学的強度を保持するため、拡張症リスクがLASIKより低いとされる2)。最小RST 220μm・総未切断実質厚300μmを保持する計画プロトコルが報告されている2)。
条件を満たせば増強手術(Enhancement)やPRKによる追加矯正が可能です。ただし、①術後6か月以上の屈折安定、②残存角膜厚の十分な確保(最低250μm)、③拡張症の進行がないこと、④拡張症リスク指標(BAD-D・PTA等)が許容範囲内であること、の全条件を満たすことが必要です。フラップリフトによる増強手術では上皮迷入が32%と高頻度に報告されており、経験豊富な術者による慎重な管理が求められます。
6. 病態生理学・詳細な発症機序
Section titled “6. 病態生理学・詳細な発症機序”エキシマレーザーによる角膜切削と過矯正
Section titled “エキシマレーザーによる角膜切削と過矯正”エキシマレーザーは193nmの紫外線パルスで角膜実質を蒸散し、切除深はムネリン公式 t = S²D/3 で推定される。過矯正は切除量が目標値を超えた場合、または角膜創傷治癒過程で切削効果が増大した場合に生じる。結果として角膜前面の過度平坦化が起こり、近視性屈折力が低下して遠視化する。
フラップ作製と角膜バイオメカニクス
Section titled “フラップ作製と角膜バイオメカニクス”LASIKのフラップ作製により、角膜の層板構造が切断される。これにより角膜の生体力学的強度が変化し、術後の角膜前方膨隆(拡張症)のリスクが生じる。フェムトセカンドレーザーによるフラップ(100〜120μm)は機械式マイクロケラトーム(平均120μm、ばらつきあり)より均一で薄く、RSB確保に有利である。
PRK vs LASIKのバイオメカニクス
Section titled “PRK vs LASIKのバイオメカニクス”PRKでは角膜フラップを作製せず、残余実質厚がLASIKより厚くなる。このため生体力学的に優位であり、拡張症リスクが低い。ただしボーマン膜が切除されるため術後角膜混濁(haze)のリスクがある。MMCの予防的使用が角膜混濁を抑制する。
KLEx(SMILE)のバイオメカニクス的優位性
Section titled “KLEx(SMILE)のバイオメカニクス的優位性”KLExではキャップが前方構造(ボーマン膜側)を温存する。前面の層板が連続しているため、角膜の圧力耐性がLASIKより高い。角膜剛性が低い患者ではKLEx後の残余屈折誤差リスクが2〜3倍高いことが報告されており2)、術前のバイオメカニクス評価が手術計画の精度向上に寄与する。
上皮リモデリングと診断への影響
Section titled “上皮リモデリングと診断への影響”角膜拡張症では実質の突出部で上皮が菲薄化し、周囲に上皮ドーナツパターンを形成する。この上皮リモデリングにより、トポグラフィのみでは拡張症の程度が過小評価される可能性がある。上皮厚マッピング(AS-OCT)を追加することで、拡張症とCLワーページの鑑別精度が向上する。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”AI画像解析による拡張症検出
Section titled “AI画像解析による拡張症検出”機械学習アルゴリズムを用いたトポグラフィ・トモグラフィ解析により、拡張症の検出精度が向上しつつある。正常角膜・疑わしい不整角膜・円錐角膜を識別する精度において、AIが角膜専門医に迫る結果も報告されている。
角膜バイオメカニクスの臨床応用
Section titled “角膜バイオメカニクスの臨床応用”角膜剛性が低い患者ではKLEx後の残余屈折誤差リスクが2〜3倍高い2)。バイオメカニクス指標をトポグラフィパラメータと組み合わせることで、KLExの予測精度が25%以上向上したとの報告がある2)。Corvis STやOcular Response Analyzerを用いた術前評価が手術計画の個別化に活用されつつある。
ノモグラム調整の個別化
Section titled “ノモグラム調整の個別化”ノモグラム調整はレーザー手術の精度と予測可能性に直結する。術前等価球面度数が最も重要な因子であり、年齢・眼左右差・角膜曲率・角膜径・角膜生体力学特性も関連する2)。多変量回帰分析やAIによる個別化調整の研究が進んでいる。
角膜デンシトメトリの応用
Section titled “角膜デンシトメトリの応用”Scheimpflugカメラによる角膜デンシトメトリは角膜透明性の客観的測定法である4)。Balpardaらの前向き研究(110眼)では、10mm以下の領域で優れた再現性を示し、1.0 GSU以上の変化が真の透明性変化と判定できることが示された4)。PRK後の角膜ヘイズの定量評価に有用となる可能性がある。
8. 参考文献
Section titled “8. 参考文献”- 日本眼科学会屈折矯正委員会. 屈折矯正手術のガイドライン(第8版). 日眼会誌. 2024;128(2):135-138.
- Ang M, Gatinel D, Reinstein DZ, et al. Evidence-based guidelines for keratorefractive lenticule extraction. Ophthalmology. 2025;132(4):404-418.
- American Academy of Ophthalmology Corneal Ectasia PPP Panel. Corneal Ectasia Preferred Practice Pattern. Ophthalmology. 2024.
- Balparda K, MesaMesa S, MayaNaranjo MI, et al. Determination of the repeatability of corneal densitometry as measured with a Scheimpflug camera device in refractive surgery candidates. Indian J Ophthalmol. 2023;71:63-68.
- Rush SW, Pickett CJ, Wilson BJ, Rush RB. Topography-guided LASIK: a prospective study evaluating patient-reported outcomes. Clin Ophthalmol. 2023;17:2815-2824.
- Li X, Gu Y. Unusual visual impairment after enhancement refractive surgery. J Surg Case Rep. 2024;2:rjae074.
- Santhiago MR, Smadja D, Gomes BF, et al. Association between the percent tissue altered and post-laser in situ keratomileusis ectasia in eyes with normal preoperative topography. Am J Ophthalmol. 2014;158(1):87-95.
