
眼腫瘍に対する放射線治療(Radiation Therapy for Ocular Tumors)
1. 眼腫瘍に用いられる放射線治療とは
Section titled “1. 眼腫瘍に用いられる放射線治療とは”放射線治療(放射線療法)は、高エネルギーの電磁波または粒子線を腫瘍に照射してDNAを損傷させ、腫瘍細胞の増殖を抑制・壊死させる治療法である。眼腫瘍領域では、眼球や視機能を温存しながら腫瘍を局所制御する手段として、外科切除・化学療法と組み合わせて広く用いられる。
眼腫瘍に対する放射線治療の意義は以下の3点にある。
- 眼球温存:外科切除(眼窩内容除去術・眼球摘出)を回避しつつ腫瘍を制御できる。
- 局所制御:リンパ腫など放射線感受性の高い腫瘍では単独で根治が期待できる。
- 補助療法:化学療法・手術後の残存腫瘍や再発抑制に使用される。
放射線治療は腫瘍の種類・大きさ・局在・周囲正常組織への影響に応じて治療法を選択する。主な照射法は「外照射(EBRT)」「定位放射線治療」「陽子線治療」「重粒子線(炭素線)治療」「プラーク療法(小線源治療)」の5種類である。
主な照射法の概要
Section titled “主な照射法の概要”- 外照射(EBRT):X線・電子線を用いた従来型の照射。眼窩リンパ腫・PIOL・転移性眼腫瘍などに広く使用される。
- 定位放射線治療:ガンマナイフ・サイバーナイフ・リニアックにより腫瘍に集中して照射する。視神経鞘髄膜腫など精密な照射が必要な疾患に用いられる。
- 陽子線治療:陽子線のブラッグピーク特性を利用して腫瘍への線量集中性を高め、周囲正常組織への影響を最小化する。ぶどう膜悪性黒色腫に対しては局所制御率90%以上、眼球温存率約80%(10年)と報告されている[1,2]。2016年4月から眼窩横紋筋肉腫に対して保険適用となった。
- 重粒子線(炭素線)治療:陽子線よりさらに高い生物学的効果を持つ炭素線を使用する。涙腺腺様囊胞癌・ぶどう膜黒色腫など難治性腫瘍に有望であり、眼窩外進展を伴う涙腺癌に対する5年眼球温存率は86%と報告されている[5]。本治療では血管新生緑内障の合併が比較的多い。
- プラーク療法(小線源治療):放射性同位元素を封入したプラーク(アプリケーター)を腫瘍対応強膜面に縫着し、腫瘍に直接照射する。局所照射が可能で眼球温存率が高い。
外照射(EBRT)・定位放射線治療(ガンマナイフ・サイバーナイフ・リニアック)・陽子線治療・重粒子線(炭素線)治療・プラーク療法(小線源治療)の5種類がある。疾患の種類・腫瘍サイズ・局在によって適切な照射法が選択される。
2. 疾患別の照射量と適応
Section titled “2. 疾患別の照射量と適応”眼腫瘍の種類によって推奨される照射量・照射法が異なる。以下に主要疾患の放射線治療の概要を示す。
疾患別の照射量と使用される照射法の対応は以下の通りである。
| 疾患 | 照射量(目安) | 主な照射法 |
|---|---|---|
| 眼窩低悪性度リンパ腫 | 30 Gy | 外照射(EBRT) |
| 眼窩中等度以上悪性度リンパ腫 | 40 Gy | 外照射(EBRT) |
| 眼窩未分化癌(極量) | 70 Gy | 外照射(EBRT) |
| 眼内リンパ腫(PIOL) | 30 Gy | 外照射(EBRT) |
| 転移性ぶどう膜腫瘍 | 40〜50 Gy | 外照射(EBRT) |
| 網膜芽細胞腫 | 40〜46 Gy | 外照射(X線分割) |
| 視神経鞘髄膜腫 | 施設依存 | 定位放射線治療 |
| 眼窩横紋筋肉腫 | 40〜50 Gy | 陽子線治療(保険適用) |
| 涙腺腺様囊胞癌 | 施設依存 | 重粒子線治療 |
眼窩リンパ腫
Section titled “眼窩リンパ腫”悪性リンパ腫は放射線感受性が高いため、眼窩部に限局した悪性リンパ腫に対して外照射が行われる。低悪性度のリンパ腫には30Gy程度、中等度以上の悪性度のリンパ腫には40Gy程度照射する。照射量が30Gyを超えると放射線白内障・網膜症・視神経症などの合併症が生じる危険性が増す。眼窩未分化癌などに対しては、合併症の発症を承知したうえで極量とされる70Gy程度を照射することもある。
眼内リンパ腫(PIOL)
Section titled “眼内リンパ腫(PIOL)”原発性眼内リンパ腫(PIOL)の眼局所病変に対しては、総量30グレイ程度の放射線照射が有効である。全身病変には化学療法を組み合わせる。
転移性ぶどう膜腫瘍
Section titled “転移性ぶどう膜腫瘍”眼部への転移腫瘍に対しては、40〜50グレイの照射が行われる。症状緩和(姑息的照射)として用いる場合が多い。
網膜芽細胞腫
Section titled “網膜芽細胞腫”40〜46グレイのX線を分割照射する方法が用いられる。ただし現在では化学療法・局所療法(プラーク療法・レーザー治療・凍結療法)の進歩により、外照射は他治療で制御できない場合に限り行われる。小児への外照射は二次がんリスクおよび眼窩発育障害を来たすため、適応を慎重に判断する。
視神経鞘髄膜腫
Section titled “視神経鞘髄膜腫”定位放射線治療(リニアック・ガンマナイフ・サイバーナイフ)により視機能の温存と腫瘍増大の抑制が可能と報告されている。外科的に完全切除すると視神経を犠牲にする可能性があるため、放射線治療が主要な治療手段となる。
眼窩横紋筋肉腫
Section titled “眼窩横紋筋肉腫”化学療法(VAC療法)と放射線療法の組み合わせが標準治療である。2016年4月から陽子線治療が保険適用となり、周囲正常組織への影響を最小限にした照射が可能になった。病期(IRSグループ)II〜IVに対しては化学療法と放射線療法を組み合わせ、4,000〜5,000cGy(40〜50Gy)を照射する。陽子線治療では水晶体や眼窩骨などの周囲構造への線量を光子線より大幅に低減でき、小児症例において優れた腫瘍制御と長期合併症の低減が報告されている[6]。
涙腺腺様囊胞癌
Section titled “涙腺腺様囊胞癌”手術不可能な腺様囊胞癌に対しては重粒子線治療が行われている。眼瞼・眼球・眼窩を温存しながら腫瘍を制圧できる有望な治療法であり、眼窩外進展を伴う症例においても5年局所制御率62%・全生存率65%と報告されている[5]。
3. プラーク療法(小線源治療)
Section titled “3. プラーク療法(小線源治療)”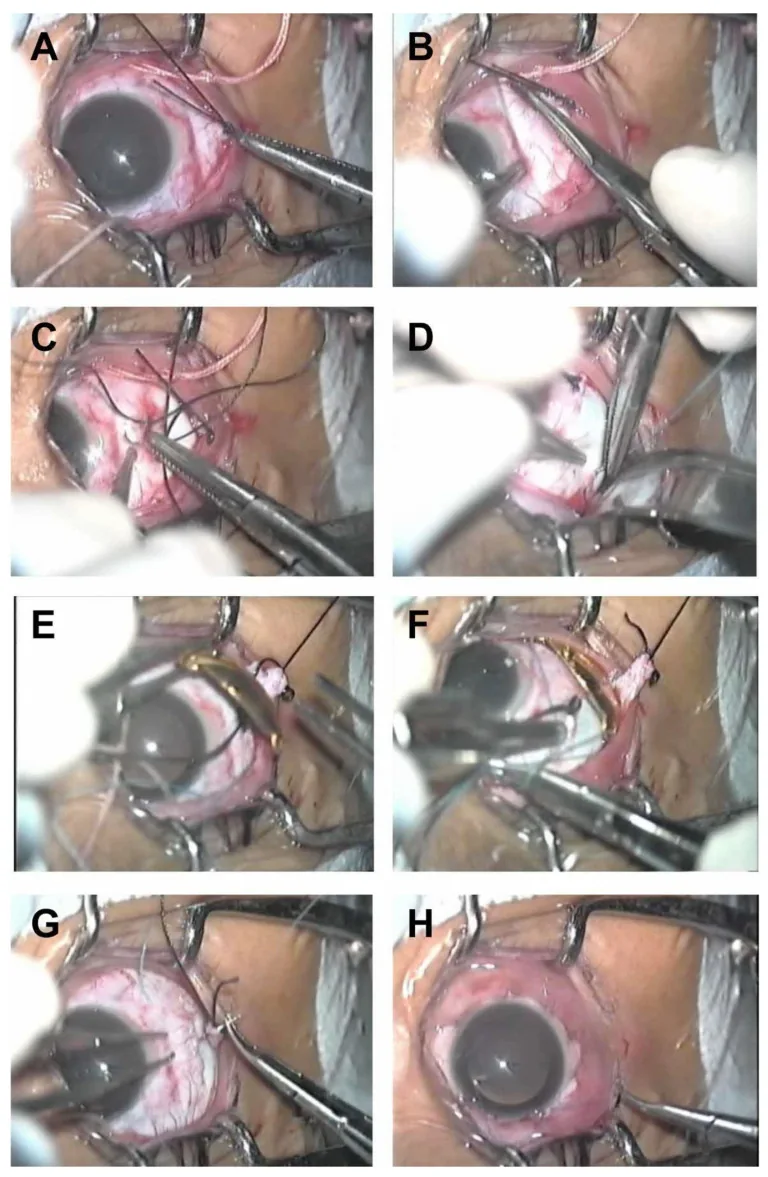
プラーク療法は、放射性同位元素を封入したプラーク(ディスク状のアプリケーター)を腫瘍に対応する強膜面に一時的に縫着し、腫瘍内部に直接放射線を照射する局所治療法である。ぶどう膜悪性黒色腫・網膜芽細胞腫(再発・残存例)に対する主要な眼球温存治療として位置づけられる。
使用される放射線源
Section titled “使用される放射線源”使用される放射線源は地域によって異なる。
- ¹⁰⁶Ru(ルテニウム、β線源):日本および欧州で主に使用される。β線(電子線)を放出し、腫瘍に選択的に照射される。
- ¹²⁵I(ヨウ素、γ線源):北米で主に使用される。低エネルギーγ線を放出する。
¹⁰⁶Ruプラーク療法の対象となる腫瘍の条件は以下の通りである。
- 腫瘍厚:5mm以下
- 腫瘍横径:15mm以下
- 腫瘍局在:視神経乳頭から離れた限局腫瘍
腫瘍が視神経乳頭や黄斑部に接している場合や、腫瘍が大きい場合は適応が困難となる。
局所制御率と治療の特徴
Section titled “局所制御率と治療の特徴”80〜90%の局所制御が可能である。COMS(Collaborative Ocular Melanoma Study)試験では中型脈絡膜悪性黒色腫に対する¹²⁵Iプラーク小線源治療と眼球摘出の生存率に有意差がないことが報告されており、眼球温存治療として確立されている[3]。¹⁰⁶Ruプラーク療法による長期成績では、5年・7年・9年の生存率がそれぞれ99%・97%・85%、局所再発率1%程度と良好である[4]。プラーク療法は腫瘍に対応する強膜面のみへのピンポイント照射であり、外照射と比べて周囲正常組織への影響が少ない点が利点である。
手術的な操作(プラーク縫着・抜去)に専門技術を要し、また放射線管理のための特殊治療室が必要であるため、実施できる施設が限定される。
プラーク療法は放射性プラークを腫瘍対応の強膜面に直接縫着する局所照射法であり、腫瘍への線量集中性が高く周囲正常組織への影響が少ない。外照射は腫瘍部位全体に体外から照射するため、より広範囲の腫瘍や多病巣への対応が可能だが、眼窩前部・水晶体・視神経など周囲構造への線量が多くなる。適応は腫瘍の大きさ・局在・種類によって選択される。
4. 放射線治療の副作用と管理
Section titled “4. 放射線治療の副作用と管理”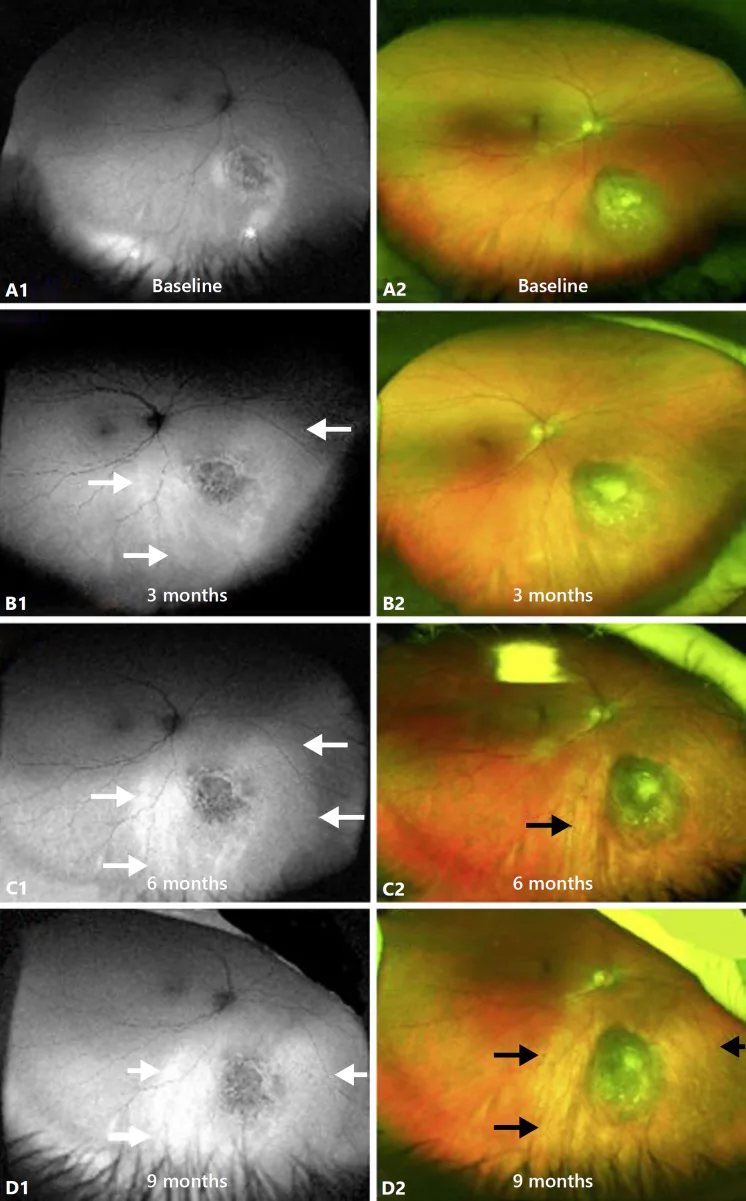
眼腫瘍への放射線治療では、腫瘍への治療効果と引き換えに周囲正常組織への影響(副作用)が生じる。副作用は照射量・照射範囲・治療法の種類によって異なる。
主な眼科的副作用
Section titled “主な眼科的副作用”- 放射線白内障:照射量が30Gyを超えると発症リスクが増大する。水晶体は放射線感受性が高く、後嚢下白内障として出現することが多い。超音波乳化吸引術による白内障手術が適応となる場合がある。
- 放射線網膜症:毛細血管の閉塞・網膜虚血により、滲出性変化・新生血管・黄斑浮腫が生じる。小線源治療後に20〜53%の頻度で発症すると報告されている[7]。抗VEGF療法やレーザー光凝固が治療に用いられ、予防的ベバシズマブ投与により黄斑浮腫の発症が低減できる可能性が示されている[7]。
- 放射線視神経症:視神経への照射によって視神経血流が障害され、視力低下・視野欠損が生じる。不可逆的な視力障害を来たす場合がある。
- ドライアイ:涙腺・結膜杯細胞への照射によって生じる。人工涙液・抗炎症点眼で管理する。
- 血管新生緑内障:重粒子線治療後に比較的多く認められる合併症であり、眼圧管理が必要となる。
- 眼窩発育不全:特に小児への照射では、眼窩骨の発育が阻害され顔面非対称が生じうる。陽子線治療・重粒子線治療は通常のX線外照射と比べて周囲正常組織への線量を低減できる。
二次がんリスク(小児)
Section titled “二次がんリスク(小児)”小児(特に網膜芽細胞腫)への外照射は、照射野内での二次がん(骨肉腫・軟部肉腫など)発生リスクを高める。遺伝性網膜芽細胞腫(RB1両アレル変異)では二次がんリスクがさらに高く、外照射の適応は慎重に判断される。陽子線治療は周囲正常組織への線量低減により二次がんリスクの軽減が期待される。
フォローアップの要点
Section titled “フォローアップの要点”- 放射線治療後は少なくとも3〜6ヶ月ごとの眼科的定期検査を継続する。
- 放射線網膜症・白内障・視神経症の早期発見のため、眼底検査・光干渉断層計(OCT)・視野検査を定期的に施行する。
- 血管新生緑内障のリスクがある疾患(重粒子線治療後など)では、眼圧測定と隅角鏡検査を追加する。
5. 治療施設と保険適用
Section titled “5. 治療施設と保険適用”放射線治療の種類によって実施可能な施設数と保険適用の状況が異なる。
2016年4月より眼窩横紋筋肉腫に対する陽子線治療が保険適用となった。陽子線治療施設は全国に限定されており、近隣施設への紹介が必要となる場合がある。
重粒子線治療
Section titled “重粒子線治療”涙腺腺様囊胞癌をはじめとする難治性眼腫瘍への重粒子線治療が国内施設で実施されている。適応疾患の拡大と施設数の増加が進んでいる。
プラーク療法
Section titled “プラーク療法”特殊治療室と専門的な技術を要するため、実施施設が限定される。プラーク療法を実施している眼科専門施設への紹介が必要となる。
外照射・定位放射線治療
Section titled “外照射・定位放射線治療”リニアック(直線加速器)による外照射は全国の放射線治療施設で実施可能である。定位放射線治療(ガンマナイフ・サイバーナイフ)は一部の施設で実施されており、眼腫瘍への適応については眼科と放射線科の連携が必要である。
6. 病態生理学:放射線の作用機序と線量設定の根拠
Section titled “6. 病態生理学:放射線の作用機序と線量設定の根拠”放射線が腫瘍細胞に与える影響
Section titled “放射線が腫瘍細胞に与える影響”放射線(X線・γ線・粒子線)は細胞内のDNA二本鎖切断を引き起こし、細胞分裂を停止させる。腫瘍細胞は正常細胞に比べてDNA修復能が低いため、放射線に対してより感受性が高い(相対的な感受性の差)。この原理を利用して腫瘍選択的な殺傷を図るのが放射線治療の基本概念である。
線量設定の考え方
Section titled “線量設定の考え方”照射量(グレイ, Gy)の設定は、腫瘍の放射線感受性と周囲正常組織の耐容線量のバランスによって決定される。
- 悪性リンパ腫:放射線感受性が非常に高く、30〜40Gyの比較的低い線量で根治が期待できる。
- 腺癌・肉腫:感受性が中等度以下で、40〜70Gyの高線量が必要となる。
- 視神経・網膜:放射線耐容線量が低く(水晶体では2〜4Gy程度で白内障リスクあり)、照射範囲の最適化が不可欠である。
分割照射の意義
Section titled “分割照射の意義”通常、外照射は1回1.8〜2Gyを週5回・数週間にわたって分割照射(フラクショネーション)する。分割照射により、正常細胞が照射間隔にDNA修復を行う機会を得る一方、腫瘍細胞は修復が不完全なまま次の照射を受けるため、治療効果と副作用のバランスが最適化される。
粒子線治療の物理学的特性
Section titled “粒子線治療の物理学的特性”陽子線・重粒子線(炭素線)は、照射軌道の末端に「ブラッグピーク」と呼ばれる線量集中域を形成する。X線が組織を通過しながら連続的にエネルギーを放出するのに対し、粒子線は特定の深さで急峻にエネルギーを放出したのちほぼゼロとなる。この特性により、腫瘍深部への高線量照射と腫瘍後方正常組織への線量低減を同時に達成できる。炭素線(重粒子線)はさらに高い生物学的効果比(RBE)を持ち、放射線抵抗性腫瘍(腺様囊胞癌等)に対してもX線より高い殺傷効果が期待される。
7. 参考文献
Section titled “7. 参考文献”- Mishra KK, Daftari IK. Proton therapy for the management of uveal melanoma and other ocular tumors. Chin Clin Oncol. 2016;5(4):50. PMID: 27558251. doi:10.21037/cco.2016.07.06
- Chan AW, Lin H, Yacoub I, et al. Proton Therapy in Uveal Melanoma. Cancers (Basel). 2024;16(20):3497. PMCID: PMC11506608.
- Diener-West M, Earle JD, Fine SL, et al; Collaborative Ocular Melanoma Study Group. The COMS randomized trial of iodine 125 brachytherapy for choroidal melanoma, III: initial mortality findings. COMS Report No. 18. Arch Ophthalmol. 2001;119(7):969-982. PMID: 11448319.
- Cennamo G, Montorio D, D’Andrea L, et al. Long-Term Outcomes in Uveal Melanoma After Ruthenium-106 Brachytherapy. Front Oncol. 2022;11:754108. doi:10.3389/fonc.2021.754108
- Hayashi K, Koto M, Ikawa H, Ogawa K, Kamada T. Efficacy and safety of carbon-ion radiotherapy for lacrimal gland carcinomas with extraorbital extension: a retrospective cohort study. Oncotarget. 2018;9(16):12932-12940. PMID: 29560121.
- Yock T, Schneider R, Friedmann A, Adams J, Fullerton B, Tarbell N. Proton radiotherapy for orbital rhabdomyosarcoma: clinical outcome and a dosimetric comparison with photons. Int J Radiat Oncol Biol Phys. 2005;63(4):1161-1168. PMID: 15950401.
- Mularska W, Chicheł A, Rospond-Kubiak I. Radiation retinopathy following episcleral brachytherapy for intraocular tumors: Current treatment options. J Contemp Brachytherapy. 2023;15(5):372-382. PMID: 38026080. PMCID: PMC10669920.
