テルソン症候群 はくも膜下出血(SAH)・硬膜下出血・脳内出血後に眼内出血(硝子体出血 ・網膜 前出血)を発症した状態である。急性SAH症例の約20%、くも膜下出血症例全体の3〜20%に発症する。SAH発症2〜3日後、多くは2週間以内に眼内出血が出現する。
発症初期は内境界膜 下血腫(網膜 前出血)をきたし、その後内境界膜 の破綻により硝子体出血 へ進展する。
硝子体出血 は自然吸収されることがあるが、黄斑前膜 ・網膜 剝離を合併した場合は不可逆的な視機能障害を生じる。両眼発症・若年者・高度硝子体出血 ・Bモード超音波での網膜 剝離疑い例には積極的に硝子体手術 を選択する。
SAH治療(脳動脈瘤クリッピング術・コイル塞栓術)の成否が生命予後を左右するため、脳外科と眼科の連携が不可欠である。
若年者では増殖硝子体網膜症 を発症しやすく、年齢と発症からの期間に細心の注意を要する。
テルソン症候群 は、くも膜下出血(subarachnoid hemorrhage: SAH)・硬膜下出血・脳内出血後に眼内出血を発症した状態を指す。眼内出血の形態としては硝子体出血 と内境界膜 下出血を生じる場合が多く、視神経乳頭 周囲や黄斑部 網膜 の種々の層(網膜 前・網膜 内・網膜 下)にも出血する。1)
1900年、フランスの眼科医Albert Tersonがくも膜下出血に伴う硝子体出血 を初めて報告した。以後、頭蓋内出血に伴う眼内出血はTerson症候群として知られるようになった。
外傷性脳損傷(traumatic brain injury: TBI)後の発症率は約3.1%と報告されており、SAH(19.3%)・脳内出血(9.1%)と比較すると低いが、TBI患者数が多いため絶対数では無視できない。1)
発生頻度:くも膜下出血症例の3〜20%程度。TBIでは約3.1%。1)
急性SAHでの発症率:約20%
発生時期:頭蓋内出血後2〜3日、多くは2週間以内
片眼性または両眼性のいずれも起こりうる
発症初期は網膜 前出血(内境界膜 下血腫)をきたすことが多い。その後、内境界膜 の物理的破綻を契機として硝子体出血 へと進行する。出血量・出血部位は患者によって異なり、軽微な網膜 前出血のみにとどまる場合から、眼底透見が不能となる大量の硝子体出血 まで幅がある。
Q
くも膜下出血の患者は全員テルソン症候群を発症するのですか?
A
全員ではない。くも膜下出血症例の3〜20%、急性SAHの約20%に発症するとされる。多くのSAH患者では眼内出血を起こさないが、頭蓋内圧の急激な上昇が大きい例や特定の解剖学的経路が関与する場合に発症しやすいと考えられている。SAH後に視力 低下や飛蚊症 が出現した場合は速やかに眼科を受診することが重要である。
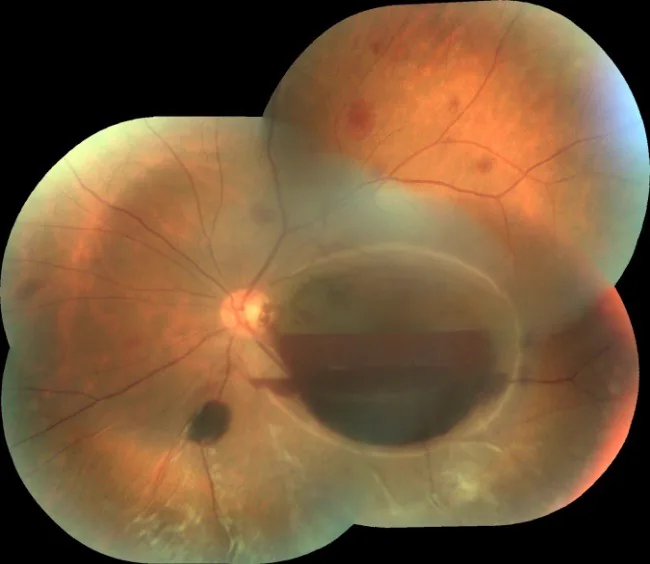
テルソン症候群の眼底像:黄斑部ドーム状網膜前血腫(二層性出血) Moraru A, et al. Terson’s Syndrome – case report. Rom J Ophthalmol. 2017;61(1):44–48. Figure 2. PM
CI D: PMC5710052. License: CC BY.
左眼の広角眼底写真で、黄斑部 中心に大型のドーム状網膜 前血腫(内境界膜 下血腫)が認められ、血液の重力沈降による水平な二層性出血レベル(上層:液性血液、下層:凝固血)が明瞭に確認できる。本文「2. 主な症状と臨床所見」の項で扱う黄斑部 網膜 前血腫(内境界膜 下血腫)に対応する。
テルソン症候群 の自覚症状は、頭蓋内出血後(多くはSAH発症後2〜3日以内)に出現する視力 低下が主体である。硝子体出血 が大量の場合は急激かつ高度の視力 低下をきたし、眼底透見が不能となる。飛蚊症 を訴えることもある。頭蓋内出血の症状(激しい頭痛・意識障害・嘔気)が前景に立つため、眼症状が見落とされやすい点に注意が必要である。
片眼性に発症することもあるが、両眼性に発症することもある。意識障害を伴うSAH患者では視力 低下の訴えが得られない場合も多く、眼科的スクリーニングが重要となる。
初期所見
内境界膜 下血腫(網膜 前出血)視神経乳頭 周囲や黄斑部 に認める。血腫は境界明瞭な暗赤色の隆起として観察される。
少量の硝子体出血 :眼底透見は可能な程度の出血量であることもある。自然吸収が期待できる段階である。
網膜 内・網膜 下出血視神経乳頭 周囲から黄斑部 にかけての各層に出血を認めることがある。
進行期所見
大量硝子体出血 :内境界膜 が破綻すると硝子体 腔への出血が急増し、眼底透見が不能となる。視力 は光覚弁以下まで低下することがある。
黄斑前膜 黄斑前膜 が形成される。視力 予後を大きく左右する合併症である。
網膜 剝離・増殖硝子体網膜症 硝子体出血 の遷延・器質化から増殖組織が形成され、牽引性網膜 剝離へ進展することがある。特に若年者でリスクが高い。
硝子体出血 が自然吸収された後も、黄斑前膜 の形成に注意した経過観察が必要である。自然吸収後に視力 が改善せず、OCT検査 で黄斑前膜 や黄斑浮腫 が確認された場合は手術を検討する。
Q
硝子体出血は自然に治るのですか?
A
軽度〜中等度の硝子体出血 であれば自然吸収が期待できる場合がある。ただし吸収には数週間〜数か月を要することがあり、その間に黄斑前膜 や増殖硝子体網膜症 を発症するリスクがある。特に若年者では増殖性変化が起こりやすいため、経過観察の期間と頻度に十分注意する。高度の硝子体出血 ・両眼性・Bモード超音波での網膜 剝離疑い例では、積極的に硝子体手術 を選択することが推奨される。
テルソン症候群 の原因となる頭蓋内出血は以下のとおりである。
くも膜下出血(最多) :脳動脈瘤の破裂が主な原因。急激な頭蓋内圧上昇が眼内出血を引き起こす。外傷性脳損傷(TBI) :交通外傷・転倒・転落・打撲による頭部外傷で発症する。TBI患者の約3.1%にテルソン症候群 が合併すると報告されている。1,2) 硬膜下出血 :頭部外傷後に生じる硬膜下血腫に伴う場合がある。乳幼児では虐待による頭部外傷(abusive head trauma: AHT、いわゆる揺さぶられっ子症候群 )の重要な所見として網膜 出血が知られており、テルソン症候群 との鑑別が問題となる。3,4) 脳内出血 :高血圧性脳出血などに続発する場合がある。
SAH重症度 :Hunt & Hess分類の高グレード(重症)例では頭蓋内圧の急激な上昇が大きく、眼内出血が起こりやすい。若年者 :若年者では増殖硝子体網膜症 を発症しやすいため、硝子体手術 を積極的に検討する必要がある。発症から眼科受診までの期間 :発症から時間が経過するほど増殖性変化のリスクが高まる。全身状態不良で眼科受診が遅れる例では特に注意する。
テルソン症候群 の診断は以下の手順で行う。
頭蓋内出血の既往確認 :SAH・硬膜下出血・脳内出血の診断を脳神経外科と共有する。細隙灯顕微鏡検査 眼底検査 散瞳 下での眼底検査 を行う。硝子体出血 が高度の場合は眼底透見が困難となる。Bモード超音波検査 :眼底透見が不能な場合に必須。網膜 剝離・増殖性変化・後部硝子体 剝離の有無を評価する。経過観察中も頻回に施行し、増殖性変化の出現を見逃さない。OCT検査 内境界膜 下血腫・黄斑前膜 ・網膜 層構造の評価に有用である。
検査法 主な評価項目 特記事項 細隙灯顕微鏡 前眼部・硝子体混濁 散瞳 下で施行眼底検査 網膜 前出血・硝子体出血 高度混濁では不可能 Bモード超音波 網膜 剝離・増殖変化眼底透見不能例で必須。頻回施行 OCT 内境界膜 下血腫・黄斑前膜 透光体清明な場合に有用 蛍光眼底造影 血管病変・虚血領域 透光体清明な場合に実施
Valsalva網膜 症 :努責(重量挙げ・嘔吐・咳嗽など)後に生じる網膜 前出血・硝子体出血 。頭蓋内出血の既往がなく、鑑別は比較的容易。糖尿病網膜症 による硝子体出血 新生血管 ・硬性白斑等)が鑑別の鍵となる。網膜静脈閉塞症 (CRVO /BRVO )後部硝子体 剝離に伴う硝子体出血 :高齢者に多く、頭蓋内出血の既往を欠く。乳幼児の虐待による頭部外傷(AHT、揺さぶられっ子症候群 ) :両眼性の多層性網膜 出血・網膜 分離・網膜 皺襞を呈し、明確な事故歴のない硬膜下血腫を伴う場合は虐待を強く疑う。テルソン症候群 との鑑別には、画像検査・骨格検査・小児科・社会福祉と連携した系統的評価が必須である。3,4)
増殖性変化が発生している場合には、網膜 剝離・網膜 下増殖・黄斑前膜 の存在を念頭において評価する。発症から時間が経過している例や全身状態不良で受診が遅れた例では増殖性変化のリスクが高まるため、Bモード超音波での頻回な経過観察が特に重要である。
Q
SAH後に眼科検査は必ずしも必要ですか?
A
テルソン症候群 の発見・管理のために、SAH患者への眼科的スクリーニングは強く推奨される。意識障害を伴う重症例でも眼底検査 は可能であり、硝子体出血 を早期に発見することで適切な治療介入のタイミングを逃さずに済む。特に眼底透見が不能な場合はBモード超音波検査で網膜 剝離の有無を確認する必要がある。脳外科医と眼科医が連携した対応体制が求められる。
テルソン症候群 の治療は、硝子体出血 の重症度・発症形態(片眼性/両眼性)・患者年齢・経過期間・合併症の有無によって決定する。大きく「経過観察」と「硝子体手術 」の二択となる。
状態 治療方針 軽度〜中等度の片眼性硝子体出血 (自然吸収が期待できる) 経過観察(Bモード超音波での頻回観察) 両眼発症 積極的に硝子体手術 を選択(視機能の早期改善が必要) 若年者 積極的に硝子体手術 を選択(増殖硝子体網膜症 のリスクが高い) 高度の硝子体出血 硝子体手術 (自然吸収が困難)Bモード超音波で網膜 剝離を疑う場合 硝子体手術 (放置で不可逆的視機能障害)出血遷延例(両眼性を含む) 硝子体手術
経過観察を選択した場合でも、Bモード超音波検査を頻回に施行して網膜 剝離・増殖性変化の出現に注意する。
硝子体手術 (経毛様体扁平部硝子体切除術 、pars plana vitrectomy: PPV )は25G または27G の小切開システムで施行される。手術の主な目的は硝子体出血 の除去であり、視機能の早期回復と増殖硝子体網膜症 の予防に寄与する。TBIに続発するテルソン症候群 に対する硝子体手術 の臨床成績は良好で、術後早期の視力 改善が多くの症例で得られると報告されている。2,5) 小児症例の検討でも硝子体 切除術により解剖学的・機能的に良好な転帰が得られている。6)
手術中の主要操作を以下に示す。
硝子体出血 の除去硝子体 を切除し、網膜 の視認性を回復する。内境界膜 (ILM )の処理黄斑前膜 を合併している場合は膜剝離を施行する。ILM 剝離の要否は術中の所見に基づいて判断する。網膜 剝離の対処網膜 剝離が確認された場合は、网膜復位術(空気・ガス・シリコンオイルタンポナーデ、必要に応じてレーザー光凝固 )を行う。
硝子体手術 後の視力 予後は、黄斑前膜 ・網膜 剝離・増殖硝子体網膜症 の有無に大きく左右される。出血のみで合併症がなければ良好な視力 回復が期待できる。
SAH自体の重篤性が生命予後を直接左右するため、脳動脈瘤のクリッピング術またはコイル塞栓術が最優先である。眼科治療はSAHの治療経過を考慮したうえで計画する。
若年者では経過観察期間中に増殖硝子体網膜症 が急速に進行する場合があるため、早期の手術介入を検討する。
黄斑前膜 が形成された後に手術を行っても、視力 回復が制限される場合がある。合併症形成前の早期手術が視力 予後に有利とされる。全身状態不良(重症SAH)で硝子体手術 が困難な場合は、Bモード超音波での厳重な経過観察を継続する。
Q
硝子体手術はいつ行うべきですか?
A
手術のタイミングは患者の全身状態・出血量・合併症の有無・年齢によって個別に判断する。両眼発症・若年者・高度硝子体出血 ・Bモード超音波での網膜 剝離疑い例は積極的な早期手術の適応とされている。一方、軽度の片眼性硝子体出血 で自然吸収が期待できる場合は経過観察を選択できる。ただし経過観察中も頻回のBモード超音波検査で増殖性変化を監視することが不可欠である。SAH自体の治療が最優先であり、眼科手術のタイミングは全身状態が安定してから脳外科と相談のうえ決定する。
テルソン症候群 の発症機序については複数の説が提唱されており、現時点でも議論が続いている。主に以下の3つの説が挙げられる。
くも膜下出血による急激な頭蓋内圧亢進が視神経 内の網膜 中心静脈を圧迫する。その結果、網膜 中心静脈圧が亢進・上昇し、網膜 の毛細血管や小静脈が破綻して硝子体出血 をきたすとする説である。この説は頭蓋内圧の急激な変動が眼内血管に伝達されるという機序を重視しており、SAH重症度(頭蓋内圧上昇の程度)とテルソン症候群 の発症頻度が相関するとされる知見とも一致する。
視神経 周囲のくも膜下腔に流入したくも膜下出血の血液が、解剖学的経路を通じて眼内に直接流入するとする説である。くも膜下腔と眼球内空間の解剖学的連続性が発症の基盤となる。この説は、内境界膜 下に血液が流入する様式を一定程度説明できる。
網膜 中心動静脈が視神経 内を走行する部分の周囲に間隙が存在し、この間隙の先端が視神経乳頭 周囲血管の周囲にまで伸びているとする説である。この経路を通じて、くも膜下腔の血液が内境界膜 下に流れ込み内境界膜 下血腫を形成する。その後、内境界膜 の物理的破綻によって硝子体出血 が生じるという機序である。この説は初期所見として内境界膜 下血腫(網膜 前出血)が観察されることをよく説明する。
また、以下の2つの説も示されている。
頭蓋内圧の急激な上昇に伴う網膜 中心静脈のうっ滞が網膜 出血を生じる説
くも膜下腔から視神経 鞘内に入った出血が網膜 中心静脈に沿って視神経乳頭 から眼内へ移動し、網膜 出血・硝子体出血 へ進展する説
[機序:くも膜下腔の血液が内境界膜下に流入/頭蓋内圧亢進による血管破綻]
現時点では単一の発症機序が確定されているわけではなく、症例によって関与する機序が異なる可能性がある。いずれの説も、SAHによる急激な頭蓋内変化が眼内出血の引き金になるという点で共通している。
若年者では硝子体 の液化・後部硝子体 剝離が進んでいないため、出血した血液が硝子体 内に留まりやすく、増殖刺激による線維血管膜の形成が促進されやすい。その結果、増殖硝子体網膜症 (proliferative vitreoretinopathy: PVR )を発症しやすく、牽引性網膜 剝離・裂孔原性網膜 剝離へと進展するリスクが高い。年齢と発症からの期間の両方に注意して経過観察の密度を決定することが重要である。
SAH患者へのルーチンの眼科スクリーニング(眼底検査 ・Bモード超音波検査)の実施プロトコルは施設によって異なり、統一された基準はまだ確立されていない。意識障害を伴う重症SAH患者への眼科スクリーニングをいつ・どのように行うかという点について、脳神経外科と眼科の連携体制の整備が今後の課題である。
テルソン症候群 に対する硝子体手術 の至適タイミングについて、早期介入(SAH発症後早期)と待機的手術(自然吸収を確認後)のどちらが視力 予後・合併症率において優れるかを検証した大規模比較研究は少ない。特に両眼発症例・若年者における早期手術の効果を明らかにするエビデンスの蓄積が求められている。
大量の硝子体出血 を伴わず内境界膜 下血腫のみを呈する症例に対して、Nd:YAGレーザーによる内境界膜 開窓(後嚢切開様アプローチ)で血腫を硝子体 腔へ解放する手技の報告がある。侵襲を最小限に抑えながら血腫の迅速な排出を図る方法として注目されているが、標準的治療として確立するためのさらなる検証が必要である。
光干渉断層計 (OCT )・OCT 血管造影(OCTA )を用いた内境界膜 下血腫の三次元的評価と、それに基づく視力 予後予測が研究されている。出血量・層別分布・黄斑 中心窩 の構造的変化を定量化することで、手術適応の判断精度を高める可能性がある。
SAH発症後の眼科的評価のタイミング・方法・頻度を定めた標準プロトコルを整備することで、テルソン症候群 の見落とし防止と視力 予後改善が期待される。救急・集中治療・脳外科・眼科が連携したチームアプローチの構築が今後の課題として認識されている。
Czorlich P, Skevas C, Knospe V, et al. Terson syndrome in subarachnoid hemorrhage, intracerebral hemorrhage, and traumatic brain injury. Neurosurg Rev . 2015;38(1):129-136. PMID: 25173620. 1)
Narayanan R, Taylor SC, Nayaka A, et al. Visual Outcomes after Vitrectomy for Terson Syndrome Secondary to Traumatic Brain Injury. Ophthalmology . 2017;124(1):118-122. PMID: 27817917. 2)
Togioka BM, Arnold MA, Bathurst MA, et al. Retinal hemorrhages and shaken baby syndrome: an evidence-based review. J Emerg Med . 2009;37(1):98-106. PMID: 19081701. 3)
Squier W. Retinodural haemorrhage of infancy, abusive head trauma, shaken baby syndrome: The continuing quest for evidence. Dev Med Child Neurol . 2024;66(3):290-297. PMID: 37353945. 4)
Citirik M, Tekin K, Teke MY. Terson syndrome with persistent vitreous hemorrhage following traumatic brain injury. Saudi J Ophthalmol . 2019;33(4):392-397. PMID: 31920451; PMCI D: PMC6950947. 5)
Sayman Muslubas I, Karacorlu M, Hocaoglu M, Ersoz MG, Arf S. Anatomical and functional outcomes following vitrectomy for dense vitreous hemorrhage related to Terson syndrome in children. Graefes Arch Clin Exp Ophthalmol . 2018;256(3):503-510. PMID: 29288413. 6)
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください