フルオレセイン(fluorescein)
吸収波長:494 nm(青色光)→ 蛍光521 nm(緑色)
染色対象:上皮細胞間の密着結合破綻部位(細胞間隙)
主用途:SPK検出・BUT測定・角膜潰瘍/びらん評価
刺激性:低い(最も使いやすい)
観察フィルター:コバルトブルー + ブルーフリー(バリア)フィルター

角膜・結膜生体染色検査(ocular surface vital staining)は、眼表面の角膜・結膜上皮の障害を色素によって可視化し、障害の分布・程度を定量化する基本的眼科検査である。
使用される主要色素は以下の3種である。
本検査の主な目的は以下の通りである。
ドライアイ診療ガイドライン(2016年版)では、涙液層破壊時間(BUT)の測定とフルオレセイン染色を組み合わせた評価がドライアイ診断の中核として推奨されている1)。2006年版では角結膜上皮障害がドライアイ診断に必須だったが、2016年版では上皮障害は必須要件ではなくなり、BUTの短縮と自覚症状に基づく診断に移行した。それでも生体染色は上皮障害の程度・パターンを客観的に記録する重要な評価手段として位置づけられている1)。
感染性角膜炎の初期評価においても、フルオレセイン染色は角膜上皮欠損の範囲と形状を把握するための標準的手技であり、感染性角膜炎診療ガイドライン(第3版)に準拠した診療に組み込まれている2)。
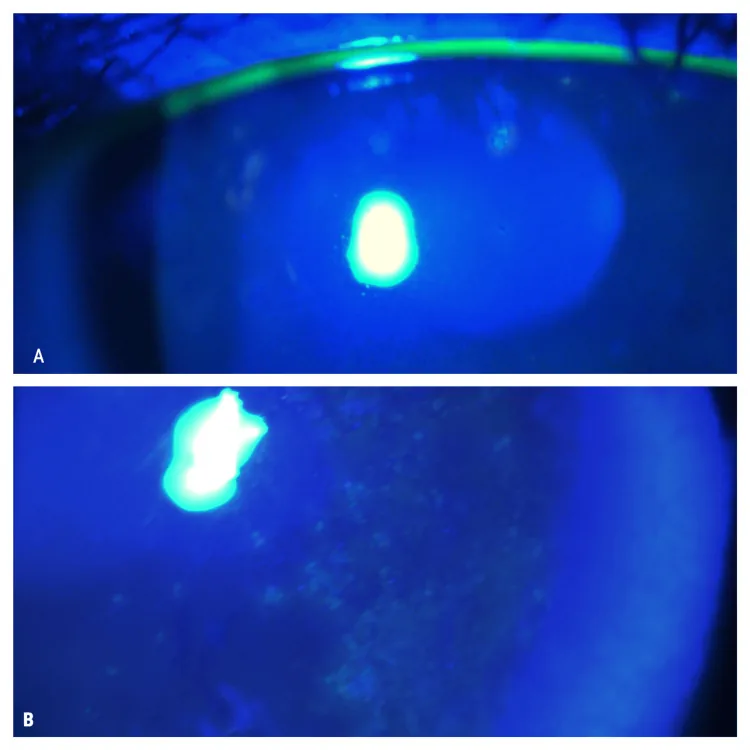
フルオレセインは生体染色色素として最も広く用いられている。入手しやすく、安全で刺激が少ないことから汎用される。フルオレセインは青色光(最大吸収波長494 nm)で励起すると緑色(521 nm)の蛍光を発する色素である。コバルトブルーのフィルターで励起するだけでも観察できるが、観察系にブルーフリーフィルターを入れると明瞭に病変を描出できる。
染色原理と観察ポイント:
染色手順(最小量染色法):
ローズベンガルはフルオレセインとは異なるメカニズムで眼表面を染色する。
染色特性:
van Bijsterveld スコアリング(ローズベンガル・リサミングリーン共用):
リサミングリーンはローズベンガルと類似した染色特性を持ちつつ、患者への刺激が少ない代替色素である。
染色特性:
フルオレセイン(fluorescein)
吸収波長:494 nm(青色光)→ 蛍光521 nm(緑色)
染色対象:上皮細胞間の密着結合破綻部位(細胞間隙)
主用途:SPK検出・BUT測定・角膜潰瘍/びらん評価
刺激性:低い(最も使いやすい)
観察フィルター:コバルトブルー + ブルーフリー(バリア)フィルター
ローズベンガル(rose bengal)
染色色:赤色
染色対象:死細胞・変性細胞・ムチン保護欠失部
主用途:Sjögren症候群診断(van Bijsterveld スコア)、ドライアイ評価
刺激性:強い(点眼時疼痛あり)
観察フィルター:白色光または赤色フィルター
リサミングリーン(lissamine green)
染色色:緑色
染色対象:死細胞・変性細胞(ローズベンガルと同様のメカニズム)
主用途:ローズベンガルの代替。ドライアイ・Sjögren症候群評価
刺激性:低い(ローズベンガルより患者負担が少ない)
観察フィルター:赤色フィルター(560 nm以上)で明瞭
| 特性 | フルオレセイン | ローズベンガル | リサミングリーン |
|---|---|---|---|
| 染色色 | 緑色蛍光 | 赤色 | 緑色 |
| 染色対象 | 細胞間隙(密着結合破綻部) | 死細胞・変性細胞・ムチン欠失部 | 死細胞・変性細胞 |
| 刺激性 | 低い | 高い(疼痛あり) | 低い |
| 観察フィルター | コバルトブルー + ブルーフリー | 白色光・赤色フィルター | 赤色フィルター(560 nm以上) |
| 主な用途 | SPK・BUT測定・角膜潰瘍 | Sjögren診断・ドライアイ | ローズベンガル代替 |
| 代表スコア | Oxford スコア・NEI スコア | van Bijsterveld スコア | van Bijsterveld スコア |
両者とも死細胞・変性細胞を染色するが、リサミングリーンの方が刺激が少なく患者の負担が軽い。ローズベンガルは点眼時に疼痛を生じることがあるため、場合によっては点眼麻酔が必要になる。リサミングリーンはこうした欠点を解消した代替色素として近年普及が進んでいる。観察には赤色フィルター(560 nm以上)を使用すると明瞭に染色部位を確認できる。
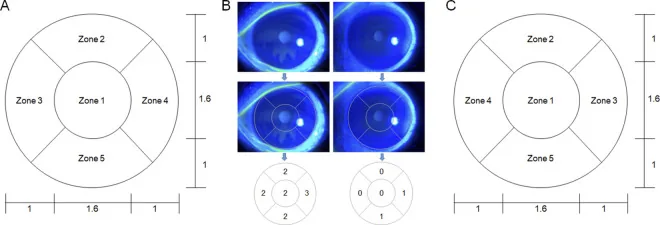
角結膜上皮障害を定量化するためのスコアリング体系が複数確立されている。
| スコア法 | 評価領域 | 評点範囲 | 合計 | 主な用途 |
|---|---|---|---|---|
| van Bijsterveld スコア | 角膜・鼻側球結膜・耳側球結膜(3領域) | 各0〜3点 | 9点満点(3.5点以上で異常) | Sjögren症候群診断基準 |
| Oxford スコアリング | 角膜・球結膜(鼻側・耳側)(3領域) | 各0〜4点(5段階) | 15点満点 | ドライアイ重症度評価 |
| NEI/Industry Workshop スコア | 角膜(5分割) | 各0〜3点 | 15点満点 | ドライアイ臨床研究 |
角膜・鼻側球結膜・耳側球結膜の3領域それぞれを0〜3点(0:染色なし、1:少数の点状染色、2:融合傾向の染色、3:広範囲の染色)で評価する。合計3.5点以上を異常とし、Sjögren症候群の診断基準として国際的に採用されている3)。
角膜・球結膜(鼻側・耳側)の3領域をそれぞれ0〜4点(5段階)で評価し、合計15点満点とする。各段階はパネル図と照合して半定量評価する。ドライアイの重症度評価や治療効果の判定に使用される。
角膜を中央・鼻上・耳上・鼻下・耳下の5区画に分割し、各区画を0〜3点で評価し合計15点満点とする。臨床研究や多施設試験で広く採用されている。
ドライアイ診療ガイドラインでの角結膜上皮障害基準(2006年版)1):
2016年版のドライアイ診断基準では上皮障害は診断の必須要件から外れたが、上皮障害の観察はドライアイの重症度評価・治療効果判定に引き続き重要な役割を担っている1)。
点状表層角膜症(superficial punctate keratopathy: SPK)は、異物感を訴える患者で最も頻度が高い眼所見である。SPKは何らかの原因によって角膜上皮が障害を受けた「結果」であり、原因診断名ではない。フルオレセイン生体染色はSPKの検出と分布パターンの把握に不可欠であり、細隙灯顕微鏡のみではわからない微細なSPKも可視化できる。
SPKを検出したら、その分布パターンから原因疾患を積極的に推定することが重要である。
| 分布パターン | 主な原因疾患 |
|---|---|
| 角膜下1/3に集中 | ドライアイ(涙液減少型)、眼瞼内反 |
| 角膜上1/3に集中 | 上輪部角結膜炎(SLK)、トラコーマ |
| 角膜全体(びまん性) | 薬剤毒性角膜症、ウイルス性角膜炎 |
| 3時〜9時方向(水平帯) | コンタクトレンズ(3-9 o’clock ステイニング) |
| 角膜中央 | 兎眼(ラグオフタルモス)、神経麻痺性角膜炎 |
外因性のSPK:
内因性のSPK:
薬剤毒性角膜症では、角膜上皮の障害に比べて結膜上皮の障害が少ないという特徴がある。この所見はフルオレセイン染色で明確に確認でき、他の原因疾患との鑑別に有用である。角膜全体にびまん性のSPKが認められる場合は、使用中の点眼薬(防腐剤・高濃度薬剤・アミノグリコシド系抗菌薬等)の影響を考慮する必要がある2)。
感染性角膜炎では、フルオレセイン染色により角膜上皮欠損の形状・面積・深さ(染色の濃淡で判断)を客観的に把握できる。潰瘍の範囲と形状が治療方針の選択・経過観察の指標として活用される2)。また抗菌点眼薬(高濃度製剤・アミノグリコシド系)は角膜上皮毒性を生じやすいため、治療経過中の上皮障害の悪化がないか生体染色で確認することが重要である2)。
生体染色で確認した上皮障害の分布と程度から原因を同定し、原因に応じた治療を選択する。
ドライアイ診療ガイドライン(2016年版)に基づく標準治療は以下の通りである1)。
感染性角膜炎診療ガイドライン(第3版)に基づき、原因菌の同定後に適切な抗菌薬を選択する2)。
フルオレセインは蛍光色素であり、コバルトブルー光(494 nm)を吸収して緑色蛍光(521 nm)を発する。蛍光発光の原理は吸収エネルギーを光として再放出するフォトルミネッセンスである。
ブルーフリーフィルター(バリアフィルター)は励起光(494 nm付近)を遮断し、蛍光波長(521 nm)のみを透過させる。これによって背景光が除去され、SPKの蛍光が際立って観察できる。細隙灯顕微鏡にブルーフリーフィルターを装着すると、コバルトブルーフィルターのみの観察に比べてSPKの検出感度が大幅に向上する。
角膜上皮の密着結合(tight junction)が破綻すると、細胞間隙にフルオレセインが浸透して蛍光を発する。正常な密着結合が保たれている部位はフルオレセインが侵入できず染色されない。
ローズベンガルはムチンによって保護されていない細胞を選択的に染色する。健常な眼表面細胞はムチン層(主に分泌型ムチンMUC5AC)で被覆されており、ローズベンガルの染色を防いでいる。死細胞・変性細胞はこのムチン保護が失われているため染色される。フルオレセインとは異なり死細胞そのものを染色するため、眼表面の細胞活性を反映する指標といえる。
リサミングリーンはローズベンガルと同様のメカニズムで死細胞・変性細胞を染色する。赤色フィルター(560 nm以上)下での観察で最も明瞭に染色を確認できる。ローズベンガルに比べて眼表面の刺激が少ない理由は、生体組織への浸透性が異なるためと考えられている。
ブルーフリーフィルターはフルオレセイン観察において特に重要である。フィルターなしのコバルトブルー光観察でも病変は確認できるが、ブルーフリーフィルターを追加することで: