
結膜擦過物細胞診・培養検査(感染症・アレルギー検査)(Conjunctival Cytology and Culture)
1. 結膜擦過物細胞診・培養検査とは
Section titled “1. 結膜擦過物細胞診・培養検査とは”結膜擦過物の細胞診・微生物培養検査は、感染性眼疾患における起炎菌の同定・薬剤感受性試験、およびアレルギー性結膜疾患における好酸球確認(確定診断)を目的とする検査である。早期に起炎菌を同定し、有効な抗菌薬を選択することで感染所見の改善をはかる。
感染性角膜炎診療ガイドライン(第3版)では、感染性角膜炎が疑われる場合に塗抹検鏡と培養検査を実施することを強く推奨している(エビデンスの強さC)1)。特に緊急性を有する角膜炎・眼内炎、特殊起炎菌の存在が疑われる症例では必須の検査と位置づけられている。
アレルギー性結膜疾患診療ガイドライン(第3版)では、好酸球検査(ハンセル染色)が確定診断の根拠として明示されており、臨床診断から確定診断への格上げに欠かせない検査法である2)。
感染性疾患を疑う場合
Section titled “感染性疾患を疑う場合”- 細菌性角膜炎・結膜炎(特に緊急性あり)
- 淋菌性結膜炎(角膜穿孔をきたしうるため早期診断が重要)
- アカントアメーバ角膜炎(一般施設では培養困難→検鏡検査を推奨)
- 真菌性角膜炎
- 特殊起炎菌が疑われる症例(難治性・治療抵抗性の角膜炎など)
アレルギー性眼疾患の確定診断
Section titled “アレルギー性眼疾患の確定診断”- アレルギー性結膜炎(好酸球検査による確定診断)
- 春季カタル(vernal keratoconjunctivitis: VKC)
- アトピー性角結膜炎(atopic keratoconjunctivitis: AKC)
2. 検体採取の手技
Section titled “2. 検体採取の手技”検体採取は起炎菌の存在が疑われる部位からしっかり採取することが原則である。採取タイミングが陽性率に大きく影響する。抗菌薬投与前の培養陽性率は77.3%であるのに対し、投与後では37.8%に低下するとされる1)。抗菌薬を投与する前に必ず採取しておく。
- 麻酔: 点眼麻酔を使用する。防腐剤フリーのものが望ましい(防腐剤による微生物への影響を避けるため)
- 採取器具: キムラスパーテルまたはゴルフ刀(結膜・角膜の擦過用)。または化学繊維の綿棒
- 採取部位: 病巣部と正常組織の境界域を擦過する。炎症部と正常角膜の境界部に菌が存在するため、その境界域が最も適している
- 乾燥防止: 綿棒で採取する際は、あらかじめ滅菌生理食塩水で綿棒を湿らせておく。乾燥により検体の質が低下する
- 綿棒の素材: 化学繊維のものを使用する。天然素材は微生物の増殖や検査方法に影響することがある
- 病巣部が極めて脆弱な例もある。無理に擦過しない
- スワブによる病巣擦過の培養陽性率は約50%、23G針では35%との報告がある1)
- 採取量が少ない場合は検査の優先順位を検査室に明記する
最も重要なのは抗菌薬投与前に採取することである。抗菌薬投与後では培養陽性率が77.3%から37.8%へと大幅に低下する。採取部位は病巣部と正常組織の境界域であり、炎症中心ではなく境界部を擦過する。綿棒はあらかじめ滅菌生理食塩水で湿らせて乾燥を防ぐ。採取器具は化学繊維の綿棒またはキムラスパーテル・ゴルフ刀を用い、点眼麻酔下で行う。病巣が脆弱な場合は無理に擦過しない。
3. 塗抹・検鏡検査(染色法と判定)
Section titled “3. 塗抹・検鏡検査(染色法と判定)”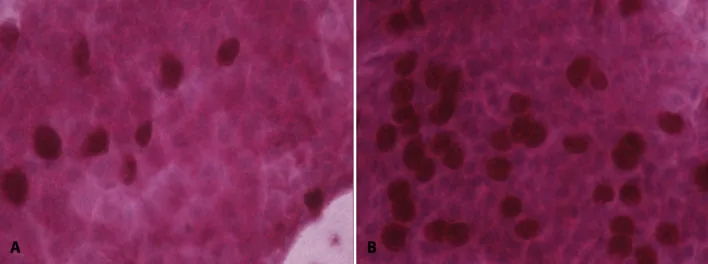
採取した検体をスライドガラスに塗抹し、染色して光学顕微鏡で観察する。塗抹検鏡の陽性率は58.1〜73.7%とされる1)。
標本作製手順
Section titled “標本作製手順”- スライドガラスをアルコールで清拭し、検体塗抹部を裏からダイヤモンドペンシルまたはマジックで丸印をつける
- スパーテルは軽く広げるように薄くのばして塗抹する。綿棒は検体量が少量の場合はスタンプを押すように、ある程度ある場合は転がすように塗抹する
- メチルアルコールまたは火炎で固定する
染色法の選択
Section titled “染色法の選択”目的に応じて5種の染色法から選択する。
- ギムザ染色(ディフクイック™): 感染・非感染を含めたスクリーニングに用いる多目的染色法。簡易迅速染色セット(ディフクイック™)で約15秒という短時間で従来法と同等の染色が得られる。微生物はすべて青色に染まるが、グラム陽性・陰性の区別は不可1)
- グラム染色: 細菌性感染に特化した染色法。グラム陽性・陰性の区別が可能で細菌の形態(球菌・桿菌)を確認できる。フェイバーG(日水製薬)を使えば約3分で完了する1)
- ファンギフローラY®染色: スチルベンジルスルホン酸系蛍光染料。β構造多糖類(キチン・セルロース)を特異的に染色し、真菌(菌糸・酵母)とアカントアメーバのシストを鋭敏に検出する。蛍光顕微鏡での観察が必要1)
- 蛍光抗体法: HSV(単純ヘルペスウイルス)・VZV(水痘帯状疱疹ウイルス)等のウイルス抗原を直接証明する1)
- ハンセル染色: アレルギー性結膜疾患における好酸球の検出に用いる専用染色法
- 400倍: 炎症細胞(好中球直径約12〜15μm)の種類を確認する。細菌性感染では好中球優位、ウイルス性感染ではリンパ球優位となる
- 油浸1,000倍: 菌体(細菌直径約1.0μm)を鏡検する
病原体別の染色法と特徴的所見
Section titled “病原体別の染色法と特徴的所見”| 疑う病原体 | 推奨染色法 | 特徴的所見 |
|---|---|---|
| 細菌(一般) | グラム染色 | グラム陽性/陰性の球菌・桿菌 |
| 淋菌 | ディフクイック™ | そら豆型双球菌・好中球内貪食 |
| 真菌 | ファンギフローラY® | 菌糸・分生子(蛍光) |
| アカントアメーバ | ファンギフローラY® | 二重壁シスト(10×10μm前後) |
| ウイルス(HSV等) | 蛍光抗体法 | 感染細胞の特異蛍光 |
| 好酸球(アレルギー) | ハンセル染色 | 好酸球1個でも陽性 |
4. 培養検査
Section titled “4. 培養検査”培養検査では原因微生物を培地上で増殖させ、同定・薬剤感受性試験が可能となる。培養陽性率は施設・条件により37.6〜74.3%と幅がある1)。外眼部には常在菌が存在するため、分離された菌が必ずしも起炎菌とは限らない。検鏡結果・眼所見・薬剤感受性・治療効果から総合的に判断する。
主な培地の種類
Section titled “主な培地の種類”| 培地 | 対象微生物 | 培養条件 |
|---|---|---|
| 血液寒天培地 | 一般細菌(溶血性判定可能) | 37℃、好気 |
| チョコレート寒天培地 | Haemophilus属・淋菌(V因子・X因子含有) | 37℃、CO₂ |
| サブロー/ポテトデキストロース培地 | 真菌 | 37℃と室温の2条件で培養 |
| 1.5% NN寒天平板 | アカントアメーバ | 30℃ |
| 輸送用培地(シードスワブ®、トランスワブ®等) | 一般菌(施設に固形培地がない場合) | 常温輸送(陽性率50〜69%)1) |
検査機関への輸送まで時間がかかる場合の保存方法は起炎菌の種類によって異なる。
- 一般細菌: 4°C(冷蔵庫)で保存
- 淋菌・髄膜炎菌: 低温に弱く死滅しやすいため、常温で保存する
- 偏性嫌気性菌を疑う場合: 嫌気ポーターに入れて保存する
検査オーダーのポイント
Section titled “検査オーダーのポイント”- 依頼票に臨床所見と標的微生物を明記する。選択培地の追加により検出率が向上する
- 採取量が少ない場合は検査の優先順位(例:培養>検鏡、細菌>真菌)を付記する
薬剤感受性試験の解釈
Section titled “薬剤感受性試験の解釈”薬剤感受性試験ではS(sensitive)の中でMIC(最小発育阻止濃度)が低い薬剤を選択することが多い。ただし、R(resistant)と判定されても臨床的に有効な場合もあり、総合的な評価が必要である。真菌・アカントアメーバの薬剤感受性試験については判定基準が確立していない点に留意する1)。
培養陽性率は37.6〜74.3%であり、陰性でも感染を否定できない。最も影響する因子は検体採取タイミングであり、抗菌薬投与後の採取では陽性率が約半減する。また、塗抹検鏡で陰性の症例での培養陽性率は42.7〜47.1%、塗抹陽性の症例での培養陽性率は57.1〜82.4%とされ、両検査を組み合わせることで診断精度が上がる。アカントアメーバは一般施設では分離培養が困難なため、ディフクイック™染色による検鏡検査でシストの二重壁構造を確認することを優先する。
5. 好酸球検査(アレルギー性結膜疾患の確定診断)
Section titled “5. 好酸球検査(アレルギー性結膜疾患の確定診断)”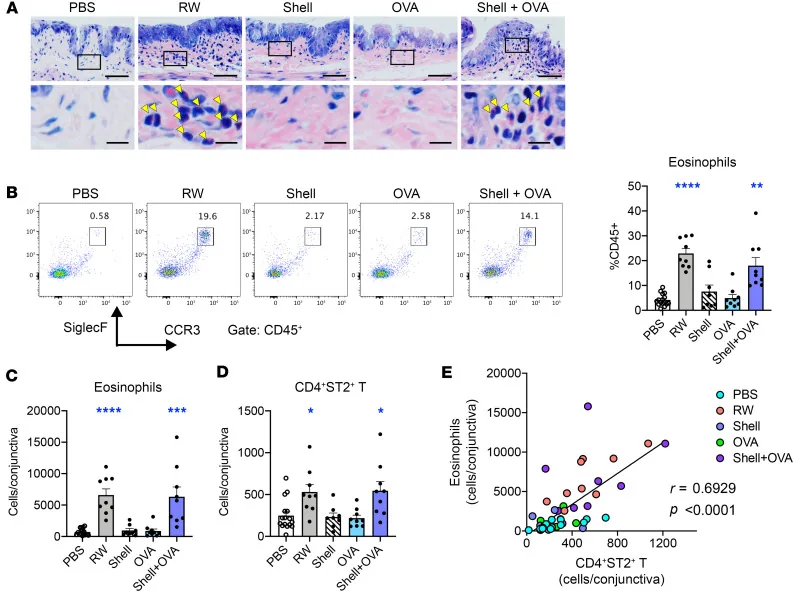
アレルギー性結膜疾患の確定診断には、結膜擦過塗抹標本のハンセル染色による好酸球検出が必要である2)。
- 点眼麻酔後に上眼瞼を翻転する
- 硝子棒で瞼結膜を軽くマッサージし、結膜表面に溜まった粘液を鑷子またはスパーテルで採取する
- プレパラートに塗抹してハンセル染色を行い、光学顕微鏡で観察する
顕微鏡下で好酸球を1つでも確認できれば陽性と判定し、アレルギー性結膜疾患の確定診断となる2)。採取時に出血がみられた場合は血液中の好酸球が混入する可能性があるため、他眼で再検査を行う。
アレルギー性結膜疾患の診断体系
Section titled “アレルギー性結膜疾患の診断体系”アレルギー性結膜疾患診療ガイドライン(第3版)に基づく診断の3段階は以下の通りである2)。
| 診断区分 | 必要条件 |
|---|---|
| 臨床診断 | 臨床所見のみ(アレルギー性の症状・所見) |
| 臨床的確定診断 | 臨床所見 + アレルギー素因確認(涙液総IgE陽性・皮膚テスト・血清抗原特異的IgE陽性) |
| 確定診断 | 臨床所見 + 好酸球検査陽性(眼局所アレルギー反応の確認) |
臨床的確定診断は全身性アレルギー素因の確認にとどまり、眼局所でのアレルギー反応を直接証明するものではない。好酸球検査によって眼局所のアレルギー反応が直接証明されることで初めて確定診断となる2)。
6. 検査結果の解釈と総合判断
Section titled “6. 検査結果の解釈と総合判断”炎症細胞の種類による病原体推定
Section titled “炎症細胞の種類による病原体推定”菌体が見つからない場合でも、炎症細胞の種類が病原体推定の手がかりとなる。
- 好中球優位 → 細菌性感染を示唆
- リンパ球優位 → ウイルス性感染を示唆
- 好酸球優位 → アレルギー性・寄生虫感染を示唆
起炎菌の総合判断
Section titled “起炎菌の総合判断”分離菌が起炎菌かどうかは複合的に判断する。
- 検鏡結果と培養分離菌の相同性(検鏡で見た菌と培養で発育した菌が一致するか)
- 眼所見との整合性(病巣部から採取した検体か)
- 薬剤感受性試験の結果と実際の治療効果の一致
特殊な病原体への注意
Section titled “特殊な病原体への注意”- 淋菌: 乾燥・温度変化に弱く死滅しやすい。採取直後の処理が不可欠。低温保存は不適切(常温保存)
- アカントアメーバ: 一般施設では分離培養が困難。ディフクイック™染色で二重壁を特徴とするシストの確認を優先する
塗抹検鏡と培養検査の組み合わせ
Section titled “塗抹検鏡と培養検査の組み合わせ”塗抹検鏡陰性の症例でも培養陽性率は42.7〜47.1%に達する1)。一方、塗抹陽性の症例の培養陽性率は57.1〜82.4%であり、両検査を同時実施することで感度が上がる。PCR検査は塗抹検鏡・培養検査の補助として有用であるが、PCRのみで細菌性角膜炎を診断することは推奨されない1)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”- メタゲノム解析(次世代シーケンサー): 培養不能菌を含む眼表面マイクロバイオームの網羅的解析が可能になりつつある。従来の培養検査では同定できない病原体の検出が期待されている
- マルチプレックスPCR: 複数の病原体(細菌・真菌・ウイルス・アカントアメーバ)を1回の検査で同時に迅速検出するシステムの開発が進んでいる。感染性角膜炎の診断精度と速度の向上が期待される3)
- MALDI-TOF質量分析法: 培養した菌をわずか数分で同定できる質量分析技術。従来の生化学同定法と比べ大幅な時間短縮が可能であり、眼科感染症への応用が研究されている4)
- 好酸球検査の感度・特異度の精密化: 電子顕微鏡や蛍光標識抗体を用いた好酸球の高感度検出法の開発が進んでいる。従来のハンセル染色では検出感度に限界があり、より高感度な検出法が確立されれば診断精度が向上する可能性がある
8. 参考文献
Section titled “8. 参考文献”- 日本眼感染症学会感染性角膜炎診療ガイドライン第3版作成委員会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023;127(10):859-918.
- 日本眼科アレルギー学会診療ガイドライン作成委員会. アレルギー性結膜疾患診療ガイドライン(第3版). 日眼会誌. 2021;125(8):741-785.
- Liu HY, Hopping GC, Vaidyanathan U, Ronquillo YC, Hoopes PC, Moshirfar M. Polymerase Chain Reaction and Its Application in the Diagnosis of Infectious Keratitis. Med Hypothesis Discov Innov Ophthalmol. 2019;8(3):152-155. PMID:31598517; PMCID:PMC6778471.
- Taravati P, Lam D, Van Gelder RN. Role of molecular diagnostics in ocular microbiology. Curr Ophthalmol Rep. 2013;1(4):170-178.
