
レーザーフレアメーター(前房蛋白濃度測定・炎症評価)(Laser Flare Meter)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. レーザーフレアメーターとは
Section titled “1. レーザーフレアメーターとは”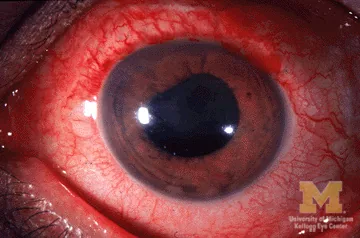
レーザーフレアメーターは前房内にHe-Neレーザー光を照射し、前房水中の蛋白質によるチンダル現象(光散乱)を電子的に定量測定する機器である。前房蛋白濃度をphoton count/ms(ph/ms)の単位で客観的に数値化できる。
前房フレアは前房内蛋白濃度を反映する指標である。フレアが上昇する機序は主に2つある。第一に、炎症や新生血管などによって虹彩・毛様体の血管バリアが破綻し、血液中の蛋白質が前房内に漏出すること。第二に、毛様体機能の低下により房水循環が悪化し、前房内に老廃物蛋白が貯留することである。
細隙灯顕微鏡を用いた主観的グレーディングは日常診療で必須のスキルである。ただし、主観的評価には施設間・観察者間のばらつきが生じる。レーザーフレアメーターはこの限界を補い、経時的な炎症の定量追跡を可能にする。
SUN Working Group(Standardization of Uveitis Nomenclature、ぶどう膜炎命名法標準化作業部会)は前房フレアおよび前房細胞の国際標準グレーディング基準を策定しており、ぶどう膜炎診療ガイドラインに採用されている1)2)。
前房内の蛋白濃度をph/ms(photon count/ms)という単位で客観的に定量できる。ぶどう膜炎の炎症活動性や治療効果を数値で追跡できるほか、白内障術後の炎症反応の推移を評価することも可能である。細隙灯顕微鏡では検出困難な低活動性の微細な変化も捉えられる点が特徴である。
2. 検査方法
Section titled “2. 検査方法”レーザーフレアメーターによる測定
Section titled “レーザーフレアメーターによる測定”代表的な機器はKOWA FM-600(FM-500後継機)である。He-Neレーザー光(波長675 nm)を前房内に照射し、散乱光をフォトマルチプライヤー(光電子増倍管)で受光してphoton countに変換する。
- 測定単位: photon count/ms(ph/ms)
- 成人正常値: 3〜7 ph/ms(機器・個人差あり)
- 測定方法: 非接触・非侵襲。散瞳は不要。1回の測定は数秒で完了する
- 標準プロトコル: 7回測定し最大値・最小値を除いた5回の平均値を採用する
- 測定精度: バックグラウンドノイズを差し引いた実測値を前房フレア値とする
細隙灯顕微鏡によるフレアグレーディング(SUN基準)
Section titled “細隙灯顕微鏡によるフレアグレーディング(SUN基準)”スリット幅を絞って高さを約3 mmにし、光線幅が前房内で見えるような角度から照射して正面から観察する。前房内蛋白濃度が上昇すると、通常は観察されない光路がチンダル現象によって明瞭に描出される。
SUN Working Groupによる前房フレアのグレーディング基準は以下のとおり1)2)。
| グレード | 記述 |
|---|---|
| 0 | none(なし) |
| 1+ | faint(軽度) |
| 2+ | moderate(中等度)虹彩および水晶体の詳細は明瞭 |
| 3+ | marked(高度)虹彩および水晶体の詳細は不明瞭 |
| 4+ | intense(著明)線維素あるいはプラスティック前房水 |
SUN Working Groupによる前房細胞のグレーディング基準(1×1 mmスリット光1視野あたりの細胞数)は以下のとおり1)2)。
| グレード | 1視野にみられる細胞数 |
|---|---|
| 0 | <1(1個未満) |
| 0.5+ | 1〜5 |
| 1+ | 6〜15 |
| 2+ | 16〜25 |
| 3+ | 26〜50 |
| 4+ | >50(51個以上) |
(1視野 = 細隙灯顕微鏡スリット光1×1 mmの大きさの視野)
細隙灯顕微鏡によるフレアグレーディングはSUN基準の0〜4+という主観的5段階評価である。施設間や観察者間にばらつきが生じやすい。レーザーフレアメーターはph/msという客観的定量値を得られるため、低活動性炎症での微細変化の検出や経時的な追跡に優れる。日常診療では細隙灯グレーディングが標準で、フレアメーターは定量的評価が必要な場合に用いられる。
3. 前房炎症所見の評価体系
Section titled “3. 前房炎症所見の評価体系”前房炎症の評価は、フレア・細胞・温流・蓄膿・フィブリンを体系的に観察することで行う。
- 前房フレア: 前房内蛋白濃度の上昇を反映する。血管バリア破綻(炎症・新生血管)と毛様体機能低下の2つの機序による
- 前房細胞: SUN基準の1×1 mmスリット光1視野内の炎症細胞数をカウントする。好中球・リンパ球・形質細胞などが混在する場合がある1)
- 前房温流(Aqueous flare circulation): 細胞グレーディングと同時に観察する。房水産生能と前房内蛋白濃度を反映し、病勢および治療効果の判定に有用である
- 前房蓄膿(Hypopyon): 下方前房に白色沈殿物として視認される。体位変換で移動するさらさらタイプと、塊状に固定するタイプに分かれる
前房蓄膿の2類型を以下に示す。
| 分類 | 特徴 | 代表疾患 |
|---|---|---|
| さらさらタイプ | 体位で変動する | Behçet病急性期・重症細菌性眼内炎 |
| 塊状固定タイプ | 一定部位に固定 | 単球系細胞・フィブリン析出を伴う炎症 |
フレアの最重症型:前房内フィブリン
Section titled “フレアの最重症型:前房内フィブリン”前房内フィブリンはフレアの最重症型である。前房内に明瞭な塊、または霧状・綿花状析出物として観察される。フィブリン析出は高頻度に虹彩後癒着(後部虹彩癒着)や眼圧上昇を引き起こすため、特に注意が必要である。
SUN基準による炎症活動性の定義
Section titled “SUN基準による炎症活動性の定義”SUN Working Group基準では、ぶどう膜炎の活動性を以下のように定義する2)。
- inactive(非活動性): グレード 0
- worsening(悪化): グレード 2段階以上の上昇
- improved(改善): グレード 2段階以上の低下
- remission(寛解): 薬物療法なしで非活動性が3か月以上持続
4. 臨床的意義と適応
Section titled “4. 臨床的意義と適応”ぶどう膜炎の活動性モニタリング
Section titled “ぶどう膜炎の活動性モニタリング”レーザーフレアメーターはぶどう膜炎診療ガイドラインに推奨される前房フレアの定量化手段である1)。細隙灯所見との相関性が高く、治療経過の定量的追跡に有用である。特に以下の場面で優れた価値を発揮する。
- 低活動性ぶどう膜炎での微細な炎症変化の検出
- 免疫抑制薬・生物学的製剤の治療効果の定量的評価
- 臨床研究でのアウトカム指標
ぶどう膜炎の頻度の高い疾患はサルコイドーシス(10.7%)、VKH病(フォークト-小柳-原田病、7.0%)、急性前部ぶどう膜炎(6.6%)である1)。これらの疾患では長期にわたる炎症モニタリングが必要であり、フレアメーターの定量評価は治療調整に役立つ。
白内障術後炎症評価
Section titled “白内障術後炎症評価”術後前房フレア値の正常化速度は術後管理の指標となる。白内障手術後は一般的に術後1週から徐々に低下し、術後1〜3か月で正常値域(3〜7 ph/ms)への回復が期待される3)。フレア値の遷延上昇は術後炎症の遷延や合併症(囊胞様黄斑浮腫等)を示唆する。
生物学的製剤の効果評価
Section titled “生物学的製剤の効果評価”アダリムマブ・インフリキシマブ等の生物学的製剤によるぶどう膜炎治療において、フレアメーター値が治療反応のバイオマーカーとして用いられる4)。細隙灯グレーディングよりも感度高く炎症の再燃・改善を検出できる。
角膜後面沈着物(KP)との関連
Section titled “角膜後面沈着物(KP)との関連”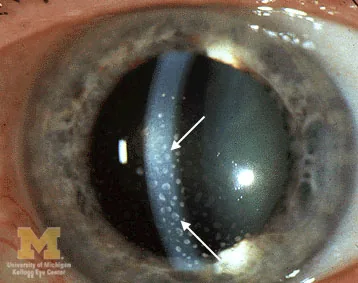
KP(keratic precipitates、角膜後面沈着物)は前房水中の白血球・虹彩色素・赤血球が角膜後面に沈着・集簇したものである。KPの性状・分布はフレア所見と組み合わせることで疾患の鑑別補助となる。
KPの性状と関連疾患の対応を以下に示す。
| KPの性状 | 特徴 | 疑われる疾患 |
|---|---|---|
| 豚脂様(mutton-fat)KP | 大型・脂肪様外観 | サルコイドーシス・VKH病(肉芽腫性ぶどう膜炎) |
| 微塵様(fine)KP | 小型・微細 | 非肉芽腫性ぶどう膜炎 |
| 白色KP | 新鮮・活動性炎症を示す | 現在の活動性眼内炎症 |
| 茶色KP | 虹彩色素を取り込んだ旧KP | 過去の炎症残存(活動性なし) |
KPの分布も診断の手がかりとなる。通常は前房水の対流により角膜中心より下方の三角形領域に多くみられる。上方まで散在性の小型白色KPがみられる場合はFuchs虹彩異色性虹彩毛様体炎(Fuchs虹彩炎症候群)が疑われる。突起(stellate)のあるKPはヘルペス性虹彩炎などの感染性ぶどう膜炎で特徴的に認められる。
以下の3つの場面で特に有用である。①低活動性ぶどう膜炎の長期経過観察:細隙灯グレーディングでは検出困難な微弱な炎症変化をph/ms値の変動として捉えられる。②白内障術後炎症評価:フレア値の正常化速度で術後の炎症収束を客観的に確認できる。③臨床研究でのアウトカム評価:ぶどう膜炎治療薬の治験等で標準的な定量的評価指標として用いられる。
5. 検査結果の解釈と対応
Section titled “5. 検査結果の解釈と対応”レーザーフレアメーター値の解釈の目安は以下のとおりである。
- 正常域(3〜7 ph/ms): 健常成人の参考値。機器・個人差あり
- 軽度上昇(8〜15 ph/ms程度): 低活動性炎症・術後早期の生理的反応として許容範囲の場合がある
- 中等度上昇(15〜50 ph/ms程度): 活動性前部ぶどう膜炎・術後炎症の遷延が疑われる。ステロイド点眼の強化等を検討する
- 高度上昇(50 ph/ms以上): 重度炎症。フィブリン析出・虹彩後癒着・眼圧上昇のリスクが高い。フルオロメトロン等のステロイド点眼を高頻度(1時間ごと等)に使用し、0.5〜1%硫酸アトロピン点眼による散瞳・毛様体筋麻痺を行う
ぶどう膜炎のフレア値と細隙灯グレーディングの相関係数は0.6〜0.8程度とされ、グレードが上昇するにつれてph/ms値も上昇するが、個体差が大きいため絶対値での比較よりも個人の経時的変化の追跡が重要である5)。
SUN基準による治療効果の判定はグレード2段階以上の変化を基準とする2)。フレアメーターでは治療開始後1〜2週でのph/ms値低下率が治療反応の早期指標となりうる3)。
治療対応の原則は原疾患に応じる。一般的には以下を考慮する。
- ステロイド点眼: ベタメタゾン0.1%点眼液・フルオロメトロン0.1%点眼液等。炎症の強度に応じて1日4〜12回の頻回点眼
- 散瞳薬: 0.5〜1%硫酸アトロピン点眼液(虹彩後癒着予防・毛様体筋麻痺による疼痛軽減)またはトロピカミド0.5%点眼液
- ステロイド内服・点滴: 重症例にはプレドニゾロン内服(0.5〜1 mg/kg/日)またはメチルプレドニゾロン500〜1000 mg/日の3日間大量点滴療法
- 免疫抑制薬: シクロスポリン・タクロリムス・メトトレキサート等を難治例に使用
- 生物学的製剤: アダリムマブ(非感染性ぶどう膜炎に保険適用)・インフリキシマブ等
6. 測定原理(光学原理の詳細)
Section titled “6. 測定原理(光学原理の詳細)”レーザーフレアメーターの光学原理はチンダル現象(Tyndall effect)に基づく。
- He-Neレーザー光(波長675 nm)が前房内に照射される
- 前房水中の蛋白質粒子によって光が散乱する(チンダル現象)。正常の透明な前房水では散乱は最小限だが、蛋白濃度が上昇するとチンダル現象が増強される
- 散乱光をフォトマルチプライヤー(光電子増倍管)で受光し、photon countに変換する
- バックグラウンドノイズ(非散乱光成分)を差し引いた実測値が前房フレア値(ph/ms)となる
- 蛋白濃度が高いほど散乱光量が増加し、ph/ms値が上昇する
細隙灯顕微鏡で観察される「チンダル現象」と同じ物理現象を電子的に定量化したものが、レーザーフレアメーターの本質的な原理である。細隙灯でのフレア観察では、スリット光が前房内を通過する際に光路が白く見えるのも同じ機序による。
蛋白粒子のサイズがレーザー波長の1/10以下の場合はRayleigh散乱、同程度以上の場合はMie散乱が支配的となる。前房内蛋白質(分子量数万〜数十万ダルトン)はMie散乱の範疇に近い散乱特性を示す。散乱光強度は蛋白濃度とほぼ線形相関するため、ph/ms値から蛋白濃度を定量推定できる5)6)。
7. 最新の研究と今後の展望
Section titled “7. 最新の研究と今後の展望”- 前眼部OCTによる前房フレア定量化: 前眼部OCT(AS-OCT)を用いた前房内光散乱の画像的定量化が試みられている。レーザーフレアメーターが普及していない施設での代替手段として研究が進む7)
- 生物学的製剤の効果評価への応用: アダリムマブ・インフリキシマブ等の生物学的製剤による非感染性ぶどう膜炎治療において、フレアメーター値が治療反応の早期指標として研究されている4)
- AIによる細隙灯画像からの自動フレアグレーディング: 細隙灯写真の機械学習による自動フレアグレーディングが研究段階にある。今後は客観的な主観的グレーディングの標準化が期待される
- ドライアイ・緑内障手術後の炎症評価への拡大応用: ドライアイに伴う前房内微小炎症の評価、線維柱帯切除術後の炎症モニタリングへの応用が報告されている8)
8. 参考文献
Section titled “8. 参考文献”- 日本眼炎症学会ぶどう膜炎診療ガイドライン作成委員会. ぶどう膜炎診療ガイドライン. 日眼会誌. 2019;123(6):635-696.
- Jabs DA, Nussenblatt RB, Rosenbaum JT; Standardization of Uveitis Nomenclature (SUN) Working Group. Standardization of uveitis nomenclature for reporting clinical data. Results of the First International Workshop. Am J Ophthalmol. 2005;140(3):509-516.
- Oshika T, Yoshimura K, Miyata N. Postsurgical inflammation after phacoemulsification and extracapsular extraction with soft or conventional intraocular lens implantation. J Cataract Refract Surg. 1992;18(4):356-361.
- Díaz-Llopis M, Salom D, Garcia-de-Vicuña C, et al. Treatment of refractory uveitis with adalimumab: a prospective multicenter study of 131 patients. Ophthalmology. 2012;119(8):1575-1581.
- Sawa M, Tsurimaki Y, Tsuru T, Shimizu H. New quantitative method to determine protein concentration and cell number in aqueous in vivo. Jpn J Ophthalmol. 1988;32(2):132-142. PMID: 3054216.
- Ladas JG, Wheeler NC, Morhun PJ, Rimmer SO, Holland GN. Laser flare-cell photometry: methodology and clinical applications. Surv Ophthalmol. 2005;50(1):27-47.
- Agarwal A, Ashokkumar D, Jacob S, Agarwal A, Saravanan Y. High-speed optical coherence tomography for imaging anterior chamber inflammatory reaction in uveitis: clinical correlation and grading. Am J Ophthalmol. 2009;147(3):413-416.
- Ayala M. Laser flare photometry: a useful tool for glaucoma management. J Glaucoma. 2012;21(5):343-347.
