鉄錆症(シデローシス)は鉄含有眼内異物 (IOFB )の残留による鉄イオン毒性で生じる進行性の眼組織障害である。
銅錆症(カルコーシス)は銅含有IOFB の残留による。純銅(90%以上)は急性型、真鍮などの低濃度銅は慢性型をとる。
有病率は眼外傷患者の約0.002%と稀だが、見逃した場合は不可逆的な視力 障害に至る。1)
鉄錆症患者の約96%が男性であり、ハンマー・タガネ作業中の金属片受傷が最多である。1)
網膜電図 (ERG )のb波減弱は鉄錆症の早期変化の指標であり、治療タイミングの決定に最重要である。4) 銅錆症に特有の所見として、エメラルドリング(水晶体 前囊下の緑色輪状混濁)とKayser-Fleischer環様の角膜 変化がある。
IOFB の早期除去が両疾患に共通する根本治療であり、除去群は非除去群に比べ視力 転帰が有意に良好である。1) 眼鉄錆症 (Ocular Siderosis / Siderosis bulbi)は、鉄または鉄合金を含む眼内異物 (intraocular foreign body; IOFB )が眼内に残留した際に生じる疾患である。残留した鉄が眼組織に溶け出し、鉄イオンが角膜 ・虹彩 ・水晶体 ・網膜 ・線維柱帯 など眼の各組織を障害する。本疾患の概念は1860年にBungeによって初めて記載された。有病率は眼外傷患者の約0.002%と稀な疾患である。1)
眼銅錆症(Ocular Chalcosis)は、銅または銅合金のIOFB の残留による疾患である。銅イオンが眼内各組織に沈着し、特有の組織障害をきたす。純銅(銅含有率90%以上)が残留した場合は急性型として重篤な眼内炎 様反応を呈する。真鍮や青銅などの低濃度銅合金では慢性緩徐な経過をとる。
IOFB は眼内に初期には無症状のまま残留し、徐々に進行性の組織障害を引き起こすため、診断の遅れが視力 予後を著しく悪化させる。眼内異物 全体の30〜40%が磁性体(鉄・鋼)を占め、銅合金異物は比較的まれである。
金属 疾患名 異物の特徴 臨床経過 鉄・鉄合金 鉄錆症(Siderosis bulbi) 磁性体 慢性進行性 純銅(≥90%) 銅錆症・急性型 非磁性体 急性重篤(眼内炎 様) 真鍮・銅合金 銅錆症・慢性型 非磁性体 慢性緩徐
Q
鉄以外の金属でも眼内で問題を起こすのか?
A
銅含有IOFB では鉄錆症と同様に重篤な「眼銅錆症(Chalcosis)」が生じる。純銅は急性の眼内炎 様反応、真鍮は慢性の沈着障害をきたす。アルミニウムやガラスは組織反応が軽微であり、鉄錆症・銅錆症とは区別される。
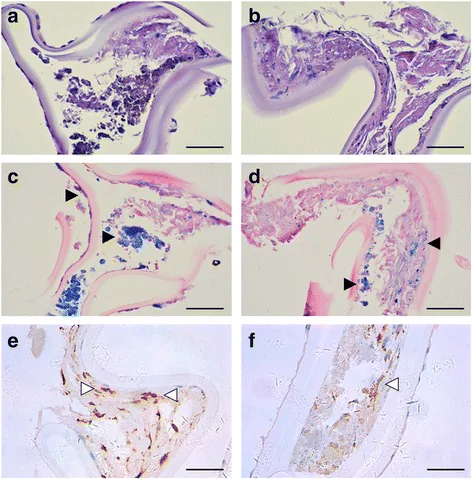
眼内鉄錆症(Siderosis bulbi)の水晶体前嚢組織病理像:ヘモジデリン沈着とプルシアンブルー鉄染色 Ye Y, et al. Ocular siderosis caused by a retained intralenticular iron foreign body: a case report. BMC Ophthalmol. 2017;17:26. Figure 5. PM
CI D: PMC5348785. License: CC BY.
眼内鉄錆症における
水晶体 前嚢の病理組織像。HE染色(a, b)でヘモジデリン沈着、プルシアンブルー染色(c, d)で鉄色素の蓄積、CD18陽性マクロファージの浸潤(e, f)が前嚢に示されている。本文「主な症状と臨床所見」の項で扱う鉄錆性
白内障 に対応する。
鉄錆症の自覚症状は受傷直後から現れるものと、異物残留後に徐々に進行するものに分けられる。
視力 低下1) 無症候性 :初期には症状が乏しく、患者の約27.58%が自覚症状を欠いた状態で発見される。1) 夜盲 ・視野狭窄眼痛 ・充血 IOFB 受傷の急性期や炎症合併時にみられる。
鉄錆症の眼所見
角膜 鉄線沈着1)
鉄性散瞳 (mydriasis siderostica) :虹彩 括約筋への鉄障害による特徴的な散瞳 。3)
鉄錆性白内障 :水晶体 前嚢下の特徴的な褐色混濁。患者の約37.93%に認められる。1)
網膜色素上皮 (RPE )変性1)
銅錆症の眼所見
Kayser-Fleischer環様変化 :角膜輪部 (Descemet膜)への銅沈着による黄緑色輪状変化。慢性型に特徴的。
エメラルドリング :水晶体 前囊下の緑色輪状混濁。銅錆症の病的特徴所見。
日光白内障 :水晶体 の虹彩 様色調変化。
急性型所見(純銅) :眼内炎 様の高度炎症・前房蓄膿 ・硝子体混濁 。
鉄錆性緑内障 は重要な合併症である。線維柱帯 への鉄沈着により、続発開放隅角緑内障 を生じ得る4) 。
Q
鉄錆症では最初に何が障害されるか?
A
網膜電図 所見から桿体(rod)が選択的に早期に障害される。b波の減弱が最初に現れ、進行するとa波の減弱、さらには網膜電図 消失へと至る。詳細は「病態生理学」の項 を参照。4)
鉄錆症の原因は鉄または鉄合金を含むIOFB の眼内残留である。受傷機転の内訳では、ハンマー・タガネ作業 が最多であり、金属加工や建設作業中の金属片が最も多い受傷源となっている。1)
患者の96.49%が男性 であり、職業上の金属作業との関連が強い。1)
銅錆症の原因は銅または銅合金のIOFB の残留である。工場・鋳造現場での作業中や農機具の損傷、雷管の爆発などが受傷機転として挙げられる。
金属加工・建設作業 :打撃や研削による金属片の飛散が主要リスク防護眼鏡の非着用 :適切な保護具の不使用が受傷の主要要因1) 小型・高速のIOFB :眼球壁を貫通しやすく、受傷に気づかない場合がある初期無症状経過 :症状が乏しいため受診が遅れ、診断が遅延する3) 銅合金の種類 :純銅(≥90%)では急性重篤な経過となるリスクが高い
鉄錆症・銅錆症の診断は、IOFB の存在証明・位置確認と、眼組織への金属毒性の評価を組み合わせて行う。見逃しIOFB では外傷歴が不明確なため、他の疾患と誤診されやすい点に注意が必要である。3)
CT検査
鉄IOFB の検出 :CTは金属IOFB の位置確認に有用であり、見逃し例でも診断の鍵となる2) 。
見逃し防止 :現病歴が不明確な症例でも系統的なCT検索でIOFB を発見できる。
銅IOFB の検出 :銅・銅合金も金属として検出可能だが、アーチファクトに注意。
超音波検査
非侵襲的な眼内評価 :眼底観察が困難な症例(水晶体 混濁・硝子体出血 )での有用性が高い。
IOFB の位置確認硝子体 腔・網膜 下など部位の絞り込みに有効。
網膜電図(ERG)
b波減弱 :桿体機能の指標として早期変化を捉える。鉄錆症の治療タイミングの決定に最も重要。4)
重症度評価 :網膜電図 パターンの変化は鉄毒性の進行程度を反映する。
細隙灯顕微鏡・OCT
銅錆症の特徴所見 :エメラルドリングやKayser-Fleischer環様変化の確認に細隙灯が必須。
OCT RPE ・光受容体層の変性程度を定量的に評価し、術後経過観察にも用いる。
銅錆症ではKayser-Fleischer環がWilson病(肝レンズ核変性症)と類似するため、外傷歴が不明確な症例では鑑別が必要である。Wilson病では全身性の銅代謝異常(血清セルロプラスミン低下・尿中銅排泄増加)を伴うが、銅錆症では局所性の銅沈着にとどまる。銅代謝検査を必要に応じて実施する。
慢性的な経過をたどる見逃しIOFB 例では、慢性前部ぶどう膜炎 と誤診されることがある。3) 難治性ぶどう膜炎 や原因不明の水晶体 混濁・虹彩 変色では、外傷歴の詳細聴取とCT撮影によるIOFB の積極的な検索が重要である。
Parameswarappaら(2023)の58眼コホートにおける受診時視力 分布を以下に示す。1)
視力 割合 0.5以上(良好) 約34% 0.1〜0.4(中等度低下) 約29% 0.1未満(高度低下) 約37%
Q
CTで異物が見つからなければ鉄錆症は否定できるか?
A
CTの感度は異物の大きさ・材質・撮影条件に依存する。金属IOFB では有用だが、極小異物や非金属異物ではCTで検出できない場合がある2) 。臨床所見(鉄性散瞳 ・鉄錆性白内障 など)と合わせた総合的な判断が必要である。
鉄錆症・銅錆症の治療の根本はIOFB 早期除去
**硝子体手術 (pars plana vitrectomy; PPV )**がIOFB 除去の主要術式である。1, 2, 3, 4)
磁気プローブの使用 :鉄含有IOFB には磁気プローブが有効であり、PPV と組み合わせて異物を眼内から取り出す。3) 白内障 同時手術水晶体 混濁(鉄錆性白内障 )を合併する場合、症例に応じてPPV と白内障 手術を同時に検討する2) 。IOFB 除去群 vs 非除去群視力 転帰が得られた。1)
銅は非磁性体のため電磁石による摘出は不可能であり、PPV が必須術式となる。
急性型(純銅) :緊急手術が必要。PPV による異物除去と眼内炎 に準じた消炎治療(ステロイド 投与)を行う。眼球萎縮に至るリスクが高い。慢性型(真鍮・銅合金) :早期のPPV + 異物除去。術後炎症管理にステロイド を用いる。
項目 鉄錆症 銅錆症(急性型) 銅錆症(慢性型) 磁気プローブ 有効(磁性体) 不可(非磁性体) 不可(非磁性体) 主要術式 PPV ± 磁気プローブPPV (緊急)PPV 術後消炎 必要に応じてステロイド 眼内炎 に準じた治療ステロイド 眼球萎縮リスク 長期放置で高い 急性期に高い 比較的低い
鉄錆性緑内障 が合併した場合は、点眼・内服・手術による眼圧 管理が必要となる4) 。異物除去後も長期的な眼圧 モニタリングが重要である。
銅IOFB は非磁性体のため、電磁石による摘出を試みてはならない。PPV 必須。
網膜電図 のb波が消失した段階では不可逆的な光受容体障害が完成しており、IOFB 除去後も視力 回復が期待できない場合がある。4) 異物を見逃して診断が遅延するほど、金属毒性による網膜 障害が不可逆的に進行する。
IOFB 除去後も残存する網膜 変性・緑内障 に対しては継続的な管理が必要である。
Q
IOFBを長期間放置した場合はどうなるか?
A
鉄毒性は持続的・進行性であり、放置により視力 低下・夜盲 ・視野狭窄が不可逆的に進行する4) 。異物除去後も長期にわたるフォローアップが必要である。銅錆症の純銅型では急性の眼球萎縮に至るリスクもある。
眼内に残留した鉄は徐々に酸化・溶解し、鉄イオン(Fe²⁺/Fe³⁺)として眼組織に拡散する。鉄イオンによる細胞障害の中心的な機序は以下の2つの反応経路である。4, 3)
Haber-Weiss反応・Fenton反応 :鉄イオンが活性酸素種(ROS)の生成を触媒し、特に水酸化ラジカル(·OH)を産生する。水酸化ラジカルは細胞膜の脂質過酸化・DNA損傷・タンパク質変性を引き起こす。ミトコンドリア障害 :ROSによるミトコンドリア機能障害が、エネルギー依存性の高い光受容体に選択的な障害をもたらす。
眼鉄錆症 では桿体(rod)が錐体(cone)より先に障害 される特徴がある。網膜電図 では暗順応下のb波(桿体由来)が最初に減弱し、進行に伴いa波消失、さらには完全な網膜電図 消失へと至る。4) この桿体選択性は、桿体外節に含まれるcGMPホスホジエステラーゼが鉄イオンによる酸化ストレス に特に感受性が高いことに起因する。
線維柱帯 への鉄沈着は流出路の機械的閉塞と細胞毒性をもたらす。4) これにより眼房水 流出抵抗が上昇し、続発開放隅角緑内障 が生じる。異物除去後も線維柱帯 障害が持続することがあり、長期的な眼圧 管理が求められる。
銅イオンの毒性発現は銅濃度に依存する。
高濃度銅(純銅≥90%) :銅イオンが急性の細胞膜破壊とタンパク質変性を引き起こし、眼内炎 様の激烈な炎症反応が生じる。硝子体 ・網膜 ・角膜 への直接傷害が急速に進行し、眼球萎縮に至ることがある。低濃度銅(真鍮・銅合金) :銅イオンが慢性的に眼組織に沈着する。角膜 のDescemet膜への沈着がKayser-Fleischer環様変化を形成し、水晶体 前囊への沈着がエメラルドリングを形成する。網膜 では金属様の黄色反射が生じる。
Wilson病では全身の銅代謝異常(セルロプラスミン産生障害)による系統的な銅沈着が生じるのに対し、眼銅錆症では局所的なIOFB からの銅溶出による組織障害という点で病態が異なる。
網膜電図 による機能評価は、眼鉄錆症 の手術適応を決定する重要な指標として研究が進んでいる。b波の減弱程度と実際の網膜 組織障害の相関を定量化することで、「鉄毒性はあるが不可逆的障害には至っていない」早期ウィンドウでのIOFB 除去が視力 温存につながる可能性がある。4)
一部の報告では、IOFB を早期に除去した場合に網膜電図 所見の改善(約40%の部分的回復)が観察されている。鉄イオン誘発性の酸化ストレス が軽度の段階では、除去後に組織機能が回復し得ることが示唆されており、早期介入の根拠となる。
遅発性の眼圧 上昇や網膜 機能低下を見逃さないため、定期的な眼圧 ・視野・視神経 評価を継続する体制の標準化が課題である。
高分解能CTによる極小IOFB の検出精度向上、およびMRI安全性評価技術の進展は、鉄・銅異物の術前評価をより精緻なものにする可能性がある。特に銅合金など組成が混合する異物のMRI適応判断は重要な研究課題である。
Parameswarappa DC, Das AV, Venugopal R, Karad M, Tyagi M. Clinical profile, demographic distribution, and outcomes of ocular siderosis: electronic medical record-driven big data analytics from an eye care network in India. Indian J Ophthalmol. 2023;71(2):418-423. doi:10.4103/ijo.IJO_1446_22.
Chuah Gim Seah S, Muhammed J, Annie L, Othman K. Missed intraocular foreign body presenting as siderosis bulbi: two case reports. Cureus. 2024;16(2):e53839. doi:10.7759/cureus.53839.
Chai X, Li W, Zhao F, et al. Ocular siderosis misdiagnosed as chronic anterior uveitis: a case report. BMC Ophthalmol. 2026;26:102.
Kannan NB, Adenuga OO, Rajan RP , Ramasamy K. Management of ocular siderosis: visual outcome and electroretinographic changes. J Ophthalmol. 2016;2016:7272465. doi:10.1155/2016/7272465.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト)してください