デスメ膜瘤
デスメ膜皺襞:潰瘍底部にDMの皺を認める
中央透明帯:菲薄化領域の中央に透明な領域が存在する
前方膨隆:DMが嚢胞様に突出することがある1)

角膜実質および上皮層の欠損部を通じて、無傷のデスメ膜(Descemet membrane: DM)がヘルニア状に前方膨隆した状態である1)。DMは8〜10μmの透明で弾性のある無細胞膜であり、内皮細胞から分泌される1)。蛋白分解や生体力学的ストレスに比較的抵抗性があり、実質の破壊過程から内皮を保護する役割を担う1)。
デスメ膜瘤は位置により以下に分類される1):
サイズによる分類は、最大径で小(3mm未満)、中(3〜6mm)、大(6mm超)に分けられる1)。
角膜潰瘍が実質深部に及びDMを超えると角膜穿孔に至る。房水が漏出し前房が消失する。感染性・非感染性・外傷性の原因がある。
穿孔創の大きさ、部位、発生からの期間、角膜の状態を考慮し、保存的あるいは外科的治療を選択する。
デスメ膜瘤はデスメ膜が無傷のまま前方に膨隆した状態であり、穿孔の「一歩手前」に相当する。角膜穿孔はデスメ膜も破綻して房水が漏出した状態である。デスメ膜瘤は穿孔のリスクが高く、緊急介入が必要となる。
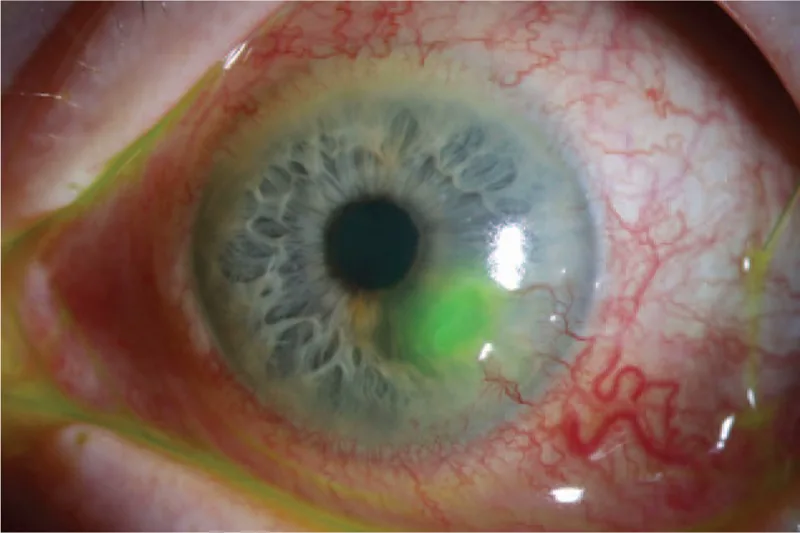
デスメ膜瘤
デスメ膜皺襞:潰瘍底部にDMの皺を認める
中央透明帯:菲薄化領域の中央に透明な領域が存在する
前方膨隆:DMが嚢胞様に突出することがある1)
角膜穿孔
ぶどう膜脱出:虹彩が欠損部から嵌頓する
サイデル試験陽性:フルオレセインの希釈・流出を確認する
浅前房・前房消失:房水漏出により前房が消失する
ぶどう膜脱出またはサイデル試験陽性は、角膜穿孔の確定診断所見である。ただしぶどう膜脱出が欠損部を塞いでいる場合、サイデル試験は偽陰性となりうる。
診断の遅れは角膜損傷の拡大、眼内炎、二次性緑内障・白内障、さらには眼球喪失につながりうる。
角膜潰瘍は中央部に生じるものと周辺部に生じるものに大別される。中央部潰瘍は感染性のものが多く、周辺部潰瘍は非感染性のものが多い。
| 分類 | 主な起炎微生物 |
|---|---|
| 細菌性 | 緑膿菌・ブドウ球菌・肺炎球菌・モラクセラ・淋菌 |
| 真菌性 | Fusarium・Aspergillus・Candida |
| ウイルス性 | 単純ヘルペス・帯状ヘルペス |
コンタクトレンズ(CL)装用は、米国における微生物性角膜炎の最大のリスク因子である7)。特にオーバーナイト装用(オルソケラトロジーを含む)は主要な感染リスクとなる7)。CL装用者ではグラム陰性菌(緑膿菌・モラクセラ・セラチア)が多い。
緑膿菌角膜炎は驚くほど急速に進行する。初期の小円形膿瘍が数日で輪状膿瘍を形成し、中央から穿孔する。菌が産生するプロテアーゼにより角膜が融解する。
真菌性角膜炎のうち糸状菌は、深層へ向かって進行しやすく前房蓄膿・角膜後面プラークを認める6)。感染が拡大すると最終的に強い融解を生じ穿孔に至ることがある6)。
淋菌による結膜炎で角膜炎を併発した場合は、高率に角膜穿孔を起こすため注意が必要である5)。
角膜穿孔の診断に不可欠な検査である。少量の滅菌生理食塩水で湿らせた滅菌フルオレセイン試験紙を穿孔疑い部位に塗布し、コバルトブルー光下で観察する。フルオレセインが希釈されて流出すれば陽性と判定する。
眼球への圧迫は穿孔を拡大させるリスクがあるため、検査時は最小限にとどめる。
角膜構造の詳細な評価に有用である1)。臨床的な視認が壊死物質や粘液性分泌物で妨げられる場合でも、実質の真の厚みやDMの膨隆を描出できる1)。経時的なスキャンにより治癒過程のモニタリングが可能である。
感染性角膜炎が原因の場合、病巣擦過物の塗抹検鏡と分離培養が必須である。抗菌薬が投与されていない状態で検体を採取することが理想的である。
フルオレセイン染料を用いて角膜からの房水漏出を確認する検査である。フルオレセインが房水で希釈されて流れ出す様子(陽性所見)はコバルトブルー光下で確認できる。角膜穿孔の確定診断に最も重要な検査の一つである。
治療法の選択は、穿孔のサイズ・範囲・部位・実質浸潤の程度・視力予後・基礎疾患に基づいて決定される。多くの場合、複数の治療が同時または段階的に行われる。
Tsengら(2024)は、眼GVHD続発のデスメ膜瘤に対しPROSE療法で7年間の非手術的管理に成功し、矯正視力20/50を維持したと報告した4)。oGVHDに伴う角膜穿孔の発生率は1〜4%と推定されている4)。
感染性角膜潰瘍が原因の場合、基礎疾患の感染制御が最優先である。
Che Ku Amranら(2024)は、淋菌性角結膜炎による角膜穿孔に対しシアノアクリレート接着剤+BCL+セフトリアキソン1g筋注で管理し、2か月後に感染制御を達成したと報告した5)。
| 穿孔サイズ | 推奨治療 |
|---|---|
| 3mm未満 | 組織接着剤またはAMT |
| 3mm超 | PKPまたはパッチグラフト |
| 全角膜 | 角膜強膜移植1) |
Kusanoら(2023)は、重度微生物性角膜炎により角膜全体がデスメ膜瘤となった症例(全角膜デスメ膜瘤)を報告した1)。前眼部OCTで角膜厚37μmを確認し、角膜強膜移植を施行して眼球保存に成功した1)。これは報告された中で最大のデスメ膜瘤とされる1)。
Shekhawatら(2022)は、傍中心角膜穿孔(1mm)に対しテノン嚢パッチグラフト+血管付き結膜弁を用いた術式を報告した3)。術後4か月で裸眼視力20/25を達成し、乱視は最小限であった3)。テノン嚢の線維芽細胞による旺盛な創傷治癒反応と、結膜弁による血管供給が治癒を促進した3)。この手技は角膜ドナー組織へのアクセスが限られる環境でも実施可能である3)。
Katoら(2021)は、金属異物による傍中心角膜穿孔(1mm)に対しone-bite mini-keratoplastyを施行し、術後矯正視力180/200、角膜乱視0.6ジオプターの良好な結果を報告した2)。17か月後の再穿孔にも同手技で対応し、2年以上良好な視機能を維持した2)。
穿孔が3mm未満で陥凹しており輪部から離れた位置にある場合は、シアノアクリレート接着剤が第一選択となりうる。接着剤は角膜移植(PKP)前の一時的措置としても有用である。3mm超の穿孔や前房が消失している場合、接着剤では対応困難であり、PKPが適応となる。治療法は穿孔のサイズ・部位・基礎疾患に基づき個別に判断される。
角膜穿孔は眼科的緊急疾患である。放置すると眼内炎・二次性緑内障・白内障・失明に至りうる。ただし全例が緊急手術を必要とするわけではない。小穿孔はBCLや接着剤で管理可能な場合があり、感染性穿孔ではまず抗菌薬治療を24〜48時間行ってからPKPを計画することもある。
角膜潰瘍は上皮欠損から始まり実質へ進行する。角膜実質の融解が深部に及びDMが露出するとデスメ膜瘤を形成し、さらにDMが破綻すると穿孔に至る。
緑膿菌による実験的角膜炎において、デスメ膜瘤の形成はアルカリプロテアーゼ・全プロテアーゼ・エラスターゼ活性と直接相関することが示されている1)。高プロテアーゼ産生株(102・115・118株)では、Ca²⁺・Mg²⁺存在下で少数の炎症細胞でも実質基質の大規模破壊・デスメ膜瘤形成・穿孔を誘導した1)。白血球プロテアーゼも角膜変性に関与するが、その存在のみでは必ずしもデスメ膜瘤形成には至らない1)。
DMは蛋白分解や生体力学的ストレスに抵抗性があるため、周囲の実質が融解しても一定期間は無傷を保つ1)。この特性がデスメ膜瘤という「穿孔前段階」を生む。しかし十分な張力強度を欠くため、最終的にはDMが前方にヘルニア状に膨隆する1)。
糸状菌は角膜表層にとどまらず深層へ向かって進行しやすい6)。菌糸がDMを破って角膜後面に到達すると角膜後面プラーク(endothelial plaque)を形成する6)。進行すると強い融解から穿孔に至る。
淋菌(Neisseria gonorrhoeae)は線毛を介して角膜上皮に付着・侵入する能力を有する5)。接種後1時間以内に上皮細胞内の空胞内に取り込まれ、24時間後には上皮厚が著明に減少する5)。この過程が上皮・実質・潰瘍性角膜炎を経て穿孔に至る5)。
テノン嚢パッチグラフトに血管付き結膜弁を組み合わせる手技が報告されている3)。結膜弁からの血管供給により従来のテノン嚢パッチグラフトよりも速い治癒(6週間で角膜実質厚の完全回復)が得られた3)。角膜ドナー組織が得られない低資源環境での有用性が期待される3)。
One-bite mini-keratoplastyは約1mmの小径穿孔に対し、単一の10-0ナイロン縫合で角膜グラフトを挿入する簡便な手技である2)。従来の層状角膜移植と比較して乱視の誘発が少ないとされる2)。
PROSE(Prosthetic Replacement of the Ocular Surface Ecosystem)療法は、手術ハイリスク患者におけるデスメ膜瘤の長期管理の選択肢として注目されている4)。角膜円蓋上に架橋する設計により角膜を保護し、持続的な潤滑と酸素供給を提供する4)。角膜拡張症においてはPROSE群が角膜移植群と比較して平均視力および視力回復速度で優位であったとの報告もある4)。