骨腫
頻度:FAP患者の60〜80%
好発部位:顎骨・副鼻腔・頭蓋骨
診断的意義:3個以上でGSを強く示唆。FAP診断に17年先行することがある

Gardner症候群(Gardner syndrome; GS)は、家族性大腸ポリポーシス(familial adenomatous polyposis; FAP)の表現型変異の一つである。大腸腺腫性ポリポーシスに加えて、骨腫・軟部組織腫瘍(デスモイド腫瘍)・表皮嚢胞などの大腸外病変を特徴とする。常染色体顕性遺伝(旧称:常染色体優性遺伝)形式をとる。
原因遺伝子はAPC(adenomatous polyposis coli)遺伝子で、第5染色体5q21に位置する。生殖細胞系列変異により発症し、子への遺伝確率は50%である。有病率は10万〜16万人に1人とされる4)。
FAPには以下のサブタイプがある1)。
FAPは全大腸癌の約1%を占める1)。大腸ポリープは10歳前後から出現し、数百〜数万個に達する。未治療では40歳で50%、60歳でほぼ全例が大腸癌を発症する。de novo変異(新生変異)は約20〜30%に認められる1)5)。
de novo変異(新生変異)がAPC遺伝子に約20〜30%の頻度で生じるため、家族歴がなくても発症しうる1)5)。家族歴がないからといってGSを除外できない点に注意が必要である。
大腸ポリープは通常無症状であり、発見が遅れることが多い。症状が出現する場合は以下が主体となる。
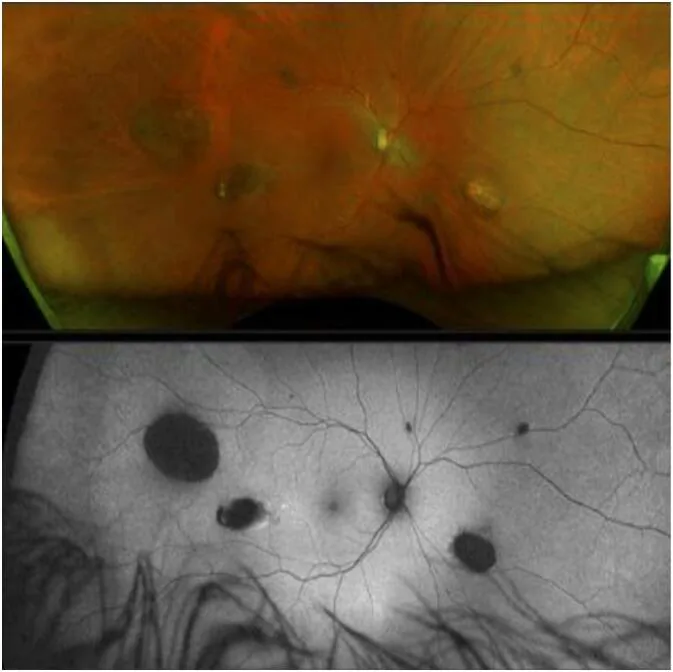
CHRPE(congenital hypertrophy of the retinal pigment epithelium)はGSの最も早期の大腸外徴候であり、出生時から存在する1)。
ただし、CHRPEが認められなくてもGSは否定できない2)。
骨腫
頻度:FAP患者の60〜80%
好発部位:顎骨・副鼻腔・頭蓋骨
診断的意義:3個以上でGSを強く示唆。FAP診断に17年先行することがある
CHRPE
頻度:FAP患者の74%
特徴:両側性・多発・えんどう豆状。出生時から存在する最も早期の徴候
注意:CHRPEなしでもGS否定不可
表皮嚢胞
頻度:約70%
好発部位:頭頸部
特徴:若年時から出現し、複数個認められることが多い
デスモイド腫瘍
頻度:FAP患者の12〜15%
好発部位:腹部(37〜50%)、次いで肩甲帯・胸壁
注意:FAP患者の死亡原因として大腸癌に次ぐ。死亡率10〜50%
FAP患者の30〜75%に認められる1)。埋伏歯・過剰歯(FAP患者の11〜27%に対して一般人口では0〜4%)がみられる1)。
大腸以外にも各種悪性腫瘍リスクが上昇する。
| 癌腫 | 生涯リスク |
|---|---|
| 甲状腺癌 | FAP 2〜12%、Gardner型10% |
| 小腸癌 | 4〜12% |
| 膵臓癌 | 約1% |
(出典:引用1)1)
孤発性のCHRPEは一般人口にも1.2〜4.4%の頻度で認められるため、CHRPEの存在だけでGSと断定することはできない。GS関連CHRPEは両側性・多発・えんどう豆状・不整境界を呈する点が特徴的である。逆に、CHRPEが認められなくてもGSは否定できない2)。
GSの原因はAPC遺伝子(5q21)の生殖細胞系列変異である。変異の大半はフレームシフトまたはナンセンス変異であり、切断型(機能喪失型)APCタンパク質が産生される。
変異部位と表現型には明確な相関がある1)。
| 変異部位 | 関連する表現型 |
|---|---|
| コドン311〜1444 | CHRPE |
| コドン767〜1578 | 骨腫 |
| エクソン1399以降 | デスモイド(800倍リスク) |
| コドン1309 | 20歳での早期大腸癌 |
変異クラスター領域(mutation cluster region; MCR)はコドン1250〜1464であり1)、最多変異はコドン1309(全体の約10%)、次いでコドン1061(約5%)である1)。大腸癌の発症年齢も変異部位によって異なり、コドン1309では20歳、コドン168〜1580では30歳前後、それ以外では52歳前後が目安となる1)。
APC遺伝子の分子遺伝学的検査は幼少期から実施可能である。大腸内視鏡検査は10歳前後からの開始が推奨されることが多い。家族内にAPC変異が判明している場合は、変異の有無を遺伝子検査で確認することが重要である。
確定診断にはAPC遺伝子の分子遺伝学的検査を行う。次世代シークエンシング(NGS)パネル検査が推奨される1)。
APC遺伝子の分子遺伝学的検査はGSの確定診断の根拠となるが、一部の患者では変異が検出されない場合もある。NGSパネル検査の活用により検出率は向上している1)。遺伝子検査の結果は臨床所見と組み合わせて総合的に判断する。
CHRPEそのものは悪性化せず、視機能への影響もない。眼科的介入は不要であり、定期観察のみ行う。
ポリープの増殖抑制を目的に、手術前や軽症例に使用される。
薬物療法単独で大腸癌のリスクを排除することはできない。
大腸切除は25歳までに行うことが推奨され、理想的には16〜20歳での施行が望ましい2)。主な術式は以下の3種類である2)。
直腸結腸全摘+永久回腸瘻
特徴:最も確実な術式。大腸上皮が残存しない
利点:大腸癌リスクを最大限に低減できる
欠点:永久ストーマが必要となり生活の質に影響する
回復的直腸結腸全摘+回腸嚢肛門吻合
特徴:腸管連続性を温存する術式
利点:永久ストーマを回避できる
欠点:泌尿器・性機能合併症のリスクがある
全大腸切除+回腸直腸吻合
特徴:侵襲が少なく、若年患者向き
利点:手術侵襲が比較的少ない
欠点:残存直腸のサーベイランスが継続的に必要
デスモイド腫瘍は組織学的に良性であるが、局所浸潤性が高く再発しやすい。治療は多職種による集学的アプローチを要する4)5)。
大腸切除後も以下のサーベイランスを継続する2)。
ポリープの数や異形成の程度によって異なる。少数のポリープであればNSAIDsやCOX-2阻害薬による薬物療法で経過をみることがある。しかし、20個以上や高度異形成ポリープが認められる場合は予防的切除が推奨される。理想的な手術時期は16〜20歳とされている2)。
APCタンパク質は2800アミノ酸からなる癌抑制因子である。主要なドメイン構造として、オリゴマー化領域・アルマジロリピート・β-カテニン結合領域・アキシン結合領域・微小管結合領域を持つ1)。
APC変異はWntシグナル伝達経路の恒常的活性化を引き起こす。正常なAPCタンパク質はβ-カテニンをリン酸化してプロテアソームでの分解を促進する。APC変異ではこの機能が失われ、β-カテニンが細胞質に蓄積し、核内でTCF/LEF転写因子と複合体を形成して細胞増殖遺伝子の転写を促進する。
変異の大半はフレームシフトまたはナンセンス変異であり、切断型(機能喪失型)APCタンパク質が産生される1)。
散発性デスモイド腫瘍では、CTNNB1(β-カテニン遺伝子)変異が75%以上に認められ、同様の経路が関与する3)。
CHRPEは網膜色素上皮の局所的な細胞増殖異常として生じる。網膜色素上皮が異常増殖した部分は色素が濃縮・肥大し、周囲のラクナ(脱色素化領域)とのコントラストで特徴的な外観を呈する。悪性化ポテンシャルはほぼなく、視機能への影響も認められない。
次世代シークエンシング(NGS)パネル検査により、APC遺伝子の変異部位の同定精度が向上している1)。遺伝子型と表現型の相関に基づくリスク層別化が進み、変異部位に応じた個別化サーベイランス・治療戦略の構築が期待されている1)。
Litchinkoら(2022)は、膵臓に発生した大型デスモイド腫瘍(170 mm)の稀な1例を報告した3)。多学科チームによる集学的管理が行われ、膵臓デスモイドにおける手術適応・タイミングの難しさを提示した。薬物療法としてソラフェニブの有効性が注目されており、外科切除が困難な症例への適用が検討されている。
高密度焦点式超音波(HIFU)の非侵襲的デスモイド治療への応用も研究段階にある3)。
Albuquerqueら(2025)は、肩関節機能再建を要した小児デスモイド腫瘍の1例を報告した5)。ビンブラスチン+メトトレキサートによる術前化学療法を含む集学的アプローチにより、機能温存と腫瘍制御を達成した。肩甲帯・胸壁デスモイドが全体の37〜50%を占めるとされ、小児例における機能再建の重要性を示している。
Diazら(2025)は、浸潤性基底細胞癌と全膝関節置換術合併例を含む外科的ジレンマを呈するGS症例を報告し、稀な合併症への集学的対応が求められることを示した4)。有病率が10万〜16万人に1人とされる本疾患において、個別化医療の重要性が増している。