黄斑上膜 (ERM)は網膜 内境界膜 (ILM)上に形成される線維細胞増殖組織であり、変視症 ・視力 低下の主要な原因となる。特発性(後部硝子体剥離 後)と続発性(裂孔・手術・外傷・炎症後)に大別される。
有病率は報告により2.2〜34.1%と幅があり、50歳以上で急増する。
多くは緩徐に進行し、自然剥離は3〜6%にとどまる。
OCT が最重要の診断・経過観察ツールであり、高輝度の膜状構造と網膜肥厚を描出する。手術(硝子体手術 +黄斑上膜剥離+ILM剥離)で73%の症例で視力が改善する。
合併症として術後PAMM 様網膜虚血やRPE 萎縮が報告されており、術前のインフォームドコンセントが重要である。
黄斑上膜(Epiretinal Membrane; ERM)は、網膜内境界膜(ILM)上に形成される線維細胞性の増殖組織である。黄斑 パッカー、セロファン黄斑症とも呼ばれる11) 。
黄斑上膜は特発性と続発性に分類される11) 。
特発性黄斑上膜 は後部硝子体剥離(PVD)に関連して発症し、50歳以上に多い。続発性黄斑上膜 は網膜裂孔 ・裂孔原性網膜剥離 ・眼内手術・外傷・網膜血管閉塞・ぶどう膜炎 などを契機とする。
有病率は検査法・対象集団によって異なり、2.2%(北京眼科研究、眼底写真基準)から34.1%(Beaver Dam Eye Study、SD-OCT基準)まで報告に幅がある11) 。米国では約3000万人が罹患していると推定される11) 。両側性は20〜35%に認められる11) 。民族差も報告されており、中国系39.0%、ヒスパニック29.3%、白人27.5%、黒人26.2%とされている11) 。
神経線維腫症 2型(NF2)では黄斑上膜有病率が80%に達する9) 。自然経過での自然剥離は3〜6%にとどまる4) 。
臨床的重症度の分類としてGass分類が広く用いられる。
グレード 所見 Grade 0 透明な薄膜(セロファン黄斑症) Grade 1 膜収縮による網膜皺襞 Grade 2 不透明な厚い膜
Q 黄斑上膜は必ず手術が必要ですか?
A すべての黄斑上膜が手術適応となるわけではない。無症状・症状が軽微・視力が良好な場合は経過観察が選択される。手術は通常、矯正視力0.7以下かつ変視症が強い場合に検討される。詳細は「標準的な治療法」の項 を参照。
黄斑上膜は無症状のことも多く、健診や他疾患の経過観察中に偶然発見される例も少なくない。症候性の場合は以下の症状を呈する。
変視症(ゆがみ) :直線がゆがんで見える。最も特徴的かつ患者が訴えやすい症状。視力低下 :膜の収縮・肥厚が進むにつれて生じる。小視症 :物が小さく見える。膜の牽引による黄斑変形が原因。単眼複視 :一方の眼で二重に見える。
細隙灯顕微鏡では黄斑部表面の光沢、網膜皺襞、血管蛇行が確認される。病変が進行すると黄斑浮腫 ・偽黄斑円孔 を呈することがある。
光干渉断層血管造影(OCTA )では中心窩 無血管野(FA Z)の形態変化が確認される。黄斑上膜を有する眼のFAZ面積は0.11 mm²であり、健常眼の0.24 mm²と比較して有意に狭小化している2) 。
黄斑上膜の最重要関連因子は後部硝子体剥離(PVD)である。PVD後に残存した皮質硝子体 がILMの裂開を引き起こし、グリア細胞・RPE細胞が硝子体腔へ遊走する。その後、線維芽細胞様細胞へ分化・増殖することで黄斑上膜組織が形成される11) 。
NF2関連黄斑上膜では免疫染色でGFAP弱陽性・ネスチン中等度陽性が確認されており、Müller細胞由来の成分が主体であることが示唆されている9) 。
主なリスク要因を以下に示す。
加齢 :50歳以上で急増し、75歳以上でさらに有病率が上昇する。後部硝子体剥離(PVD) :特発性黄斑上膜の最大の誘因。網膜裂孔・網膜剥離 :続発性黄斑上膜の主要原因。眼内手術歴 :白内障 手術・網膜剥離手術後に続発する。網膜血管閉塞・ぶどう膜炎 :炎症後の増殖反応として生じる。放射線治療 :プロトン線照射後の続発性黄斑上膜が報告されている3) 。
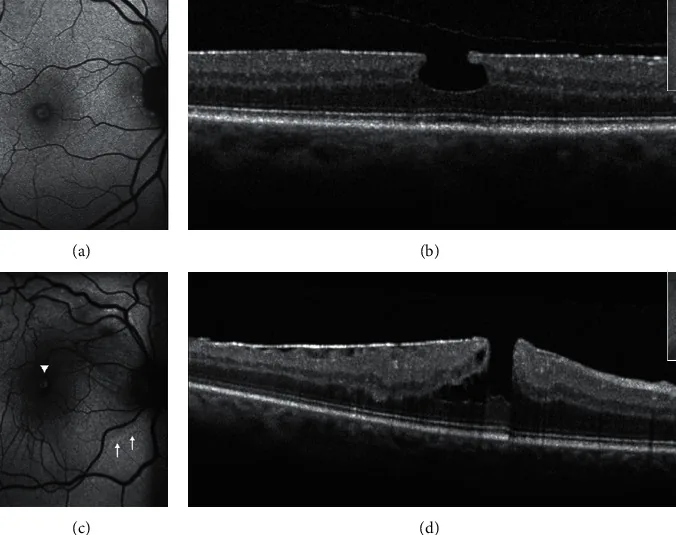
Epiretinal Membrane image Roberto dell’Omo; Mariaelena Filippelli; Serena De Turris; Andrea Govetto; Pasquale Napolitano; Ermanno dell’Omo; Ciro Costagliola. Multimodal Imaging of Lamellar Macular Holes. J Ophthalmol. 2021 Jan 30; 2021:8820444. Figure 4. PMCID: PMC7868145. License: CC BY.
Blue fundus autofluorescence (B-
FAF ) and optical coherence tomography images (OCT) in an eye with standard macular pseudohole (PSH) and in an eye with PSH with lamellar cleavage of its edges according to Gaudric et al. [14]. B-FAF (a, c): an increased autofluorescent signal is present at the fovea in both cases. On OCT (b), standard PSH is characterized by foveal centre sparing epiretinal membrane, retinal thickening, verticalised/steepened foveal profile, and near normal central foveal thickness. PSH with lamellar cleavage of its edges (d) shows in addition an intraretinal schisis. and has been reclassified as epiretinal membrane foveoschisis by Hubschman and coworkers [10].
各検査の役割をまとめる。
検査 主な目的 特徴 OCT 膜の描出・厚み評価 最重要・非侵襲的 OCTA 血管フロー評価 FAZ面積・新生血管 検出 眼底検査 表面光沢・皺襞確認 スクリーニング
**光干渉断層計(OCT)**が診断の中核をなす。黄斑上膜は網膜表面の高輝度膜状構造として描出され、網膜肥厚・内境界膜との癒着の有無が評価できる。術前のILM欠損の予測にはen face OCTが有用であり、22.7%の症例でILM欠損が術前に確認されている1) 。
**OCTA(光干渉断層血管造影)**では表層毛細血管網(SCP)の血管面積密度(VAD)の上昇が確認される2) 。黄斑上膜誘発性の網膜内新生血管の検出にも有用である6) 。
手術適応の判断基準 :矯正視力0.7以下かつ変視症が強い場合を手術適応の目安とする。症状の進行速度・患者の職業・生活への影響も考慮する。
Q 黄斑上膜の診断で最も重要な検査は何ですか?
A OCT(光干渉断層計)が最重要の検査である。網膜表面の高輝度膜状構造と網膜肥厚を非侵襲的に描出でき、診断・手術適応の判断・術後経過観察のすべてに活用される。
黄斑上膜治療の標準術式は経毛様体 扁平部硝子体手術(PPV )+黄斑上膜剥離+ILM剥離 である。現在は25G・27Gの小切開硝子体手術(MIVS)が主流であり、低侵襲・早期回復が可能となっている。
黄斑上膜剥離
目的 :牽引源となる増殖膜 を除去し、網膜形態を回復させる。
手技 :マイクロフォーセップス(鑷子)で黄斑上膜の端を把持して剥離する。
ILM剥離
目的 :黄斑上膜の再発を防ぎ、網膜のより完全な伸展を促す。
ILM欠損の対処 :術前en face OCTでILM欠損を22.7%の症例に認める1) 。欠損縁からの剥離手技が有用1) 。
視力改善率 :73%の症例で視力改善を認める11) 。視力改善の程度 :logMAR 0.4から0.1へ改善(術前後比較)2) 。変視症の改善 :術前56%が変視症を有し、術後は13%へ減少11) 。視力回復の経過 :術後3〜6ヶ月かけて徐々に改善する。術後12ヶ月まで緩徐な改善が続くことがある。
標準治療は手術であるが、以下の非手術的な自然剥離・誘発剥離の報告がある(いずれも症例報告レベル)。
デキサメタゾン硝子体内インプラント (DEX implant)7) 。抗VEGF+光線力学的療法 (PDT)後の自然剥離 :光線力学的療法施行後に黄斑上膜の自発的剥離が生じた症例が報告されている4) 。
これらは症例報告にとどまり、現時点での標準治療とはなっていない。
PAMM様網膜虚血 :黄斑上膜硝子体手術後に傍中心窩急性中間部黄斑症(PAMM)様の網膜虚血が生じる場合があり、視機能に影響する5) 。術前から血流状態を評価しておくことが重要である。RPE萎縮 :黄斑上膜・ILM剥離後にRPE萎縮が生じることがある。色素上皮の直接的な機械的損傷や光毒性が関与すると考えられている8)10) 。染色剤の安全性 :ILM染色に用いるブリリアントブルーG(BBG)は適切なプロトコールを遵守して使用する必要がある。エンドイルミネーション光との組み合わせによる黄斑障害の症例が報告されており、注意が必要である10) 。 Q ILM(内境界膜)剥離は必ず行う必要がありますか?
A ILM剥離は黄斑上膜再発防止のために有効であり、現在の標準手術に組み込まれている。術前のen face OCTでILM欠損が確認される場合(22.7%に存在)は欠損縁からの剥離手技が必要となる1) 。ただし技術的難度が高く、RPE萎縮などの合併症リスクとのバランスを考慮して判断する。
Q 手術後、視力はいつ頃回復しますか?
A 視力回復は術後3〜6ヶ月かけて緩徐に進行し、術後12ヶ月まで改善が続くこともある。術前の網膜変形の程度が回復の見通しを左右する。73%の症例で視力改善が得られる一方、一部では変視症が残存する場合がある11) 。
黄斑上膜の形成は以下の段階を経る創傷治癒様反応として理解されている11) 。
PVDと残存硝子体皮質 :PVDの際、一部の硝子体皮質がILM上に残存する。ILMの微小裂開 :残存した硝子体皮質の牽引によりILMに微小な裂け目が生じる。細胞の遊走 :ILM裂開部から網膜グリア細胞(Müller細胞・星状膠細胞)・RPE細胞・マクロファージが硝子体腔へ遊走する。増殖・線維芽細胞分化 :遊走した細胞が増殖し、線維芽細胞様の収縮性細胞へと分化して黄斑上膜を形成する。
血管への影響 :黄斑上膜による牽引はFAZ面積の縮小をもたらし、表層毛細血管網(SCP)のVADが有意に上昇する2) 。FAZ面積と最良矯正視力(BCVA)の間には有意な逆相関(r = −0.683)が認められており2) 、FAZ形態が視機能の重要な指標となる。
NF2に伴う黄斑上膜では、腫瘍抑制遺伝子の機能喪失によりMüller細胞様グリア成分が異常増殖して黄斑上膜を形成する。免疫染色ではGFAP弱陽性・ネスチン中等度陽性のパターンを示す9) 。
Frisina ら(2023)は特発性黄斑上膜眼においてFAZ面積が健常眼の約半分(0.11 mm² vs 0.24 mm²)に縮小し、SCPのVADが有意に上昇することをOCTAで確認した2) 。さらにFAZ面積とBCVAの間に有意な逆相関(r = −0.683)を報告し、OCTAが術前予後予測ツールとして有望であることを示した。logMAR視力は術後に0.4から0.1へ有意に改善した。
Sasajima と Zako(2023)は術前en face OCTで22.7%の症例にILM欠損を認め、ILM欠損縁からの剥離手技(defect-edge technique)が安全で有効であることを報告した1) 。術前に欠損部位を特定することで、手術計画の精度向上が期待される。
Giachos ら(2021)は糖尿病のない患者において黄斑上膜牽引が誘因となり網膜内新生血管が形成された症例を報告した6) 。OCTAにより血管の詳細な評価が可能であり、黄斑上膜手術後に新生血管が退縮することも確認された。
Venkatesh ら(2022)はBBGとエンドイルミネーション光の組み合わせによる黄斑障害の症例を報告し10) 、BBG使用時の露光時間制限と適切な光量管理の重要性を示した。安全な染色プロトコールの確立が今後の課題である。
Koiwa ら(2024)は黄斑上膜硝子体手術後にPAMM様の傍中心窩網膜虚血が生じた症例を報告し5) 、術前の血流評価と術中の眼圧 管理が合併症予防に重要であることを指摘した。
Sasajima H, Zako M. ILM peeling technique from ILM defect edge. Clin Case Rep. 2023;11:e7279.
Frisina R, et al. Vascular flow in idiopathic macular pucker. Eye. 2023;37:1470-1478.
Mashayekhi A, et al. Malignant ERM after proton beam radiation. J Ophthalmic Vis Res. 2023;18(4):445-451.
Munoz-Solano J, et al. Resolution of ERM after anti-VEGF+光線力学的療法. Am J Ophthalmol Case Rep. 2024;33:101994.
Koiwa C, et al. PAMM-like ischemia after ERM vitrectomy. Am J Ophthalmol Case Rep. 2024;36:102221.
Giachos I, et al. ERM-induced intraretinal neovascularization. Am J Ophthalmol Case Rep. 2021;23:101180.
Alshahrani ST, et al. ERM separation after DEX implant. Am J Ophthalmol Case Rep. 2022;25:101252.
Rivera-Valdivia N, et al. RPE atrophy after ERM/ILM peeling. Rom J Ophthalmol. 2022;66(1):79-83.
Kunikata H, et al. ERM in NF2: surgery and pathology. Digit J Ophthalmol. 2022;28:13-16.
Venkatesh R, et al. BBG+endolight macular damage. J Curr Ophthalmol. 2022;34:267-270.
AAO PPP. Idiopathic ERM and VMT PPP. Ophthalmology. 2020;127(2):P145-P183.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください