前眼部所見
結膜充血・角膜浮腫:炎症の活動期に認められる。
角膜後面沈着物(KP):肉芽腫性または非肉芽腫性。
前房細胞・フレア:炎症の程度を反映する。
虹彩後癒着:反復した炎症で形成される。
虹彩異色症:一部の症例で認められる。

エボラウイルス病(Ebola Virus Disease: EVD)は、フィロウイルス科(Filoviridae)エボラウイルス属に属するマイナス鎖一本鎖RNAウイルスによる人獣共通感染症である。致死率は平均約50%に達する。
急性期の眼症状として結膜充血(48〜58%)が知られているが、眼科的に問題となるのは主に感染後の後遺症である。EVD生存者に生じる多彩な症状は総称して**エボラウイルス病後症候群(post-Ebola virus disease syndrome: PEVDS)**と呼ばれる。PEVDSの症状には関節炎、難聴、神経精神障害が含まれるが、眼科的合併症は最も頻度の高い後遺症の一つである1)。
2013〜2016年の西アフリカでのアウトブレイクは28,000人以上の症例と約11,000人の死者を出した過去最大の流行であった。シエラレオネのEVD生存者112人を対象とした2024年の研究では、アウトブレイクから中央値8年後においてもぶどう膜炎が生存者の21%(23/112人)に認められ、眼疾患の負担が長期にわたって持続することが示された1)。
ウイルスは、免疫監視が及びにくい「免疫特権部位」のひとつである前房水から生きたウイルス粒子が分離された報告がある。涙液からは分離されていない。ウイルス血症が消失した後も眼内に持続感染が存在しうる。
PEVDS関連の眼症状は非特異的である。
PEVDSの眼所見は、過去の炎症または現在の炎症性変化として現れる。
前眼部所見
結膜充血・角膜浮腫:炎症の活動期に認められる。
角膜後面沈着物(KP):肉芽腫性または非肉芽腫性。
前房細胞・フレア:炎症の程度を反映する。
虹彩後癒着:反復した炎症で形成される。
虹彩異色症:一部の症例で認められる。
後眼部所見
硝子体混濁:炎症細胞の浸潤による。
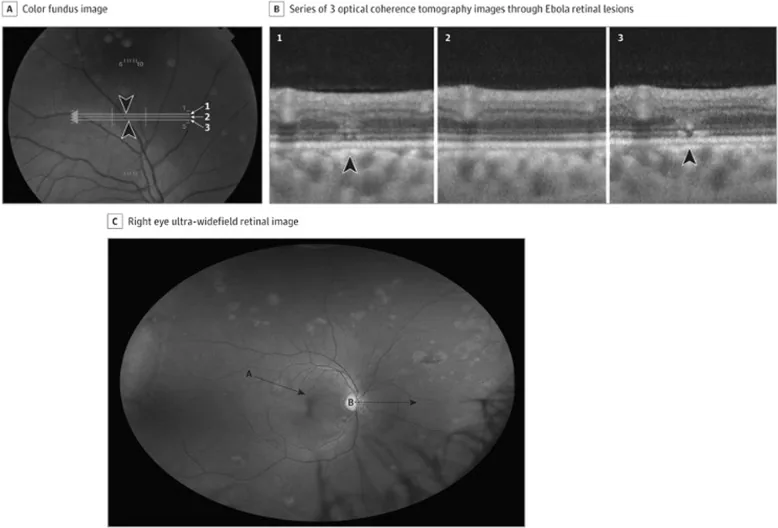
網膜病変:非色素性で、病変周囲に「dark without pressure」領域を伴う。視神経乳頭周囲病変は水平縫線に沿い中心窩を避けた湾曲を示す。
黄斑浮腫:視力低下の原因となる。
視神経乳頭浮腫:一部の症例で認められる。
牽引性網膜剥離・眼球癆:最重症例で生じる。
シエラレオネのコホート研究では、ぶどう膜炎が確認された眼の39%で視力が20/400(WHOの失明閾値)より不良であった1)。後部ぶどう膜炎(57%)と汎ぶどう膜炎(29%)が主な病型であった1)。また白内障(18%)、角膜瘢痕(9%)、視神経症(6%)が二次的合併症として認められた1)。
通常、EVDからの退院後3〜8週間で発症する。ほとんどの場合、片眼性かつ前部ぶどう膜炎として発症するが、後部や汎ぶどう膜炎も一定数みられる。また、感染から数年後においても眼疾患の負担が持続することが報告されている1)。
EVD後のぶどう膜炎発症のリスク因子には以下が含まれる。
ウイルスの免疫特権部位への持続感染も眼合併症の主要なメカニズムとして考えられている1)。エボラウイルスは前房水や精液を含む体液中に、全身のウイルス血症が消失した後も長期間持続しうる。
EVDが風土病となっているサハラ以南のアフリカ地域への旅行が最大のリスク因子である。医療従事者も感染リスクが高い。
PEVDS関連ぶどう膜炎の診断は、EVDの既往歴を持つ患者における眼内炎症所見の確認によって行われる。現在の文献では、前部ぶどう膜炎が最も頻度が高いとする報告が多数あるが、後部ぶどう膜炎が最多と報告する研究も存在する。
| 検査法 | 目的 |
|---|---|
| 眼底写真・OCT | 網膜病変・黄斑浮腫の評価 |
| フルオレセイン血管造影(FA) | 黄斑浮腫・血管炎の評価 |
| Bモード超音波 | 後眼部評価・硝子体混濁の評価 |
OCTでは外網膜層の異常が認められる。眼底写真では非色素性の網膜病変、病変周囲に「dark without pressure」領域を伴う所見が特徴的とされる。
シエラレオネのコホートでは、白内障手術予定の50人のEVD生存者の前房水・硝子体液・結膜サンプルを19ヶ月・34ヶ月の時点でRT-PCRにより検索し、すべてエボラウイルスRNA陰性であったことが確認されている。
感染後エボラぶどう膜炎の鑑別には幅広い炎症性・感染性原因を考慮する。
PEVDSの眼科的後遺症は、原因となる病態に応じて管理される。
治療は初診時の重症度に基づき段階的に行われる。
抗ウイルス薬(ファビピラビル経口投与)をステロイドと併用した報告があるが、疾患の解消に寄与したかどうかは不明である。現在までに、慢性エボラ関連ぶどう膜炎の管理において免疫調節薬が使用された報告はなく、その役割は不明である。
PEVDSにおける最も一般的な外科的介入は白内障手術である。EVD生存者の白内障は非常に高度であることが多く、合併症リスクが高い。手術中に生きたウイルス粒子と接触する可能性への注意が必要であり、適切な感染防御措置が必須である。
エボラウイルスは初期にマクロファージ・クッパー細胞・樹状細胞などの抗原提示細胞(APCs)に感染し、血液・リンパ系を通じて全身に播種される。その後、線維芽細胞・内皮細胞・肝細胞・副腎皮質細胞などにも感染が拡大する。
APCへのウイルス感染は免疫調節不全を引き起こし、大量の炎症性・血管拡張性ケモカインが放出される。最終的に内皮機能不全と凝固障害が低血圧・ショック・多臓器不全へとつながる。
眼においては、ウイルスが前房水などの免疫特権部位に持続的に潜伏することが眼科合併症の主要メカニズムとされる1)。前房水からは生きたウイルス粒子が分離されたことがあるが、涙液からは分離されていない。
Mandizadzaら(2024)のメタ解析では、エボラウイルスが免疫特権部位(精巣・中枢神経系・眼内液)に蓄積し、再活性化による炎症と直接的な組織障害を引き起こす機序が提唱された。ウイルスの眼内液・中枢神経系への持続感染が、眼科的症状と神経学的症状の原因となりうる1)。
また、急性感染時のエボラウイルスによる強力な免疫応答(サイトカインストーム)が組織損傷を残し、長期的な炎症の素地となる可能性も指摘されている1)。
2014年のアウトブレイクを受け、ワクチン開発が本格化した。2019年12月19日、米国FDAはrVSV-ZEBOVワクチン(商品名「エルベボ(Ervebo)」)を18歳以上の個人におけるEVD予防のために承認した。このワクチンの普及が、EVD後の眼科合併症発症頻度の将来的な低減につながる可能性がある。
コンゴ民主共和国のEVD患者を対象としたランダム化比較試験において、MAb114とREGN-EB3がZMappやレムデシビルよりも急性期治療において優れていることが示された。これらの治療法の普及が生存者の増加につながり、眼科的後遺症への対応がより重要な課題となる。
シエラレオネの研究では、EVDアウトブレイクから中央値8年後においても眼疾患の負担が持続することが示された1)。影響を受けた地域における長期的な眼科ケア体制の整備が、今後の重要な公衆衛生的課題として浮き彫りになっている。