ウイルス陽性メルケル細胞癌
メルケル細胞ポリオーマウイルス関連:全体の約80%。ウイルスオンコプロテインがRB1・p53を不活化。高い免疫原性を有し、T細胞標的治療の基盤となる1)。
細胞起源:真皮線維芽細胞、pro/pre-Bリンパ球、表皮前駆細胞など諸説あり1)。

メルケル細胞癌は、表皮基底層に存在するメルケル細胞に由来する稀な神経内分泌腫瘍である。メルケル細胞は1875年にFriedrich Merkelにより発見された感覚細胞で、軽い触覚や形状・質感の識別に関与する。
年間罹患率は人口10万人あたり0.23例である。頭頸部に全症例の約43〜50%が発生し、うち5〜10%が眼瞼に生じる1)。2000〜2013年にかけてメルケル細胞癌症例数は95%増加しており、全固形腫瘍(15%増)やメラノーマ(56%増)を大きく上回る速度で増加している1)。人口の高齢化、免疫抑制患者の増加、診断技術の向上が背景にある。
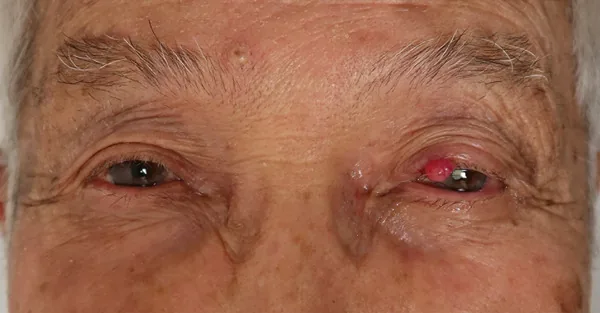
眼瞼では特徴的に睫毛部に発生し、赤く表皮が緊満して光沢がある。増殖速度が速くリンパ行性転移を生じやすいため、迅速な診断・治療が必要である。
年間罹患率は人口10万人あたり0.23例であり、皮膚悪性腫瘍の中でも稀である。ただし近年急速に増加しており、2000〜2013年で症例数が95%増加した1)。
メルケル細胞癌は通常無痛性であり、初期には自覚症状に乏しい。急速に増大する皮膚結節として気づかれることが多い。
メルケル細胞癌は多くの場合「紫色(violaceous)」の無痛性単発結節として現れる。診断の助けとしてAEIOU基準が提唱されている。
| 基準 | 内容 |
|---|---|
| Asymptomatic | 無症状(圧痛なし) |
| Expanding rapidly | 急速な拡大 |
| Immunosuppression | 免疫抑制状態 |
| Older than 50 | 50歳以上 |
| UV-exposed site | 紫外線曝露部位 |
メルケル細胞癌患者の89%が3つ以上の基準を満たし、52%が4つ以上を満たす。
眼周囲では上眼瞼の睫毛部付近に最も多く発生する。赤色調でドーム状に隆起する結節を形成し、拡張した腫瘍血管を伴う。部分的または完全な**睫毛脱落(madarosis)**や表面の毛細血管拡張が特徴的である。
診断時に最大37%にリンパ節転移、6〜12%に遠隔転移が認められる。耳前・顎下・頸部リンパ節の触診が不可欠である。
ウイルス陽性メルケル細胞癌
メルケル細胞ポリオーマウイルス関連:全体の約80%。ウイルスオンコプロテインがRB1・p53を不活化。高い免疫原性を有し、T細胞標的治療の基盤となる1)。
細胞起源:真皮線維芽細胞、pro/pre-Bリンパ球、表皮前駆細胞など諸説あり1)。
ウイルス陰性メルケル細胞癌
紫外線変異関連:高い変異負荷。紫外線によるDNAネオ抗原を発現し免疫原性が高い1)。
細胞起源:紫外線変異を多数持つ角化細胞/表皮前駆細胞から発生。扁平上皮癌との衝突腫瘍の報告あり1)。
メルケル細胞ポリオーマウイルスはほぼユビキタスなウイルスで正常皮膚にも存在するが、メルケル細胞癌に至るのは生涯で3000人に1人程度と極めて稀である1)。ウイルスゲノムの宿主への組み込みとラージT抗原の変異という2つの事象が同一細胞で生じる必要がある。
腫瘍細胞は乏しい細胞質を持ち、微細分散クロマチンを含む大型円形核と多数の核分裂像を示す。表皮下に大きな胞巣を形成する。一見リンパ腫に似るが、免疫染色で鑑別する。
| マーカー | メルケル細胞癌 | 小細胞肺癌 |
|---|---|---|
| サイトケラチン20(CK20、ドット状) | 陽性 | 陰性 |
| 神経特異エノラーゼ(NSE) | 陽性 | 陽性 |
| S-100 | 陰性 | 陰性 |
| TTF-1 | 陰性〜陽性 | 陽性 |
サイトケラチン20のドット状(核周ドットパターン)陽性がメルケル細胞癌に最も特徴的な所見であり、パンサイトケラチンとの共発現を示す2)。サイトケラチン20はメルケル細胞癌で100%陽性と報告される。電子顕微鏡では細胞質内に電子密度の高い芯を持つ神経内分泌顆粒が認められる。
臨床的にリンパ節転移のない患者でもセンチネルリンパ節生検により1/3で微小転移が同定される1)。センチネルリンパ節生検陽性患者は陰性患者と比較して再発リスクが約3倍(3年再発率: 60% vs 20%)であり、サーベイランス計画の決定に重要である1)。
FDG PET/CTによるベースライン画像で約6人に1人(16.8%)がアップステージされる1)。メラノーマ(<1%)と比較して潜在転移の頻度が著しく高い。
免疫組織化学染色が鍵である。サイトケラチン20の核周ドットパターン陽性はメルケル細胞癌に特異的であり、小細胞肺癌はサイトケラチン20陰性・TTF-1陽性を示す2)。
管理の基本は外科的切除と病理学的リンパ節評価である。体の他部位では1〜2cmの切除縁が推奨されるが、眼周囲では5mm程度の保存的切除縁が許容される2)。モース顕微鏡手術または凍結切片で切除断端の確認を行う。
眼瞼では脂腺癌に準じて眼瞼全層切除と再建術が必要となる。切除断端陰性を確認し、切除面に冷凍凝固(freeze and thaw)を2〜3セット追加する場合もある。
術後補助放射線療法
適応:NCCN(米国総合がん情報ネットワーク)ガイドラインでは全病期で外科切除後4〜6週以内の補助放射線療法を推奨。5年局所再発リスクを大幅に低下させる。
線量:通常50〜66Gy2)。眼周囲では眼構造への影響に注意。
根治的放射線療法
適応:手術適応のない患者に対する一次治療。メルケル細胞癌は放射線感受性が非常に高く、放射線単独でも治療される場合がある。
単回照射:8Gyの単回照射で94%超の奏効率。高齢・虚弱患者への代替選択肢1)。
従来のプラチナ製剤+エトポシドの化学療法は初期奏効率が高いが、奏効期間は短く(多くが90日以内に進行)、生存改善は示されていない1)。
免疫チェックポイント阻害薬が進行メルケル細胞癌の標準全身療法となっている:
一次治療としての奏効率は55〜62%であり、化学療法を大幅に上回る1)。化学療法と異なり奏効は持続的(数年間)であることが多い。ウイルス陽性・陰性いずれでも効果が期待できる。
メルケル細胞癌の発症には2つの主要な経路がある。
ウイルス陽性メルケル細胞癌では、メルケル細胞ポリオーマウイルスのオンコプロテイン(短縮型ラージT抗原・スモールT抗原)がRB1やp53を不活化し、Mycシグナルを活性化する1)。ウイルス陰性メルケル細胞癌では、紫外線誘発変異がこれらの経路を直接的に調節不全にする。両タイプとも「PARCB」因子(p53、Akt1、RB1、c-Myc、Bcl2の異常)が神経内分泌分化を駆動する1)。
メルケル細胞癌は不連続に拡散する傾向があり、病理学的に切除縁陰性であっても局所再発が生じうる1)。再発リスクを高める6因子として、1)慢性T細胞免疫抑制、2)腫瘍径>1cm、3)リンパ管侵襲、4)センチネルリンパ節生検陽性、5)切除縁陽性、6)頭頸部原発が報告される1)。
メルケル細胞ポリオーマウイルスのオンコプロテインに対する循環抗体の測定が予後指標として有用である。血清陰性患者は陽性患者より約42%再発リスクが高い1)。血清陽性患者では抗体価の推移が再発の早期検出に利用でき、NCCNガイドラインにサーベイランス法として採用されている1)。
術前(ネオアジュバント)の免疫チェックポイント阻害薬により、局所進行メルケル細胞癌の約50%で急速な腫瘍縮小が得られると報告される1)。症例ごとの検討が必要である。
進行メルケル細胞癌患者の約半数が抗PD-1/PD-L1療法に持続的な効果を得られない1)。一次耐性または獲得耐性への対応が最大の未充足ニーズであり、多くの臨床試験が進行中である。
循環腫瘍DNA(ctDNA)の解析がウイルス陰性メルケル細胞癌患者の再発早期検出に有望な新規ツールとして開発されている1)。病期別再発リスク計算ツール(merkelcell.org/recur)もサーベイランスの個別化に貢献している。