定義
病態:後期非滲出型加齢黄斑変性の病変。RPE・視細胞・脈絡膜毛細血管が境界明瞭に萎縮する。
別称:萎縮型加齢黄斑変性(atrophic AMD)。“dry AMD”はearly AMDを含む広義の用語で混同注意。

地図状萎縮(geographic atrophy; GA)は、後期加齢黄斑変性(AMD)の非滲出型として生じる疾患である。網膜色素上皮(RPE)・視細胞・脈絡膜毛細血管の境界鮮明な萎縮を特徴とする。3)
定義
病態:後期非滲出型加齢黄斑変性の病変。RPE・視細胞・脈絡膜毛細血管が境界明瞭に萎縮する。
別称:萎縮型加齢黄斑変性(atrophic AMD)。“dry AMD”はearly AMDを含む広義の用語で混同注意。
疫学
世界の罹患者数:約500万人(うち米国約100万人)1)
有病率:欧米での研究で0.66〜1.34%。85歳以上では滲出型AMDの4倍の頻度との報告もある。
自然経過
失明までの中央値:6.2年4)
進行パターン:中心窩周囲から始まり、馬蹄形→リング状と拡大。中心窩への進展は比較的遅い。
AMDの病期分類は以下の3段階である。2)
「黄斑萎縮(macular atrophy)」という用語は、2018年の国際ガイドラインにより、黄斑新生血管の有無にかかわらず境界明瞭な萎縮病巣に使用できる包括的な用語とされた。2)
GAは出血や滲出を伴わない萎縮性病変で、視力低下の進行は滲出型より緩徐である。一方、滲出型AMDは脈絡膜新生血管(MNV)が生じ、急激な視力低下をきたしやすい。3)GAの経過中にも10〜15%でCNVを発症し、その際は滲出型に対する治療が必要となる。
萎縮型AMDは変視・中心暗点に始まり、進行すると0.1未満の視力低下に陥る。50歳以上の男女(男性:女性=3:1)の片眼または両眼(40%)にみられる。
患者の約半数が急速な疾患進行を経験し、QOLに大きな負の影響をもたらす。1)
病変は中心窩周囲(旁中心窩)から始まり、馬蹄形→リング状と拡大し、中心窩へ進展する。4)
以下に主要な進行パラメータを示す。
| 指標 | 数値 |
|---|---|
| GA成長速度 | 1.28〜2.6 mm²/年 |
| 中心窩進入までの中央値 | 2.5年 |
| 対側眼のGA転換率(12ヶ月) | 30% |
| 対側眼のCNV転換率(12ヶ月) | 6.7% |
出典:3)4)
Anegondiら(2025)のランパリズマブ試験後向き解析(両眼性GA、2年間)では、2年間で平均最高矯正視力(BCVA)が66→57文字へ低下し、GA面積は8.07→12.05 mm²へ拡大した。1)中心1mm圏内のGAが視力低下と相関し、多病巣GAは単一病巣より成長速度が速い。3)
中心窩が保たれている間は高コントラスト視力はほぼ正常でも、GAは暗所感度・コントラスト感度・読書速度など「視力検査では測定されない機能」を早期から障害する。中心窩の外(旁中心窩)にもGAが及ぶと、読書や距離感知などの日常視機能が著しく低下する。3)
地図状萎縮はRPEとBruch膜の間に軟性ドルーゼンが蓄積し、RPEの変性萎縮が起こることから始まる。病態は複雑・多因子的で、炎症と補体経路が重要な役割を担う。1)
主なリスク要因は以下の通りである。
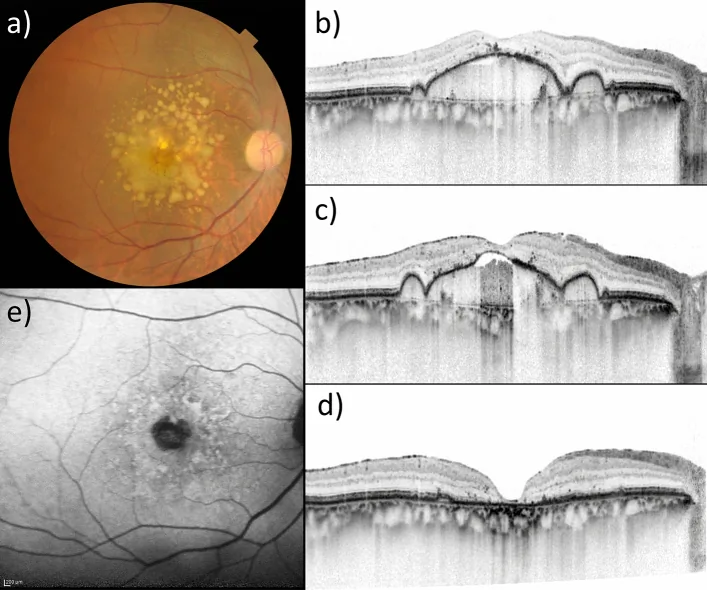
日本眼科学会(2015年)による萎縮型AMDの診断基準では、地図状萎縮に対して以下の必須所見が定められている。
| 項目 | 基準 |
|---|---|
| 大きさ | 直径250μm以上 |
| 形態 | 円形、卵円形、房状または地図状 |
| 境界 | 鮮明 |
| RPE変化 | 低色素または脱色素変化 |
| 脈絡膜 | 中大血管が明瞭に透見可能 |
診断は年齢50歳以上で、黄斑部の直径6,000μmの範囲内に地図状萎縮を認めることが要件となる。
| 検査法 | 評価内容 |
|---|---|
| 眼底自発蛍光(FAF) | 萎縮域の自発蛍光欠如。境界部の過自発蛍光が進行予測に有用 |
| OCT | 外層網膜の萎縮・RPEまたはBruch膜の反射低下・脈絡膜反射増強 |
| マイクロペリメトリ | 網膜感度測定。GAによる絶対暗点・感度低下を定量化 |
OCTでは「完全RPE・外層網膜萎縮(cRORA)」の分類が用いられ、臨床試験での主要評価項目にも設定されている。4)眼底自発蛍光で測定されるGA面積の変化は、多くの臨床試験で主要評価項目とされている。
RPE萎縮はさまざまな疾患で生じるため、以下の疾患との鑑別が必要である。
複数の研究で1.28〜2.6 mm²/年と報告されている。3)ただし個人差が大きく、多病巣性のGA・病変面積の大きいGAほど成長速度が速い。ランパリズマブ試験のデータでは2年間でGA面積が平均約50%(8.07→12.05 mm²)拡大した。1)
日本では、現時点で中心窩を含むGAが確立された症例に対する治療法はまだない。中心窩外GAに対しては、中心窩へのGA進展とCNV発生予防のため、ライフスタイル・食生活の改善とAREDS2サプリメントの摂取が勧められる。
AREDS2処方(ルテイン10mg+ゼアキサンチン2mg+ビタミンC500mg+ビタミンE400IU+亜鉛80mg)は、intermediate AMDから新生血管型AMD(中心窩を含む後期AMD)への進行リスクを約38%低下させる。ただし、GA進行そのものを抑制する効果は示されていない。
経過中にCNVを発症した場合(10〜15%)、抗VEGF薬による硝子体内注射が標準治療となる。
視力低下が進行した患者には、遮光眼鏡・拡大鏡などの視覚補助具の提案や、日常生活・就労支援などのロービジョンケアが重要である。
萎縮型AMDは、RPEとBruch膜の間に軟性ドルーゼンが蓄積・沈着することから始まる。ドルーゼンの構成成分には膜様残渣物・非エステル化コレステロール・補体などが含まれ、慢性炎症の起源となる。病態は複雑・多因子的であり、炎症と補体経路が中心的な役割を担う。1)
萎縮の進行は段階的である。5)
GAは中心窩周囲から始まることが多く、中心窩は萎縮に対して相対的な耐性を示す。4)これが馬蹄形・リング状のGA形状を生む。中心窩への進展は中央値2.5年かかるとされ、その間は高コントラスト視力が保たれる。
補体系の関与が強く示唆されており、CFH(補体因子H)Y402H変異やARMS2遺伝子多型がGAのリスクおよび進行と関連する。遺伝子多型とGA進行速度の関連が複数の研究で示されている。5)補体C3・C5を標的とした薬剤が開発されたのはこの機序に基づく。
GAの病態において、補体カスケードを介した慢性炎症がRPEと脈絡膜毛細血管の萎縮を促進することが示されている。1)CFHなど補体制御タンパクの遺伝子多型がGAリスクと強く関連することもこの仮説を支持している。5)補体C3を阻害することでC5以降の終末経路全体を抑制し、C5を阻害することで膜侵襲複合体(MAC)の形成を防ぐことで、組織傷害を抑制することが期待されている。
2023年に米国で2剤の補体阻害薬がGAに対してFDA承認された。日本では未承認であり、国内では使用できない。
ペグセタコプラン
機序:補体C3阻害薬(PEGylated C3阻害ペプチド)
用法:15mg/0.1ml、硝子体内注射、25〜60日毎
承認時期:2023年2月(米国FDA)。製品名SYFOVRE®
アバシンカプタドペゴル
機序:補体C5阻害薬(アプタマー)
用法:2mg、硝子体内注射、月1回
承認時期:2023年8月(米国FDA)。製品名Izervay®
ペグセタコプランの第III相試験OAKS(637名)・DERBY(621名)では、GA病変面積の進行を有意に抑制したが、2年時点で最高矯正視力・低輝度視力・読書速度・マイクロペリメトリー・NEI-VFQ-25のいずれの機能的評価項目も統計的有意差に達しなかった。アバシンカプタドペゴルの第III相GATHER 2試験(448名)でも24ヶ月時点の15文字以上の最高矯正視力喪失に有意差は認められなかった。すなわち、病変の解剖学的進行抑制が視機能の改善に直結しない「構造-機能乖離」が現時点の大きな課題である。
補体D因子阻害薬ランパリズマブの第III相CHROMA(906名)・SPECTRI(975名)試験はGA面積の抑制を示せず中止に至った。視覚サイクル阻害薬エミクススタトのSEATTLE試験(580名)も有効性を示せなかった。
現在のGA臨床試験では、最高矯正視力だけでなく、マイクロペリメトリによる網膜感度・低輝度視力(LLVA)・コントラスト感度・患者報告アウトカム(PRO)などの機能的エンドポイントが検討されている。4)最高矯正視力はGAの機能的影響を十分に捉えられないため、より包括的な評価指標の確立が求められている。
Dinahら(2025)のレビューでは、マイクロペリメトリ・低輝度視力(LLVA)・読書速度などが、最高矯正視力よりもGA患者の機能障害を鋭敏に反映するとして、今後の臨床試験での採用を推奨している。4)
RPE細胞の移植を用いた幹細胞治療が研究段階にあり、複数の試験が進行中である。遺伝子治療(補体因子を標的とする)も研究段階にある。
CFH・C3・ARMS2の遺伝子多型はGA発症リスクとは関連するが、疾患進行速度との関連は限定的との報告もある。5)一方、CFH・CFB・C3・FHR1-3・ARMS2の多型とFAFで測定されたGA成長速度の関連を示す研究もある。