RPE・網膜破壊型
代表薬剤:クロロキン(CQ)・ヒドロキシクロロキン(HCQ)・ペントサンポリサルフェート(PPS)
特徴:網膜色素上皮(RPE)の変性・崩壊。bull’s eye maculopathy(牛眼様黄斑症)を呈する。長期投与・高用量・腎疾患が主なリスク。

薬剤誘発性黄斑症(Drug-Induced Maculopathy)は、全身または局所に投与された薬剤が黄斑・網膜に直接または間接的に毒性を及ぼす病態の総称である。
毒性の機序・臨床パターンは原因薬剤によって異なる。以下の分類が概念整理に有用である。
RPE・網膜破壊型
代表薬剤:クロロキン(CQ)・ヒドロキシクロロキン(HCQ)・ペントサンポリサルフェート(PPS)
特徴:網膜色素上皮(RPE)の変性・崩壊。bull’s eye maculopathy(牛眼様黄斑症)を呈する。長期投与・高用量・腎疾患が主なリスク。
血管障害・直接毒性型
代表薬剤:ミトマイシンC(MMC)・セフロキシム・アミノグリコシド
特徴:不慮の眼内混入による血管閉塞・外層崩壊・網膜虚血。局所薬剤の誤注入・脈絡膜上腔遊走が原因となる。
免疫・炎症介在型
代表薬剤:免疫チェックポイント阻害薬(ICI;ニボルマブ・イピリムマブ)
特徴:VKH(Vogt-小柳-原田)様のpachychoroidal変化・漿液性網膜剥離(SRF)・BALAD(両眼急性局所滲出性網膜色素上皮症)。
その他の機序
代表薬剤:ジダノシン(DDI)・ガンシクロビル(GCV)・ネラチニブ・タモキシフェン
特徴:ミトコンドリア毒性(DDI)・高浸透圧結晶析出(GCV)・ERBB受容体介在性RPE脱分化(ネラチニブ)・結晶性網膜症(タモキシフェン)など多様。
多くは原因薬剤の中止で可逆的だが、一部では永続的・進行性の視力低下が生じる。初期は検眼鏡的に正常にみえることがあり、OCTや電気生理学的検査が診断に不可欠である。
クロロキン誘導体・免疫チェックポイント阻害薬・抗ウイルス薬(ガンシクロビル・ジダノシン)・抗癌剤(ミトマイシンC・ネラチニブ・タモキシフェン)・抗菌薬(セフロキシム)など多岐にわたる。原因薬剤によって毒性機序・臨床像・予後が大きく異なるため、使用薬剤を常に念頭に置いた診察が重要である。
原因薬剤によって特徴的な眼底所見が異なる。以下に主要薬剤の所見と可逆性をまとめる。
薬剤別の特徴的所見と可逆性を以下に示す。
| 薬剤 | 特徴的所見 | 可逆性 |
|---|---|---|
| CQ/HCQ | bull’s eye maculopathy | 不良(進行性) |
| MMC | 外層崩壊・血管閉塞 | 不良1)3) |
| ICI | pachychoroidal変化・SRF | 良好(中止+ステロイド)2) |
| GCV(高用量) | 全層高反射帯・EZ破壊 | 部分的4) |
| セフロキシム | SMD・ONL schisis様変化 | 良好(早期対応)7) |
| DDI | 中間周辺部色素性変化 | 不良(進行性)5)9) |
| ネラチニブ | MacTel type II類似像 | 不明8) |
各薬剤の詳細所見を以下に示す。
ミトマイシンC(MMC):trabeculectomy(線維柱帯切除術)中の不慮の硝子体内注入で、外層(IS/OS・EZ)崩壊および複数の区域性血管閉塞が生じる1)。脈絡膜上腔への遊走で区域性網膜障害が起こりうる3)。
免疫チェックポイント阻害薬(ICI):ニボルマブ・イピリムマブ投与後に、VKH様のpachychoroidal変化(脈絡膜厚505〜510μm)・SRF・BALADが報告されている2)。OCTで外層構造は比較的保たれ、免疫抑制療法への反応性が良好である。
ガンシクロビル(GCV)高用量硝子体内注射:全層にわたる高反射垂直帯・EZ(ellipsoid zone)破壊・神経網膜下液(NSD)が出現した症例が報告されている4)。反復投与では検眼鏡・OCT所見が正常でも、視野障害・多焦点網膜電図(mfERG)振幅低下が慢性的に蓄積する6)。
セフロキシム(前房内誤投与):黄斑下液(SMD)・外顆粒層(ONL)のschisis様変化をOCTで認める7)。早期の前房洗浄と抗炎症治療で良好な転帰が得られる場合がある。
ジダノシン(DDI):中間周辺部の色素性網膜症として発症し、黄斑を温存する9)。ABCA4変異を有する患者では毒性が重度となり、重篤な中心窩障害が生じうる5)。
ネラチニブ(TKI):黄斑毛細血管拡張症2型(MacTel type II)に類似した、内境界膜(ILM)draped外観・cavitationをOCTで呈した症例が報告されている8)。
視力低下・変視症・色覚異常・傍中心暗点・羞明・夜盲などが生じうる。初期には自覚症状が乏しく、OCTや視野検査で偶然発見されることもある。ジダノシン毒性では夜盲が先行することがある9)。
特定の遺伝子変異が薬剤性毒性のリスクを増大させることが明らかになっている。
投与開始時にベースライン検査を行い、5年目以降は年1回のスクリーニングが推奨される(AAOガイドライン)。腎機能障害・高用量・長期投与例はより早期・高頻度の検査が必要となる。詳細は「4. 診断と検査方法」を参照。
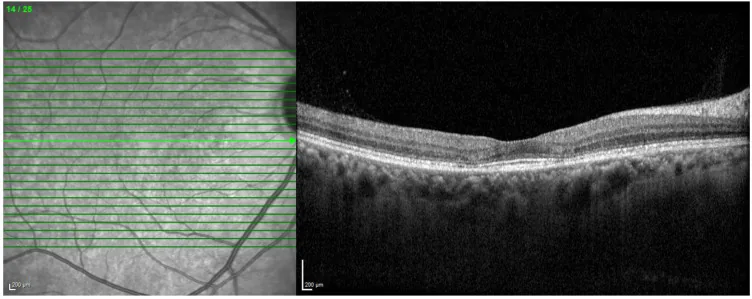
薬剤誘発性黄斑症の診断では、服用薬剤の把握と複数のモダリティを組み合わせた検査が重要である。
SD-OCT
適応:外層構造変化の高感度検出。全薬剤で第一選択。
所見:EZ破壊・外層崩壊・SRF・SMD・ONL変化1)4)7)2)。初期は正常にみえることがある。
眼底自発蛍光(FAF)
適応:RPE変化の非侵襲的検出。CQ/HCQ・DDIで有用。
所見:低蛍光域(RPE萎縮)・高蛍光域(RPE活性化)の分布3)5)。
網膜電図・視野
適応:機能的障害の定量評価。形態変化より早期に異常検出。
所見:mfERGはffERGより感度高い場合あり7)6)。Humphrey 10-2がCQ/HCQ監視に有用。
原因薬剤の中止が最重要かつ全例に共通する第一処置である。処方医との緊密な連携のもとで中止・変更を判断する。
薬剤別の治療基本方針を以下に示す。
| 原因薬剤 | 主な治療法 | 予後 |
|---|---|---|
| CQ/HCQ | 中止・代替薬検討 | 中止後も進行しうる |
| ICI | 中止+ステロイド全身投与2) | 良好(早期対応) |
| セフロキシム | AC洗浄+局所抗炎症7) | 良好(早期) |
| GCV | IVT中止+バルガンシクロビル4) | 部分的回復 |
| MMC | 硝子体手術考慮1)3) | 不良 |
| DDI | 中止+長期経過観察5)9) | 不良(進行性) |
イピリムマブを中止し、メチルプレドニゾロン1 g/日の点滴静注を開始する。報告例では投与2日で急速に改善し、ニボルマブ単剤での再開が可能であった2)。
22 mL BSS前房洗浄・局所ステロイド・NSAIDおよびデポメドロール40 mg結膜下注射の治療により、BCVAが0.02 logMAR(ほぼ正常)まで回復した報告がある7)。網膜電図は治療後も振幅低下が残存したが、視力予後は良好であった7)。
硝子体内注射中止とバルガンシクロビル900 mg/日の全身投与により、1ヶ月でOCT所見の改善が得られた報告がある4)。
不慮の硝子体内注入直後の硝子体切除術が考慮されるが、予後不良例が多い1)3)。脈絡膜上腔遊走例においても、視機能の実質的な回復は限定的である3)。
薬剤によって大きく異なる。ICIによる障害やセフロキシム誤投与では早期の適切な治療により良好な回復が期待できる2)7)。一方、クロロキン誘導体やジダノシンによる障害は中止後も進行しうるため、長期フォローアップが必要である5)9)。
メラニンへの結合→リソソーム内蓄積→pH上昇→リソソーム機能破壊→RPEおよび光受容体の変性というカスケードで毒性が発現する。
ミトコンドリアDNAポリメラーゼγ(pol-γ)を阻害し、ミトコンドリアDNA(mtDNA)合成を障害する。これによりRPE・光受容体のエネルギー代謝が破綻する5)。
Lenis ら(2022)は、CRB1変異を有する患者でDDI毒性への感受性が顕著に増大し、中間周辺部色素性変化が急速に進行した症例を報告した9)。CRB1は光受容体外節の構造維持に関与するタンパクであり、その機能喪失がDDI毒性の閾値を低下させると推察されている。
Nunziata ら(2026)はABCA4関連網膜症にDDI毒性が重畳した症例を報告した5)。ABCA4変異による既存のRPE脆弱性にDDI毒性が加わることで、通常よりはるかに重度かつ急速な黄斑障害が生じたとしている。
DNAに対する架橋形成が主機序である。動物実験では、0.4 mg/mLの硝子体内注射後、2日目にMüller細胞変性、4日目にRPE障害、7日目に外顆粒層(ONL)変性が観察された1)。脈絡膜上腔への遊走では、MMCが脈絡膜循環を通じて区域性に網膜へ到達し、局所的な血管閉塞と外層崩壊を引き起こす3)。
T細胞の免疫抑制解除→眼組織(RPE・脈絡膜メラノサイト等)への自己免疫反応→VKH様炎症という機序が想定される2)。pachychoroidal変化・SRF・BALADはいずれも脈絡膜・RPEへの免疫介在性障害を反映する所見と考えられる。
セフロキシムによるグルタミン酸トランスポーター1(GLT1)の過剰発現が、双極細胞周辺のグルタミン酸濃度を低下させ、網膜電図所見の変化を引き起こすと推察されている7)。
高用量では硝子体内での結晶析出による浸透圧障害が光受容体を傷害する可能性がある4)。低用量反復投与では、慢性的な光受容体外節変性が機能障害をもたらすと考えられている6)。
ERBB1/ERBB2受容体のチロシンキナーゼ阻害→mTORシグナル伝達異常→RPEの脱分化というカスケードが推察されている8)。MacTel type IIに類似した形態変化は、RPEと内境界膜の相互作用の破綻を反映する可能性がある。
変わりうる。CRB1変異はジダノシン毒性感受性を増大させ9)、ABCA4変異はジダノシンとの相乗的な黄斑障害をもたらすことが報告されている5)。遺伝性網膜疾患の患者に特定の薬剤を使用する際は、これらのリスクについて事前に評価・説明することが求められる。
DDI毒性とCRB1・ABCA4変異の関係は、薬剤使用前の遺伝学的スクリーニングによる個別化医療の可能性を示している9)5)。遺伝性網膜疾患の患者への薬剤投与前に遺伝子検査を行い、毒性リスクを予測する枠組みが今後発展すると期待される。
ICI使用患者では投与前のベースライン眼科検査を行い、経過中の変化を早期に把握する体制が推奨されている2)。新規ICI・ICI-TKI併用療法の普及に伴い、眼毒性の頻度・パターンの系統的な集積が求められる。
ネラチニブによるMacTel type II類似毒性は初めての報告であり8)、CYP3A4活性の個人差が毒性リスクを左右する可能性が示唆された。TKIの代謝酵素活性測定による毒性予測が今後の研究課題となる。
MMCの脈絡膜上腔への遊走が区域性網膜毒性をもたらすことが初めて詳細に報告された3)。手術中の薬剤管理・眼内圧制御が予防につながる可能性があり、さらなる検討が必要である。
単回高用量GCV注射での重篤な網膜毒性4)と、低用量反復投与での慢性障害6)の両方が報告され、硝子体内GCVの安全域の再評価が課題となっている。累積投与量・注射間隔・モニタリング法の標準化が今後求められる。