網膜内層ゾーン崩壊
網膜内層ゾーン崩壊(DRIL):内顆粒層・外顆粒層・神経線維層の境界が不明瞭になった状態。
予後意義:視力回復不良リスクが約8倍となる。血糖値や中心窩厚よりも視力と強く相関する。

糖尿病黄斑浮腫は、黄斑部における網膜内細胞外スペースへの過剰な液体貯留である。内顆粒層・外線状層・ヘンレ線維層・網膜下腔に液体が蓄積する。
糖尿病黄斑症には黄斑浮腫・虚血性黄斑症・網膜色素上皮症の3型があり、黄斑浮腫が最も頻度が高い。糖尿病網膜症(DR)は就労年齢成人の法的失明の主要原因であり、米国における糖尿病網膜症の有病率は28.5%(約420万人)、世界では34.6%(約9,300万人)と報告されている。6)
増殖糖尿病網膜症を含む視力を脅かす糖尿病網膜症の有病率は米国4.4%(約70万人)・世界10.2%(約2,800万人)、臨床的に意義のある黄斑浮腫の世界有病率は4.07%(約1,883万人)と推計される。10) 2020年時点の糖尿病網膜症患者数は世界1億312万人と推計され、2045年には1億6,050万人に増加すると予測されている。6)
糖尿病黄斑浮腫は非増殖期から増殖期まで、糖尿病網膜症のどの病期においても発生しうる。1型糖尿病では罹病25年間の発症率が約29%(WESDR)、インスリン使用2型糖尿病では25.4%、非使用例では13.9%と報告されている。
軽度の糖尿病黄斑浮腫では無症状のことも多く、定期眼底検査で偶発的に発見されるケースがある。黄斑虚血を合併した場合は視力低下・変視症がより顕著となる。
起こりうる。軽度の黄斑浮腫では視力が比較的保たれており、自覚症状がないことがある。糖尿病の方は症状の有無にかかわらず、定期的な眼科検査を受けることが重要である。
臨床的に意義のある黄斑浮腫(ETDRS基準) :以下のいずれかを満たすものと定義する。
光干渉断層計(OCT)所見 :糖尿病黄斑浮腫は3つの基本形態に分類される。9)
視力予後に関連するOCTバイオマーカー :
網膜内層ゾーン崩壊
網膜内層ゾーン崩壊(DRIL):内顆粒層・外顆粒層・神経線維層の境界が不明瞭になった状態。
予後意義:視力回復不良リスクが約8倍となる。血糖値や中心窩厚よりも視力と強く相関する。
外境界膜・楕円体帯
外境界膜・楕円体帯の破綻:光受容体の構造的完全性を反映するOCT層。
予後意義:破綻の程度は最高矯正視力(BCVA)と強く相関する。楕円体帯の修復は良好な視力回復に不可欠とされる。
その他の重要所見:
網膜内層ゾーン崩壊が視力回復不良リスクを約8倍高めるとされており、中心窩厚より強い予後指標である。外境界膜・楕円体帯の破綻も最終視力と強く相関し、楕円体帯の修復が良好な視力回復に必要とされる。詳細は「診断と検査方法」の項を参照。
糖尿病黄斑浮腫の根本原因は慢性高血糖による血液網膜関門の破綻である。高血糖が持続すると終末糖化産物が蓄積し、血管内皮細胞間接合部の破綻と周細胞消失が生じ、血管透過性が亢進する。7)
血液網膜関門には内側(網膜毛細血管内皮細胞)と外側(網膜色素上皮)の2層があり、糖尿病黄斑浮腫ではいずれも障害される。7)
高血糖による代謝異常として以下の経路が関与する。8)
主なリスク因子は以下の通りである。
DRCR Protocol W試験では、中心窩を含まない糖尿病黄斑浮腫に対するアフリベルセプト予防投与により、中心窩を含む糖尿病黄斑浮腫への進行が4.1%(対照群14.8%)に抑制された。しかし2年間の視力に有意差がなかったため、現時点で視力が良好な段階での予防的注射は標準治療ではなく、適応は個別に検討される。
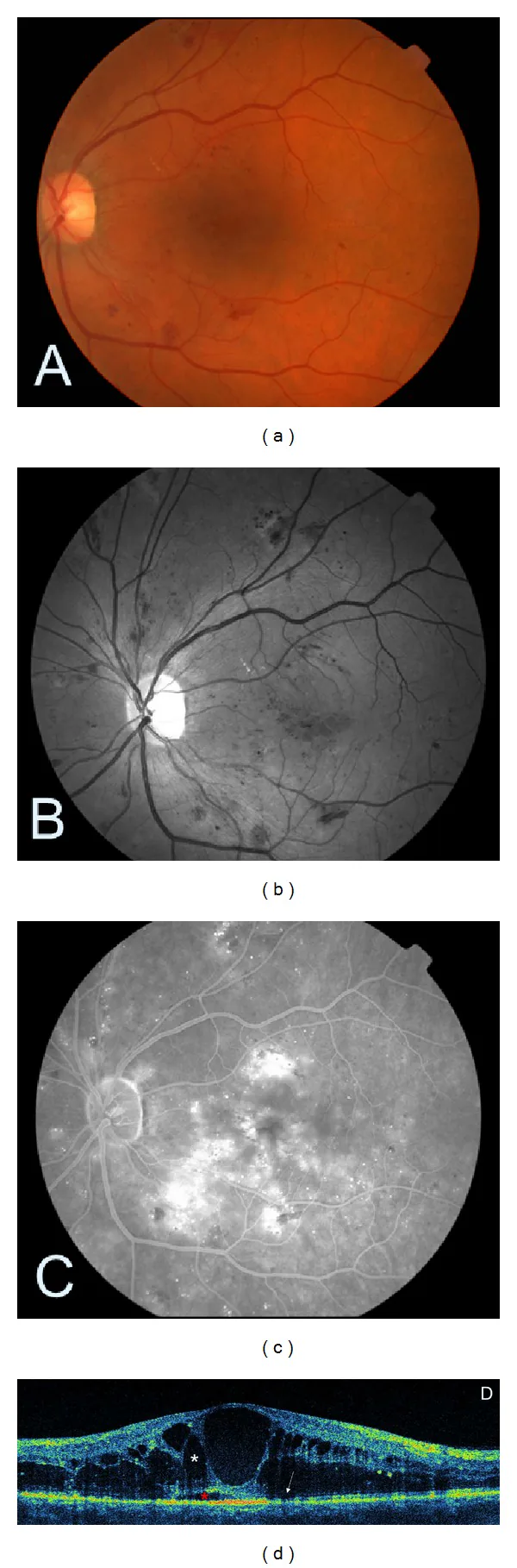
糖尿病黄斑浮腫の診断の中心的検査である。中心窩を含む型と含まない型の判別、中心窩厚の定量的評価、バイオマーカー(網膜内層ゾーン崩壊・外境界膜・楕円体帯・硝子体黄斑牽引)の評価に不可欠である。
OCT機種別の中心窩厚 治療閾値は以下の通りである。
| OCT機種 | 男性 | 女性 |
|---|---|---|
| Spectralis | 320μm | 305μm |
| Cirrus | 305μm | 290μm |
| Stratus | 250μm | 250μm |
DRCR Networkの解析では、中心窩厚が100μm減少するごとに視力が約4.4文字改善することが示されている。
漏出性毛細血管瘤の同定と虚血領域の特定に有用である。抗VEGF治療の普及に伴い使用頻度は低下しているが、黄斑虚血の評価や治療抵抗例では今なお重要な検査である。
類似した黄斑浮腫を呈する疾患との鑑別が必要である。
抗VEGF薬が糖尿病黄斑浮腫の第一選択治療である。日本で承認されている主な薬剤を以下に示す。
| 薬剤名 | FDA承認年 | 特徴 |
|---|---|---|
| ラニビズマブ | 2012年 | Fab断片、0.5mg/0.05mL |
| アフリベルセプト | 2014年 | VEGF-A/B・PlGF結合融合蛋白、2mg/0.05mL |
| ブロルシズマブ | 2022年 | 最小分子量26kDa一本鎖抗体 |
| ファリシマブ | 2022年 | Ang-2/VEGF-A二重特異性抗体 |
日本における標準投与プロトコールは以下の通りである(教科書)。
DRCRアルゴリズムでは、視力20/20以上かつ中心窩厚閾値未満になるまで毎月注射を6回施行する。6)
ブロルシズマブの難治性糖尿病黄斑浮腫への応用 :
ブロルシズマブは分子量26kDa(既存最小の抗VEGF薬)であり、アフリベルセプトの約4分の1の分子量、12倍のモル投与量を可能にする。2)
Chakraborty Dら(2021)は、既存の抗VEGF薬(ベバシズマブ・ラニビズマブ・アフリベルセプト・デキサメタゾンインプラント)で効果不十分だった難治性糖尿病黄斑浮腫3眼に対し、ブロルシズマブ6mgの適応外投与を行い報告した。最高矯正視力20/60→20/25等の改善が12週まで持続し、16週で再発を認めた。2)
KESTREL/KITE試験では、ブロルシズマブ6mgがアフリベルセプトに対して非劣性を示し、50%以上の患者がq12w(12週ごと)の投与間隔を維持できた。5)
抗VEGF薬に治療抵抗性を示す症例や、硝子体手術後・白内障術後の黄斑浮腫に用いる。
硝子体黄斑牽引を合併した糖尿病黄斑浮腫では硝子体牽引の解除が有効である。内境界膜剥離を伴う25G硝子体手術が標準的手技とされる。
巨大毛細血管瘤の外科的摘出 :
Tanakaら(2025)は、中心窩近傍の巨大毛細血管瘤(TelCaps)を有する治療抵抗性糖尿病黄斑浮腫3眼に対し、27G硝子体手術で内境界膜剥離後に巨大毛細血管瘤を摘出し、さらにレーザー凝固を施行した。最高矯正視力20/100→20/33への改善を報告しており、巨大毛細血管瘤を有する糖尿病黄斑浮腫の新たな外科的アプローチとして提唱されている。1)
他の抗VEGF薬への変更(スイッチ療法)、ステロイド(トリアムシノロン・デキサメタゾンインプラント)の追加・切り替え、蛍光眼底造影ガイド下のレーザー併用などを検討する。光干渉断層計で硝子体黄斑牽引の合併が確認された場合は硝子体手術が有効であり、巨大毛細血管瘤を認める場合は外科的摘出が選択肢となる。1)
内側の血液網膜関門は網膜毛細血管内皮細胞の密着結合(タイトジャンクション)・アドヒアレンスジャンクションによって構成される。外側の血液網膜関門は網膜色素上皮細胞間の密着結合で形成される。7)
慢性高血糖によって以下の機序で血液網膜関門が破綻する。7)
周細胞(pericyte)のアポトーシスは糖尿病網膜症の最早期変化の一つであり、内皮細胞増殖の制御が失われ異常血管新生が生じる。7)
グリコカリックスは血管内皮表面を覆う糖衣構造である。高血糖によって剥離が生じると、ICAM-1発現上昇と粘膜類天疱瘡-9/粘膜類天疱瘡-2の活性化により白血球接着が促進され、炎症が増幅される。7)
高血糖下で活性化される4つの代謝経路すべてにおいて活性酸素種が産生され、酸化ストレスが血管障害を増幅させる。8)
白血球停滞・赤血球変形能低下が毛細血管閉塞を引き起こす。閉塞が不可逆的になると低酸素誘導因子(HIF-1α)が誘導され、VEGFのさらなる亢進と新生血管形成が促進される。
Tanakaら(2025)は、中心窩近傍の巨大毛細血管瘤(150μm超の拡張毛細血管瘤)が抗VEGF治療抵抗性の主因となることを示し、27G硝子体手術による内境界膜剥離と巨大毛細血管瘤の直接摘出・レーザー凝固の3ステップ手技を報告した。巨大毛細血管瘤関連の糖尿病黄斑浮腫の多施設前向き比較試験(TalaDME試験)が進行中であり、このアンメットニーズへの対応が期待されている。1)
Chakrabortyら(2022)は、片眼へのブロルシズマブ6mg硝子体内注射後、未投与の対側眼において中心窩厚が15.26%減少したことを報告した。ブロルシズマブの分子量が26kDaと小さいため全身循環に移行しやすく、対側眼の網膜血管に影響を与えた可能性が示唆される。薬物動態のさらなる解明が課題である。3)
Kikuchiら(2022)は、アフリベルセプト2mg×22回(総44mg)投与を受けた糖尿病患者において腎血栓性微小血管症およびネフローゼ症候群が発症し、投与中止後6か月で改善したことを報告した。著者らは腎生検で確認された18例を含む系統的分析を行い、長期投与・糖尿病性腎症の背景を持つ患者での腎毒性リスクを指摘している。4)
Hiranoら(2023)は、ブロルシズマブ投与後に網膜動脈閉塞性血管炎を発症した糖尿病黄斑浮腫の症例を報告した。糖尿病黄斑浮腫眼は糖尿病網膜症自体に炎症成分があるため眼内炎症の診断が困難であり、レーザーフレアセルメーターや広角眼底撮影を用いた早期検出体制の構築が課題として挙げられている。5)
Tanaka H, et al. Surgical management of foveal telangiectatic capillaries in diabetic macular edema. Cureus. 2025;17(8):e91026.
Chakraborty D, et al. Off-label intravitreal brolucizumab for recalcitrant diabetic macular edema: a case series. Am J Ophthalmol Case Rep. 2021;24:101197.
Chakraborty S, Sheth JU. Contralateral effect following intravitreal brolucizumab injection in diabetic macular edema. Case Rep Ophthalmol Med. 2022;2022:3755249.
Kikuchi Y, et al. Renal thrombotic microangiopathy induced by intravitreal aflibercept for diabetic macular edema. BMC Nephrology. 2022;23(1):348.
Hirano T, et al. Retinal arterial occlusive vasculitis after brolucizumab injection for diabetic macular edema. Am J Ophthalmol Case Rep. 2023;29:101788.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. AAO. 2024.
O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEBS J. 2023;290(4):878-891.
Yang S, et al. The cells involved in the pathological process of diabetic retinopathy. Chin Med J. 2020;133(22):2579-2585.
(著者未詳)Diabetic macular edema: OCT classification and blood-retina barrier review. Eur J Pharmacol. 2024.
(著者未詳)Global epidemiology of diabetic retinopathy. Front Endocrinol. 2025;16:1664604.