血管性
糖尿病網膜症:最多原因。血管内皮増殖因子(VEGF)関与。
網膜静脈閉塞:分枝/中心静脈閉塞ともに高頻度。
動脈閉塞(CRAO):急性期は外顆粒層、慢性期は内顆粒層に局在。3)

嚢胞様黄斑浮腫(Cystoid Macular Edema; CME)は、血液網膜関門(blood-retinal barrier; BRB)の破綻によって黄斑部(中心窩周囲)の毛細血管から液体が漏出し、外網状層・内顆粒層を中心に嚢胞様の液体貯留を来す病態である。嚢胞隔壁はMüller細胞と神経軸索線維から構成され、Henle線維層に沿って液体が貯留することで特徴的な花弁状パターンを形成する。
先進国における中心視力障害の主要原因の一つであり、多彩な眼疾患・全身疾患・薬剤が原因となりうる。CMEには病態から3つの基本メカニズムが存在する:①滲出性(BRB破綻による血管漏出)、②変性性(Müller細胞障害による細胞内液体貯留)、③牽引性(硝子体黄斑牽引・網膜前膜による機械的変形)である。3)
OCTにおける液体の層別局在が原因推定の手がかりとなる。内顆粒層限局は変性性機序を、外顆粒層限局は急性Müller細胞浮腫または牽引性を、両層にわたる分布は滲出性を示唆する。3)
多くは3〜4ヶ月以内に自然消退する。ただし慢性化(6〜9ヶ月以上)すると光受容体の永久損傷が生じうる。原因の特定と適切な治療介入が重要であり、詳細は「標準的な治療法」の項を参照されたい。
蛍光眼底造影(FA)での漏出の程度は、視力低下の程度と必ずしも相関しない。
細隙灯顕微鏡での中心窩反射消失が初期の重要所見である。中心窩厚≧300μmになると臨床的に有意な浮腫として認識される。緑色光(無赤色光)照射で嚢胞の輪郭が強調される。
眼底では中心窩を中心に花弁状配列の嚢胞が形成され、蜂の巣状パターンとして観察されることが多い。高度例では嚢胞の融合により大嚢胞を形成する。
CMEの主要な原因は「DEPRIVENS」の語呂合わせで整理される:Diabetes(糖尿病網膜症)、Epinephrine(エピネフリン)、Pars planitis(中間部ぶどう膜炎)、Retinitis pigmentosa(網膜色素変性)、Irvine-Gass syndrome(白内障術後)、Vein occlusion(静脈閉塞)、Nicotinic acid(ニコチン酸)、External beam radiation(放射線)、Surgery(手術)。
白内障手術後CMEは最も頻度が高い術後CMEである。IOL挿入眼の最大20%で発症するが、視力低下を伴うのは1〜20%とされる。後嚢破損は高リスク因子である。発症は術後6〜10週が多く、95%が6ヶ月以内に自然消退する。黄斑円孔術後のCME発症率は10%未満である。14)
以下の薬剤による報告が蓄積している。
| 薬剤 | 適応 | 特徴 |
|---|---|---|
| ラタノプロスト | 緑内障 | 有水晶体眼でも発症。22年使用後の初報告あり1) |
| フィンゴリモド | 多発性硬化症 | 0.5mgで ME 0.4%。白内障手術がトリガーに8) |
| シポニモド | 多発性硬化症 | EXPAND試験でCME 2%。開始1週で発症4) |
| Nab-パクリタキセル | 乳癌 | FA漏出なし(Müller細胞毒性)2) |
| イブルチニブ | 慢性リンパ性白血病 | 中心窩網膜厚 600μm。中止6ヶ月で消退7) |
| ペントサンポリ硫酸(PPS) | 間質性膀胱炎 | 中止10年後にも発症。黄斑症の17%に合併10) |
プロスタグランジン関連薬(PGA)は血液房水関門を障害してCMEを誘発する。ラタノプロストに関するWarwarらのレビューでは94名中2.1%がCMEを発症し、Huらのレビューでは48眼中47眼が偽水晶体眼または無水晶体眼であった。1)有水晶体眼での発症は稀だが、22年にわたる長期使用後の発症例も報告されている。1)
血管性
糖尿病網膜症:最多原因。血管内皮増殖因子(VEGF)関与。
網膜静脈閉塞:分枝/中心静脈閉塞ともに高頻度。
動脈閉塞(CRAO):急性期は外顆粒層、慢性期は内顆粒層に局在。3)
炎症性
ぶどう膜炎:IRUはCMEリスク20倍。5)
術後炎症:白内障・緑内障・硝子体手術後。
デバイス合併症:Hydrus屈曲→虹彩炎→CME。9)
薬剤性
PGA点眼:有水晶体眼でも発症しうる。1)
S1P受容体調節薬:フィンゴリモド・シポニモド。4)8)
抗癌剤:タキサン系・BTK阻害薬・PPS。2)7)10)
術後/牽引性
IOL挿入眼の最大20%でCME(Irvine-Gass症候群)が生じるが、実際に視力低下を来すのは1〜20%とされる。後嚢破損がある場合はリスクが高まる。95%は術後6ヶ月以内に自然消退するが、高リスク例への予防的NSAIDs投与が推奨されている。12)
フィンゴリモド・シポニモド(多発性硬化症治療薬)、Nab-パクリタキセル(抗癌剤)、イブルチニブ(血液がん治療薬)、ペントサンポリ硫酸(間質性膀胱炎治療薬)などで報告されている。原因薬の中止が最も効果的な治療であり、詳細は「標準的な治療法」の項を参照されたい。
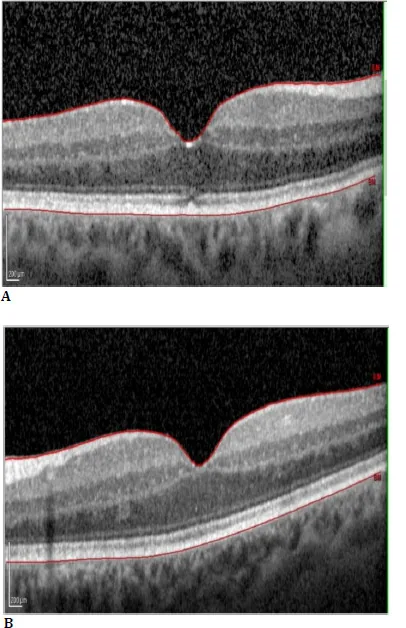
CMEの診断には複数の画像検査が用いられる。以下に主要な検査法を示す。
| 検査法 | 特徴 | 主な用途 |
|---|---|---|
| OCT | 非侵襲・定量評価 | 確定診断・治療効果判定 |
| 蛍光眼底造影(FA) | 造影剤使用 | 漏出パターン確認 |
| 眼底自発蛍光(FAF) | 非侵襲 | RPE障害評価 |
最重要の検査法。嚢胞の位置・分布・網膜厚の定量評価が可能であり、治療効果の経時的モニタリングに不可欠である。CMEの基本的OCT所見には3型が存在する:①網膜膨化(びまん性)、②嚢胞様浮腫(嚢胞形成)、③漿液性網膜剥離。
層別局在は原因推定に有用であり、内顆粒層限局は変性性機序を、外顆粒層限局は急性Müller細胞浮腫を示唆する。3)En face OCTはCMEの分布パターン可視化に有用である。3)
治療反応性のOCTバイオマーカーに関する系統的レビューでは、以下が示されている。13)
網膜下液は67%の症例で改善、網膜内嚢胞は76%で改善する一方、EZ(楕円体帯)障害は64%が不変または悪化、ELM(外境界膜)障害は67%が不変または悪化、高反射fociは63%が不変または悪化、DRIL(disorganization of retinal inner layers)は50%が不変または悪化した。13)
EZ・ELM障害の存在は治療後も視機能回復が不良であることを示す予後不良バイオマーカーである。13)
後期相(10〜20分)でHenle線維層に沿った花弁状漏出が特徴的。ただしタキサン系抗癌剤誘発CMEではFA漏出が見られないことが多く(変性性機序による)、FA陰性でもCMEを否定できない。2)
ペントサンポリ硫酸(PPS)関連黄斑症では特徴的なFAF異常パターンが認められ、当初AMDと誤診されやすい。10)CMEそのものよりもRPE障害の評価に有用である。
嚢胞の位置・分布・大きさ、網膜厚の定量評価が可能で、治療効果の経時的判定に不可欠である。層別局在(内顆粒層か外顆粒層か)が原因推定の手がかりとなる。EZ・ELM障害は視機能予後に影響するバイオマーカーとして評価される。13)
治療は原因疾患と病態に応じて選択する。薬剤性CMEでは原因薬の中止が第一選択である。
ケトロラク0.5%、ネパフェナク0.1%、ブロムフェナク0.07%などが使用される。シクロオキシゲナーゼ(COX)阻害によりプロスタグランジン産生を抑制し、BRBを安定化させる。
術後高リスク眼(後嚢破損・単眼・糖尿病例など)へのNSAIDs周術期予防投与が推奨されている。術前投与開始と術直後からの継続投与が視力回復を促進する。12)
Hydrus Microstent屈曲によるCME症例ではケトロラク+プレドニゾロン点眼2ヶ月で完全消退(視力20/60→20/25)が報告されている。9)
ステロイドはMüller細胞のアデノシンシグナルを刺激してVEGF産生を低下させる機序が示唆されている。なお、IRU関連CMEにおいて大腿骨頭壊死などでステロイドが禁忌の場合はトシリズマブが代替となりうる(後述)。
糖尿病黄斑浮腫・RVO関連CMEの主要治療。ベバシズマブ1.25mg/0.05mL、ラニビズマブ0.5mg、アフリベルセプト2mgなどが使用される。
ベバシズマブ1.25mg/0.05mLの2回投与により、PPS関連CMEが完全消退した症例が報告されている。NSAIDs・ステロイド点眼が無効であった当該症例において良好な転帰が得られた。10)
高ホモシステイン血症を伴う両眼静脈うっ滞・CME症例でも抗VEGF 2回投与で改善が得られている。6)
RPEポンプ機能を増強し網膜下液の吸収を促進する。点眼(ドルゾラミド、ブリンゾラミド)または内服(アセタゾラミド)で投与される。ラタノプロスト誘発CMEにおいて、ラタノプロストをドルゾラミドへ切り替えることで1ヶ月以内の消退が報告されている(CMT 319→218μm、326→227μm)。1)
薬剤性CMEでは原因薬の中止が最も効果的な治療である。
VMTを伴う牽引性CMEでは硝子体切除術により80〜92%でCMEが改善する。オクリプラスミン(酵素的硝子体剥離薬)は第2・3相試験で58%に1ヶ月以内のVMT解除をもたらすことが示された。
原因に応じてNSAIDs点眼、ステロイド(テノン嚢下/硝子体内注射)、抗VEGF硝子体内注射、炭酸脱水酵素阻害薬、硝子体手術などが選択される。薬剤性CMEでは原因薬の中止が最も効果的な第一選択治療である。治療法の詳細は「標準的な治療法」の項を参照されたい。
BRBは2層構造から成る。内側BRB(網膜血管内皮細胞間のタイトジャンクション)と外側BRB(網膜色素上皮細胞間のタイトジャンクション)が網膜の水分恒常性を維持する。炎症・虚血・毒性物質などによりタイトジャンクションが弱化すると血清蛋白・脂質が漏出し、浸透圧上昇が生じる。11)
Müller細胞はaquaporin-4とKir4.1チャネルを用いた排水機構により、正常では液体の貯留を防いでいる。BRB破綻が高度になるとこの代償排出機構が飽和し、CMEが顕在化する。11)
滲出性
BRB破綻:血管内皮・RPEタイトジャンクション弱化。
液体成分:血清蛋白・脂質の漏出。FAで花弁状漏出を認める。
代表疾患:糖尿病網膜症、RVO、ぶどう膜炎。11)
変性性
Müller細胞障害:タキサン系・CRAO慢性期。
特徴:FA漏出なし。内顆粒層に限局しやすい。2)3)
例:Nab-PTX誘発CME、CRAO 28ヶ月後の内顆粒層CME。
牽引性
機械的変形:VMT・ERMによる。
特徴:外顆粒層に多い。硝子体手術で改善。
治療:硝子体手術(80〜92%改善)、オクリプラスミン。
S1P受容体調節薬(フィンゴリモド・シポニモド):血管内皮カドヘリンの調節を阻害し、血管透過性を亢進させることでBRBを障害する。4)EXPAND試験ではシポニモド群の2%にCMEが発生した(プラセボ群<1%)。4)
イブルチニブ(BTK阻害薬):血液脳関門(BBB)を通過する薬物特性からBRBも障害する可能性が示唆されている。第3相試験ではイブルチニブ群の10%がかすみ目を報告(オファツムマブ群3%)。7)
CRAO急性期:虚血により細胞外イオン恒常性が破綻し、Müller細胞への急激なイオン流入が生じる。その結果aquaporin-4とKir4.1チャネルの発現が増加し、Müller細胞性浮腫(外顆粒層限局)が生じる。3)
免疫回復性ぶどう膜炎(IRU)に続発したCMEに対してトシリズマブが有効であった症例が報告されている。
Nguyenら(2024)は、T細胞性急性リンパ性白血病治療後CMV網膜炎→IRUによるCMEを生じた17歳女性(全身ステロイドが大腿骨頭壊死で禁忌)に対し、トシリズマブ8mg/kg静注を月1回×2サイクル投与した。2サイクル後にCMEの著明な改善が得られた。5)
STOP-UVEITIS試験においてトシリズマブがCME改善をもたらすことが示されており、ステロイド禁忌例における代替治療としての位置づけが期待されている。IL-6がCME病態に直接関与することが示唆される知見である。5)
PPS関連黄斑症は2018年に初めて認識された比較的新しい疾患概念である。PPS中止後も10年以上にわたり病変が進行・CMEが発症する可能性があり、長期経過観察の重要性が示されている。10)
Szelogら(2023)は、PPS 3年使用・中止10年後にCMEを発症した57歳女性を報告した。初診時AMDと誤診され、NSAIDs・ステロイド点眼が無効であったが、ベバシズマブ1.25mg/0.05mL 2回投与で完全消退した。5ヶ月後に僚眼にもCMEが発症した。10)
PPS関連黄斑症の17%にCMEが合併し、累積500g以上の使用で10%超に黄斑症が生じると報告されている。10)
OCT所見の治療反応性を系統的に評価した研究では、以下のバイオマーカーが予後予測に有用であることが示された。13)
2025年のSurvey of Ophthalmology掲載の系統的レビューでは、網膜内嚢胞(76%改善)・網膜下液(67%改善)は治療反応性が高い一方、EZ障害(64%不変/悪化)・ELM障害(67%不変/悪化)・高反射foci(63%不変/悪化)・DRIL(50%不変/悪化)は予後不良を示唆した。13)
EZ・ELM障害の有無を治療方針決定に組み込む動きが進んでいる。
En face OCTを用いたCMEの分布パターン解析により、原因疾患の鑑別に有用な画像特徴が特定されつつある。3)特にCRAO合併CMEにおける急性・慢性期の層別分布の違いは、非侵襲的な病因推定手段として注目されている。