主要リスク因子
高血圧:最も重要なリスク因子。動脈硬化を介して網膜静脈分枝閉塞症発症リスクを高める5)。
脂質異常症:O’Mahoneyらのメタ解析で網膜静脈分枝閉塞症との有意な関連が示されている5)。
糖尿病:血管内皮障害・血液凝固亢進を介して発症に寄与する5)。
緑内障:眼圧上昇による静脈うっ滞がリスクを増加させる5)。

網膜静脈分枝閉塞症(Branch Retinal Vein Occlusion; BRVO)は、網膜の動静脈交叉部で静脈が閉塞し、その支配領域に網膜出血・黄斑浮腫・毛細血管無灌流を生じる血管疾患である。
網膜静脈分枝閉塞症は糖尿病網膜症に次いで2番目に多い網膜血管疾患であり、世界有病率は1000人あたり4.42と推定される1)。Beaver Dam Eye Studyによる15年間の累積発症率は網膜静脈分枝閉塞症 1.8%、網膜中心静脈閉塞症(CRVO)0.5%であり、網膜静脈分枝閉塞症の発症頻度は網膜中心静脈閉塞症を大きく上回る1)。
閉塞部位は上耳側が58〜66%と最多で、下耳側22〜43%、鼻側12.9%の順である1)。病型はその閉塞部位と範囲により以下に分類される。
また虚血性の程度により以下の2型に分類される。
対側眼の発症リスクは7〜10%と報告されており1)、両眼性は5〜10%に認められる。高血圧・脂質異常症などの全身リスク因子が共通するため、対側眼の定期的な眼底検査と全身管理が重要である。
網膜静脈分枝閉塞症の自覚症状は閉塞部位によって異なる。
急性期は閉塞領域に一致した特徴的な眼底所見を呈する。
OCT所見は黄斑浮腫の評価に必須である。
側副血行路は上下の網膜静脈領域の間に発達し、閉塞部位をバイパスする5)。
視力低下の主な原因を以下に示す。
| 原因 | 時期 | 頻度 |
|---|---|---|
| 黄斑浮腫 | 急性〜慢性 | 最多 |
| 黄斑虚血 | 急性期 | 重症例 |
| 新生血管出血 | 慢性期 | 虚血型の約30% |
網膜静脈分枝閉塞症は動静脈交叉部において、硬化した動脈が静脈を圧迫することで発症する。この部位では動脈と静脈が共通の外膜(共有外膜)に包まれており、動脈壁の肥厚・硬化が静脈を直接圧迫する。動脈が静脈の前方(表層側)を走行している比率は97.6〜100%に達する。
圧迫により静脈内腔が狭小化し、Virchowの3徴(血液凝固亢進・血流異常・血管内皮障害)が成立して血栓が形成される。
主要リスク因子
高血圧:最も重要なリスク因子。動脈硬化を介して網膜静脈分枝閉塞症発症リスクを高める5)。
脂質異常症:O’Mahoneyらのメタ解析で網膜静脈分枝閉塞症との有意な関連が示されている5)。
糖尿病:血管内皮障害・血液凝固亢進を介して発症に寄与する5)。
緑内障:眼圧上昇による静脈うっ滞がリスクを増加させる5)。
その他のリスク因子
加齢:動脈硬化の進行に伴い発症率が上昇する。
肥満・喫煙:血管内皮障害・血液粘度増加を介して関与する5)。
高凝固状態:50歳未満・両眼性・再発例ではスクリーニングが推奨される2)。
心血管疾患:網膜静脈分枝閉塞症は心血管イベントリスクの上昇と関連する5)。
近年、mRNAワクチン接種後の網膜静脈分枝閉塞症発症例が報告されている。
Sugiharaら(2022)は、BNT162b2(ファイザー社)接種2日後に発症した38歳男性の網膜静脈分枝閉塞症を報告した2)。アフリベルセプト2mg硝子体内注射2回で最高矯正視力が0.9から1.2に改善した。
Tanakaら(2022)は、mRNAワクチン接種3日後に発症した50歳・56歳の女性2例を報告した3)。いずれもタモキシフェン服用歴を有しており、ワクチン後の凝固亢進にタモキシフェンによる静脈血栓リスクが重なった可能性を指摘した。ラニビズマブ3回投与で視力は20/25から20/20に改善した3)。
Girioniら(2023)は、mRNA-SARS-CoV-2ブースター投与24時間後に両眼性網膜静脈分枝閉塞症を発症した50歳男性を報告し、ワクチン接種後の両眼性網膜静脈分枝閉塞症初報告として記録した4)。ワクチン関連網膜静脈閉塞症の50%超がmRNAワクチンによるもので、発症までの中央値は2日であった4)。
スパイクタンパクによる血栓形成促進・炎症性反応が発症機序として仮説されているが3)4)、発症頻度は極めて稀であり、ワクチン接種の利益がリスクを大幅に上回ると考えられている。
mRNAワクチン(ファイザー・モデルナ)接種後の網膜静脈分枝閉塞症報告が蓄積されており、発症までの中央値は約2日である4)。発症頻度は極めて低く、ワクチン接種の便益がリスクを大幅に上回る。接種後に急激な視力低下や視野欠損を自覚した場合はすぐに眼科を受診することが勧められる。
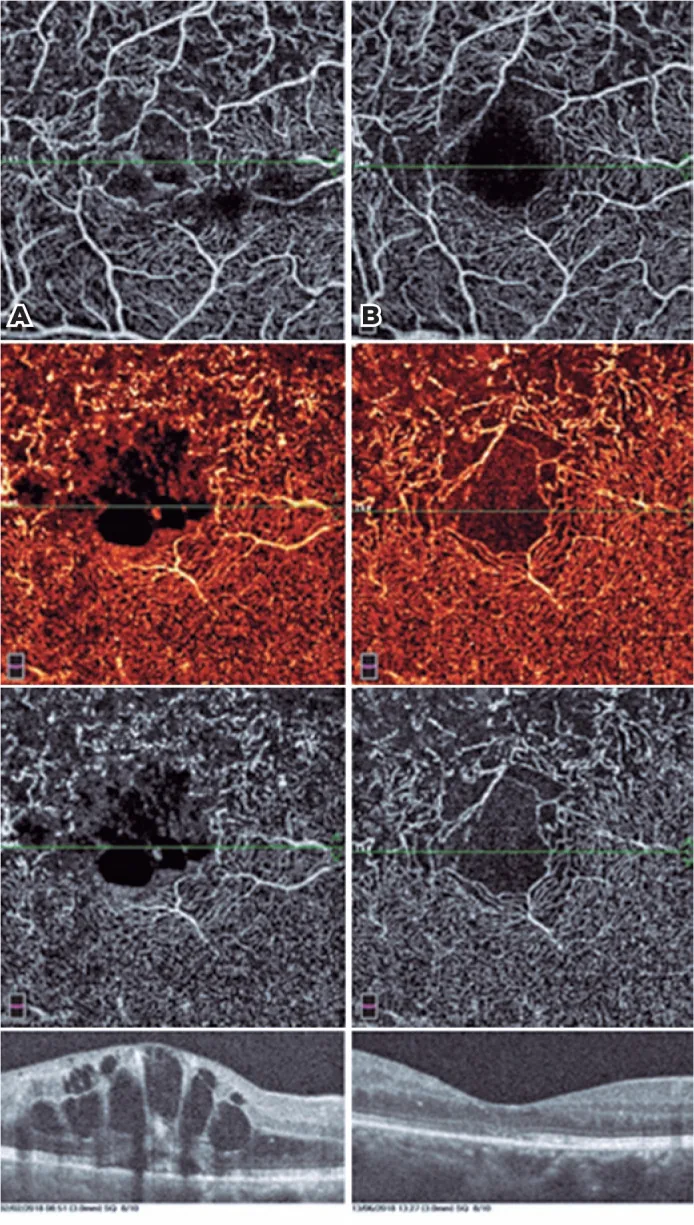
網膜静脈分枝閉塞症の診断は眼底所見が基本となる。閉塞静脈の支配領域に一致した扇形の網膜出血・静脈拡張・綿花状白斑の組み合わせで臨床診断が可能である。
50歳未満・両眼性・再発例では血栓素因(プロテインC・S欠乏、抗リン脂質抗体症候群など)のスクリーニングが推奨される2)。高血圧・脂質異常症・糖尿病の評価も全例で実施する。
| 疾患 | 鑑別ポイント |
|---|---|
| 糖尿病網膜症 | 両眼性・点状出血・新生血管 |
| 高血圧性網膜症 | 出血が静脈分布に限局しない |
| 放射線網膜症 | 放射線照射歴 |
抗VEGF薬の硝子体内注射が網膜静脈分枝閉塞症に伴う黄斑浮腫の第一選択治療である5)。主な臨床試験の結果を以下に示す。
抗VEGF療法
ラニビズマブ(BRAVO試験):0.5mg月1回×6か月で+18文字、61.1%が15文字以上の視力改善を達成5)。
アフリベルセプト(VIBRANT試験):2mgの月1回投与でグリッドレーザーに対して優越性を示し、24週時点で48% vs 24%が15文字以上改善5)。
ファリシマブ(BALATON試験):6mgの投与でアフリベルセプトと同等の効果(56.1% vs 60.4%が15文字以上改善)5)。
ベバシズマブ:保険適用外だが、臨床での使用実績あり5)。
ステロイド療法
デキサメタゾンインプラント(GENEVA試験):0.7mgで41%が15文字以上の改善(6か月時点)5)。
トリアムシノロン(SCORE試験):1年時点でグリッドレーザーに対して優越性なし。
適応:抗VEGFに抵抗する症例、または再発間隔延長を目的として使用する。
症例報告でも抗VEGF療法の有効性が確認されており、アフリベルセプト2回投与で最高矯正視力0.9→1.2への改善2)、ラニビズマブ3回投与で20/25→20/20への改善が報告されている3)。
BVOS研究によれば、未治療でも37%が自然に視力改善する一方、23%は最終視力が20/200以下となり、34%が20/40以上を達成する5)。自然経過の幅が広いため、治療介入の意思決定にはOCTによる黄斑浮腫の定量評価が重要である。
以下の場合に適応を検討する。
RETAIN研究では平均53か月間・14.8回の注射が必要との報告がある。治療反応を見ながらPRN(必要に応じて)またはT&E(treat-and-extend)で調整するのが一般的である。詳細は「標準的な治療法」の項を参照。
BVOSによれば未治療でも37%が自然に視力改善するが、23%は最終視力が20/200以下となる5)。自然経過は予測が難しく、黄斑浮腫が持続する場合は治療介入が推奨される。
網膜静脈分枝閉塞症の発症機序は多因子性であり、完全には解明されていない。
動静脈交叉部では動脈と静脈が共通の外膜(共有外膜)に包まれている5)。動脈硬化による動脈壁の肥厚・硬化が静脈の外側から圧迫を加え、静脈内腔を狭小化する。OCT研究では交叉部での静脈内腔の変形(扁平化ではなく狭小化)が確認されている。この狭小化により乱流(turbulence)が生じ、慢性的な血管内皮障害→リモデリング→血栓形成へと至る。
炎症性カスケードも重要な役割を担う。網膜静脈分枝閉塞症患者の硝子体液では以下のサイトカインが上昇している。
ワクチン関連網膜静脈分枝閉塞症の機序については、スパイクタンパクによる血栓形成促進・炎症性反応が仮説として提唱されている3)4)。スパイクタンパクが血管内皮細胞を直接障害し、von Willebrand因子の放出を促進するとする説もある。
ファリシマブはAngiopoietin-2(Ang-2)とVEGF-Aの両方を同時に阻害する二重特異性抗体である。BALATON/COMINO試験ではアフリベルセプトと同等の有効性が示され、より長い投与間隔が期待されている5)。
BALATON試験では、ファリシマブ6mgとアフリベルセプト2mgを比較し、24週時点で視力改善率(≥15文字)がそれぞれ56.1%と60.4%と同等であった5)。Ang-2阻害による血管安定化効果が長期的な治療間隔延長につながる可能性が検討されている。
ワクチン接種後の網膜静脈閉塞症症例報告が世界的に蓄積しており、因果関係の解明が進んでいる。
Girioniら(2023)は、mRNA-SARS-CoV-2ブースター投与後の両眼性網膜静脈分枝閉塞症を初めて報告した4)。ワクチン関連網膜静脈閉塞症の50%超がmRNAワクチンによるもので、発症までの中央値は2日であった。スパイクタンパクの直接的な血管内皮障害・プロコアギュラント反応が病態に関与する可能性が示唆されている4)。