原発先天緑内障(PCG)は前房 隅角 の発育異常(線維柱帯 形成不全)による房水 流出障害で眼圧 が上昇する稀な先天性疾患である。
白人での発症率は12,000〜18,000出生に1人であり、近親婚がある場合は5〜10倍に上昇する1) 。日本では出生10万人あたり1.8〜2.4人の発生が報告されている。
羞明 ・流涙・眼瞼痙攣 の「三徴」が典型的な初期症状であり、眼圧上昇により牛眼(buphthalmos)やHaab線条を生じる1) 。CYP1B1が最も一般的な原因遺伝子であるが、遺伝子検査で原因を特定できる確率は約40%にとどまる。
治療の第一選択は手術(隅角切開術・線維柱帯切開術 )であり、薬物療法は補助手段として用いる2) 。
早期診断・治療により良好な視機能が得られる一方、診断の遅れや治療抵抗例では重篤な視力 障害に至ることがある。
生涯にわたる眼圧管理と屈折 矯正・弱視 治療が必要である1) 。
原発先天緑内障(primary congenital glaucoma; PCG)は、他の眼球または全身の発達異常を伴わずに、遺伝的に決定された線維柱帯(trabecular meshwork)および前房隅角の異常によって眼圧が上昇する稀な疾患である。以前は線維柱帯形成不全(trabeculodysgenesis)、隅角形成不全(goniodysgenesis)、原発乳児緑内障 などの用語が用いられていたが、2013年の小児緑内障研究ネットワーク(CGRN)による国際分類で原発先天緑内障に統一された1) 。
原発先天緑内障は原発小児緑内障の中で最も一般的な形態であり、発症時期に基づき以下の4型に分類される1) 。
新生児期発症 (0〜1か月):最も重症な型である。乳児期発症 (1か月超〜24か月):最も頻度が高い。生後3〜9か月に好発する。遅発性(遅延認知型) (2歳超):発症時期が遅いほど症状・所見が乏しくなる。自然停止型 :極めて稀。眼圧は正常であるが牛眼やHaab線条など原発先天緑内障の典型的所見を認める。
白人ヨーロッパ人における発症率は12,000〜18,000出生に1人である1) 。東欧の一部地域では1,250人に1人と高率である。近親婚がある場合、発症率は5〜10倍に増加する1) 。65〜80%の症例が両眼性であり、男女比は約3:2と男性に多い1) 。
原発先天緑内障は全眼疾患患者の0.01%未満であるが、世界の小児失明の5%を占めるとされている。
Q 原発先天緑内障はどのくらいの頻度で発症するか?
A 白人では12,000〜18,000出生に1人とされるが、近親婚が多い地域では1,250人に1人にまで上昇する。65〜80%が両眼性である1) 。
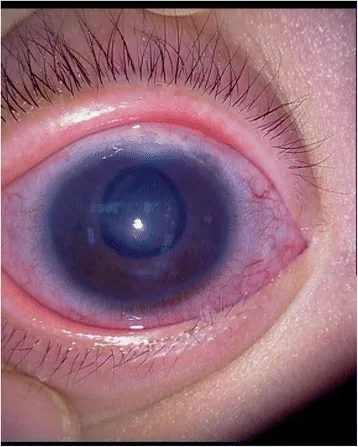
原発先天緑内障の角膜浮腫とハーブ線条 Li H, Liu T, Chen X, et al. A rare case of primary congenital glaucoma in combination with neurofibromatosis 1: a case report. BMC Ophthalmol. 2015 Oct 29;15:149. Figure 2. PMCID: PMC4625924. License: CC BY.
角膜浮腫 とハーブ線条を示す臨床写真である。原発先天緑内障でみられる
角膜 拡大と
デスメ膜 断裂の具体像として参考になる。
原発先天緑内障患者は眼圧上昇に伴う角膜浮腫による刺激症状として、以下の「臨床的三徴」のうち1つ以上を呈する1) 。
羞明(photophobia) :光を嫌がり、屋外で目を細める。流涙(epiphora) :眼脂を伴わない涙が特徴的。鼻涙管閉塞との鑑別が重要である。眼瞼痙攣(blepharospasm) :まぶたを強く閉じる。
角膜浮腫・混濁による視力低下、進行性の近視 、乱視 なども生じる。乳幼児では、保護者が「目が白い」「目が大きい」「目が青っぽい」と気づいて受診するきっかけとなることが多い。
角膜所見
Haab線条 :Descemet膜の水平〜斜方向の断裂で、先天緑内障の強い指標である1) 。
角膜径増大 :出生時正常値は9.5〜10.5 mm。1歳未満で12 mm超、年齢を問わず13 mm超は緑内障を強く疑う。
角膜浮腫・混濁 :上皮性(ときに実質性)の浮腫。未治療では永久的瘢痕化に至る。
眼球・視神経所見
牛眼(buphthalmos) :眼圧上昇による眼球全体の拡大。角膜拡大は3歳頃まで、強膜 伸展は10歳頃まで進行しうる。
視神経乳頭陥凹
眼軸長 増大1) 。
EGS第6版では、以下の5項目中2項目以上を満たす場合に原発先天緑内障と診断する1) 。
眼圧 :21 mmHgを超える角膜所見 :Haab線条、角膜浮腫、角膜径増大(新生児≧11 mm、1歳≧12 mm、年齢問わず>13 mm)視神経乳頭陥凹 :進行性のrim減少、左右C/D差≧0.2進行性近視 :年齢不相応な眼軸長増大隅角所見 :虹彩 の高位付着、残存ぶどう膜組織、線維柱帯形成不全
Q 子どもの目が大きいだけでも緑内障の可能性はあるか?
A 年齢を問わず角膜径が13 mmを超える場合は緑内障の疑いが極めて濃厚である。自然停止型原発先天緑内障では眼圧正常にもかかわらず牛眼やHaab線条を認めることがあり、緑内障疑いとしての経過観察が必要となる。
原発先天緑内障の大多数は孤発性(家族歴なし)であるが、約10〜40%は家族性であり、浸透率40〜100%の常染色体劣性遺伝 形式をとる1) 。連鎖解析により5つの遺伝子座が同定されている。
主要な原因遺伝子は以下のとおりである。
遺伝子 遺伝子座 染色体 機能 CYP1B1 GLC3A 2p22-p21 脂肪酸・ビタミン代謝酵素 LTBP2 GLC3D 14q24.2-q24.3 潜在型TGF-β結合タンパク TEK/TIE2 GLC3E 9p21 Schlemm管発達シグナル
CYP1B1 (GLC3A):最も一般的な原因遺伝子である。胎児・成人の神経上皮や毛様体 で発現し、眼の発達に不可欠な化合物を代謝する。CYP1B1欠損マウスでは重度の線維柱帯萎縮がみられる。CYP1B1変異例は比較的早期に発症し、両眼性で典型的な経過をたどりやすいとされる。LTBP2 (GLC3D):線維柱帯や毛様突起で発現するが、眼における役割は完全には解明されていない。TEK/TIE2 (GLC3E):アンジオポエチン/TEKシグナル伝達経路はSchlemm管の発達に必須であり、TEKノックアウトマウスではSchlemm管が欠損する。MYOC :原発先天緑内障症例の最大5.5%に関与する可能性がある。EFEMP1 も候補遺伝子として報告されている1) 。
現在、遺伝子検査で原因を特定できる確率は約40%である。遺伝子検査は他の先天異常の除外と家族計画のために推奨される1) 。
近親婚は疾患の重症化および予後不良因子とされる1) 。原発先天緑内障患者の第2子が罹患する確率は通常3%以下であるが、すでに2人の子が罹患している場合は常染色体劣性遺伝を仮定すると25%に上昇する。
Q 遺伝子検査は受けるべきか?
A EGSガイドラインでは、他の先天異常の除外と家族計画の観点から遺伝子検査が推奨されている1) 。ただし現時点で原因を特定できる確率は約40%であり、検査陰性でも原発先天緑内障は否定できない。
原発先天緑内障の診断は、眼圧測定 値が正確でなくても臨床的に下せることが多い。Haab線条の存在は先天緑内障の強い指標である1) 。
眼圧測定 :覚醒下の安静時にハンドヘルド眼圧計(リバウンド眼圧計を含む)で測定するのが最良である1) 。泣いている児では偽高値となり、全身麻酔薬は偽低値を生じるため注意が必要である。リバウンド眼圧計は在宅測定にも使用可能である1) 。鎮静にはケタミンやトリクロホスナトリウムが眼圧への影響が少ない。セボフルレン吸入麻酔下では眼圧が著明に低下するため、15 mmHg以下を正常上限とみなす意見がある。角膜径・角膜厚測定 :角膜径は経時的にモニタリングし、年齢相応の正常範囲を超える場合は眼圧コントロール不良を疑う。中心角膜厚は浮腫がなくても増加していることがあり、眼圧測定値に影響を与えうる1) 。眼軸長測定 :診断・経過観察に不可欠である。近視の進行と眼軸長増大は緑内障進行を示唆する。隅角検査 :病型診断と治療法選択に不可欠であるが、乳幼児では全身麻酔を要することが多い。角膜混濁で隅角鏡観察が困難な場合は超音波生体顕微鏡 (UBM)が有用である。視神経乳頭 評価視力・屈折検査 :不正乱視、角膜混濁、Haab線条は弱視の原因となるため、屈折検査は経過観察中に眼圧測定と並行して定期的に行う。
原発先天緑内障と紛らわしい疾患を以下に示す1) 。
鑑別疾患 鑑別のポイント 結膜炎 眼脂・充血あり、角膜径正常 鼻涙管閉塞 眼脂あり、角膜径正常 PPMD 角膜後面の小胞状変化 CHED 両眼性角膜浮腫、眼圧正常 X連鎖巨大角膜 角膜径増大、眼圧正常 出生時外傷 外傷歴、Haab線条は通常垂直
治療の第一選択は手術である2) 。原発先天緑内障の原因が隅角の発育異常であり手術的に解決可能なこと、乳幼児では薬物治療の実効確認が困難なこと、保護者依存のアドヒアランスに問題があることが理由である2) 。薬物療法は周術期ないし術後の補助手段として用いる2) 。
小児眼科および緑内障治療に十分な経験を有する施設で行うべきであり、再手術や長期にわたる経過観察、弱視治療を含む包括的管理が必要である2) 。
線維柱帯切開術(trabeculotomy) :角膜透見が困難でも施行できる利点がある2) 。結膜 弁・強膜弁の作製が必要であり、将来の濾過手術 の施行を困難にする可能性がある。マイクロカテーテルを用いた360°線維柱帯切開術も試みられている2) 。日本では小児緑内障手術の第一選択として線維柱帯切開術が広く普及しており、成功率は原発先天緑内障で65〜85%、他の先天異常を伴う場合でも30〜80%と報告されている。隅角切開術(goniotomy) :透明な角膜を有する症例が適応である2) 。1回の手術で90〜120°の切開が可能であり、3回まで別の部位からアプローチできる2) 。生後3〜12か月に発症した原発先天緑内障では、隅角切開術・線維柱帯切開術ともに同様の成功率(70〜90%)である2) 。術式の選択は術者の経験による。不成功の危険因子は隅角の未発達の程度と前眼部の過剰拡大である2) 。
濾過手術(trabeculectomy) :隅角手術が無効な症例が適応となる2) 。原発先天緑内障患者の強膜は薄く弁作製が困難であり、代謝拮抗薬 を併用しても濾過胞形成が困難な場合がある。1年後成功率は50〜87%と成人に比べ不良である2) 。プレート付きチューブシャント 手術 :海外では濾過手術無効例に使用されるが、日本における明確なエビデンスはまだない2) 。毛様体破壊術 2) 。
原発開放隅角緑内障 に準じて薬物を組み合わせて使用するが、以下の注意が必要である2) 。
乳幼児では体重・体表面積に比して投与量が過大となりやすいため、可能な限り低濃度薬剤から開始する。
交感神経α₂受容体作動薬 (ブリモニジンなど)は2歳未満で絶対禁忌である。精神神経症状(傾眠・徐脈・低血圧など)を引き起こす1) 2) 。プロスタノイドFP受容体作動薬 の小児における効果は成人に比べ弱い2) 。小児ではぶどう膜強膜流出路が未発達なためノンレスポンダーが多いが、β遮断薬 よりは眼圧下降効果がやや優れるとされる。点眼薬は涙嚢・鼻腔粘膜から直接全身循環に入るため、小児では1滴でも重篤な全身性副作用をきたしやすい。点眼後の涙嚢部圧迫の指導が推奨される。
生涯にわたる眼圧経過観察が必須であり、屈折矯正と弱視治療による最適な視覚発達の支援も不可欠である1) 。
Q なぜ薬物療法ではなく手術が第一選択なのか?
A 原発先天緑内障の原因は隅角の発育異常であり、手術で解決可能である。乳幼児では薬物の効果確認が困難であり、アドヒアランスにも問題がある。また、α₂受容体作動薬の禁忌やプロスタノイドの効果減弱など、小児に使用可能な薬剤が限られている2) 。
原発先天緑内障における眼圧上昇は、前房隅角の異常発達に伴う房水流出障害によって生じる1) 。
1950〜60年代には前房隅角を覆う非穿孔性の膜(Barkan膜)が原因と説明されていたが、その後の組織学的調査でそのような膜の存在は否定された。現在は流出障害が線維柱帯自体に起因すると考えられている。
通常、妊娠第3三半期に毛様体と周辺部虹彩は角膜・強膜から離れるように後方へ移動する。原発先天緑内障では線維柱帯内でのコラーゲン梁の過剰または早期の蓄積がこの後方移動を妨げ、虹彩根部や毛様体筋が前方に付着したまま残り、線維柱帯を閉塞させたりSchlemm管を圧迫したりすると提唱されている。
Rao(2025)は原発先天緑内障患者4名から得た線維柱帯標本の組織学的解析を行い、傍管部(juxtacanalicular meshwork: JCM)および角膜強膜部(corneoscleral meshwork)の拡大、TM梁の肥厚、紡錘形核の増加(上皮間葉転換の示唆)、ならびにJCM内に形態学的に異なる2つのゾーンが存在することを報告した3) 。これらの所見は、原発先天緑内障におけるTM各領域の異常な分化と分化異常の不均一性を示唆している。
GATT(gonioscopy-assisted transluminal trabeculotomy)は、角膜切開から隅角鏡下にSchlemm管にマイクロカテーテルまたは縫合糸を挿入し、全周の線維柱帯を切開する比較的新しい手技である。成人緑内障では有効性が確立されつつあり、小児への応用が進んでいる。
Songら(2022)は、3歳の原発先天緑内障男児に対しGATTを施行した症例を報告した。虹彩がSchwalbe線まで隅角全体を覆い、通常の隅角構造が不可視であったが、フック操作で虹彩を剥離してSchlemm管を同定し、GATTを成功させた。術後6か月の眼圧は安定していた4) 。
Elhusseinyら(2023)は、過去に緑内障手術歴のある原発先天緑内障患者6名7眼に対するGATTの1年成績を報告した。平均眼圧は術前25.7±5.9 mmHgから12か月後に12.0±1.5 mmHgへ有意に低下した。完全成功率は85.7%(6/7眼)、限定的成功を含めると100%であり、追加の緑内障手術を要した眼はなかった。重篤な合併症は認めなかった5) 。
Dadaら(2022)は、角膜混濁を伴う原発先天緑内障に対し、23Gレーザー内視鏡プローブを用いて隅角構造を可視化しながら隅角切開術を施行する新技術を報告した6) 。従来、隅角切開術は透明角膜が適応条件であったが、内視鏡の補助により角膜混濁眼でも施行可能となる可能性が示された。
家族歴がある場合や近親婚が多い地域などのハイリスク群に対して、将来的に出生前遺伝子スクリーニングが予防的手段として浮上する可能性がある。
European Glaucoma Society. European Glaucoma Society Terminology and Guidelines for Glaucoma, 6th Edition. Br J Ophthalmol. 2025;109(Suppl 1):S1-S270.
日本緑内障学会. 緑内障診療ガイドライン(第5版). 日眼会誌. 2022;126(2):85-177.
Rao A. Histopathological changes in the trabecular meshwork in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2025;38:102340.
Song Y, Zhang X, Weinreb RN. Gonioscopy-assisted transluminal trabeculotomy in primary congenital glaucoma. Am J Ophthalmol Case Rep. 2022;25:101366.
Elhusseiny AM, Aboulhassan RM, El Sayed YM, et al. Gonioscopy-assisted transluminal trabeculotomy following failed glaucoma surgery in primary congenital glaucoma: one-year results. Case Rep Ophthalmol Med. 2023;2023:6761408.
Dada T, Satpute K, Bukke AN, et al. Endoscope-assisted goniotomy in primary congenital glaucoma with corneal opacification. BMJ Case Rep. 2022;15:e252958.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください