PACNS(primary angiitis of the central nervous system)は脳・脊髄・髄膜に限局した炎症性血管炎で、全身性疾患を伴わない。
年間発症率は約2.4例/100万人ときわめてまれな疾患である。
最も多い初発症状は頭痛(最大63%)と認知機能障害(最大54%)で、全身症状は乏しい。
確定診断のゴールドスタンダードは脳生検だが感度は約75%にとどまり、MRI・脳血管造影・髄液検査を組み合わせた総合診断が必要である。
治療の柱は副腎皮質ステロイド とシクロホスファミドの免疫抑制療法 であり、神経内科・リウマチ科との連携が不可欠である。
眼科的には一過性の片眼性視力 障害、同名半盲 、複視 などが生じうる。
最も類似するRCVS(可逆性脳血管攣縮症候群)との鑑別が重要であり、誤診による免疫抑制療法の投与はRCVSでは禁忌となる。
原発性中枢神経系血管炎(PACNS)は、脳・脊髄・髄膜の動脈・静脈に限定して炎症が生じる血管炎で、二次性CNS血管炎(全身性疾患に関連するもの)とは明確に区別される。
1922年にHarbitzが初めて報告し、1988年にCalabreseが診断基準を提唱した5) 。
疫学的には年間発症率は約2.4例/100万人とまれな疾患である1)2) 。診断時の年齢中央値は約50歳だが、小児を含むあらゆる年齢層で発症しうる。性別は以前2:1で男性優位とされたが、近年の症例集積では性差がみられないとする報告もある。
血管炎症候群は障害される血管の太さにより分類される概念の総称であり、PACNSはこの中でCNS血管に限局した亜型に位置づけられる。
病因は不明で、VZV・マイコプラズマなどの感染因子による炎症反応の関与が提案されているが、確証はない。
Q PACNSと二次性CNS血管炎はどう違うのか?
A PACNSはCNSに限局した血管炎であり、全身性疾患を伴わない点が特徴である。二次性CNS血管炎はSLE ・シェーグレン症候群 ・感染症・悪性腫瘍などの全身疾患に関連して発症し、はるかに頻度が高い。発熱やESR著明上昇がみられる場合は二次性を積極的に疑う。
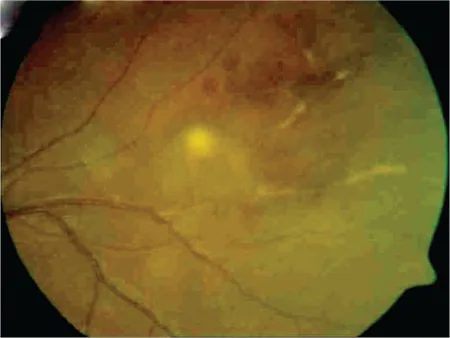
primary cns vasculitis occlusive retinal vasculitis A Case of Presumed Tuberculosis Uveitis with Occlusive Vasculitis from an Endemic Region. Turk J Ophthalmol. 2017 Jun 1; 47(3):169-173. Figure 1. PMCID: PMC5468532. License: CC BY.
Occlusive vasculitis and choroiditis focus in the left eye
PACNSの症状は非特異的なものが多く、診断の遅れを招きやすい。
頭痛 :最も多い初発症状。最大63%の患者で認められ、進行性に増悪する。認知機能障害 :2番目に多く最大54%。記憶障害・集中力低下・見当識障害など。脳卒中様症状 :片麻痺・失語・感覚障害などの局所神経脱落症状、TIA様の一過性症状。痙攣発作 :局所性発作が初発となることもある10) 。全身症状の乏しさ :発熱・体重減少・ESR上昇はまれ。CNSに病変が限局するため。
小児では片麻痺(最大80%)・感覚脱失(79%)・微細運動障害(73%)が高頻度で、頭痛や認知障害は成人より少ない(56%・37%)。
求心路障害による視力障害 :一過性黒内障 (片眼性)・同名半盲(両眼性)。遠心路障害による複視 :眼球運動神経麻痺に起因する。乳頭浮腫 黄斑部 滲出物を呈した症例も記載されている。バリント症候群 眼球運動失行 ・同時失認 ・視覚性運動失調の三徴。後頭頭頂葉病変で生じる。ぶどう膜炎 ・網膜血管炎
Zhuoら(2022)が報告した腫瘍様PACNSの5歳女児では左同名半盲を呈し、画像上左後頭葉・側頭葉に腫瘤様病変を認めた2) 。
Q PACNSで眼の症状が出ることはあるか?
A 視覚路(視神経 ・視交叉 ・後頭葉)や眼球運動神経が障害されると、視力低下・視野欠損 ・複視が生じる。ぶどう膜炎・網膜血管炎はPACNSでは典型的ではなく、認められる場合は全身性血管炎など二次性疾患の除外が必要となる。
PACNSの正確な病因は未解明であり、特定のリスク因子も証明されていない。
以下は二次性CNS血管炎の原因であり、PACNSを診断する際には除外が必要な疾患群である。
原因カテゴリ 代表的な疾患・因子 感染症 VZV、HIV、HCV、CMV、梅毒、結核、アスペルギルス症 結合組織疾患 SLE、RA、シェーグレン症候群、皮膚筋炎 その他の全身疾患 抗リン脂質抗体症候群、悪性リンパ腫、神経サルコイドーシス 薬物 コカイン、アンフェタミン、エフェドリン
PACNSは除外診断であり、単一の確定的バイオマーカー は存在しない。
Calabrese & Mallek(1988)の基準が広く用いられる1) 。
他の原因では説明できない局所神経脱落症状の存在
脳血管造影陽性所見または脳生検による血管炎の組織学的確認
全身性血管炎の証拠がないこと
またRice & Scolding分類では「確実例」(組織学的証拠あり)と「可能性大例」(臨床・画像・髄液所見によるがの診断)に分けられる5) 。
血液検査 :PACNSに特異的なバイオマーカーはない。CBC・ESR・CRP は通常正常または軽度異常。ESR・CRP著明上昇は二次性CNS血管炎を示唆する。ANA・ANCA・抗リン脂質抗体などで二次性を除外する。髄液(CSF)分析 :確定患者の最大90%に異常を認める。蛋白上昇・軽度白血球増多が典型的。培養・PCR・フローサイトメトリーで感染・悪性疾患を除外する。Lopesら(2023)の症例ではCSF白血球44個/L、蛋白0.52 g/Lを認めた3) 。MRI :初期画像診断の第一選択。皮質・皮質下の多発両側性梗塞が最多。ガドリニウム増強病変・頭蓋内出血・腫瘤様病変も生じうる。所見は非特異的で多様である。小児では片側性白質病変が多い。脳血管造影 :血管の「ビーズ状(beaded)変化」(狭窄と拡張が交互に出現)・閉塞・側副血行路形成が特徴的所見4) 。感度は変動し非特異的であるが、鑑別に有用。経頭蓋ドプラ超音波 :PACNSが疑われる際の初期評価に有用。血行動態変化をモニタリングでき、治療反応の評価にも使用できる。Camposら(2023)の症例では右MCA収縮期血流速度が470 cm/秒に達し、ステロイド開始10日後に285 cm/秒に改善した1) 。脳生検 :診断のゴールドスタンダード。ただし病変が分節性のため感度は約75%であり、系統的レビューでは35.4%との報告もある3) 。陰性でも疾患を除外できない。
最も重要な鑑別疾患はRCVS(可逆性脳血管攣縮症候群)である。RCVSは若年者に多く、重度の再発性雷鳴頭痛を呈し、CSFは正常であることが多い。PACNSと異なり、RCVSに対する免疫抑制療法は禁忌である。
巨細胞性動脈炎 は60歳代後半以降に頭痛で初発し、動脈生検で確定する。25〜50%に前部虚血性視神経症を合併するため、眼科的所見の確認が重要である。
Q PACNSの確定診断にはどのような検査が必要か?
A ゴールドスタンダードは脳生検による組織学的確認だが、感度は約75%と高くない3) 。MRI・脳血管造影・髄液分析を組み合わせ、二次性原因を除外したうえで総合的に診断する。感度が補完できるよう複数の検査を並行して実施することが推奨される。
PACNSの治療は免疫抑制療法が中心となる。神経内科医・リウマチ専門医との多職種連携のもとで管理する。
副腎皮質ステロイド :メチルプレドニゾロンパルス療法(1 g/日、3〜5日間)を行い、その後プレドニゾロン1 mg/kg/日経口投与へ移行する3) 。シクロホスファミド(CYC) :ステロイドとの併用がより標準的。NIHプロトコールが用いられ、500 mg/月×6か月の静注投与が行われることがある3)7) 。CYCを併用することでステロイド単独より再発が少ないとする報告がある6) 。
導入療法
ステロイドパルス :メチルプレドニゾロン1 g/日×3〜5日間。
経口ステロイド :プレドニゾロン1 mg/kg/日へ移行後、漸減。
シクロホスファミド :500 mg/月×6か月(NIHプロトコール)。ステロイドとの併用が標準。
維持療法
開始時期 :導入療法4〜6か月後に切り替え。
薬剤選択 :ミコフェノール酸モフェチル (MMF)、メトトレキサート 、アザチオプリン のいずれかを使用。
MMFの用量例 :500 mg×2回/日から開始し、1000 mg×2回/日へ増量4) 。
導入療法4〜6か月後から切り替える。MMF・メトトレキサート・アザチオプリンが用いられる6) 。
Kuruvilaaら(2022)の35歳男性例では、ステロイド+MMF(500 mg×2→1000 mg×2)で治療を開始し良好な転帰を得た4) 。
Datynerら(2023)の8歳小児SV-cPACNS例(GFA P抗体陽性)では、Brainworksプロトコールに基づきデキサメタゾン→メチルプレドニゾロンパルス5日→12か月漸減+CYC 7回→MMF維持の順で治療した8) 。
リツキシマブ 6) 。TNF -α阻害薬 :インフリキシマブ ・エタネルセプトが急速進行例で良好な反応を示したとする報告がある。
ステロイドの長期使用は白内障 ・緑内障 ・高血糖・骨粗鬆症・易感染性に注意が必要である。眼科的副作用(ステロイド白内障・ステロイド緑内障 )の定期的モニタリングを行う。
シクロホスファミドは骨髄抑制・出血性膀胱炎・日和見感染・催奇形性のリスクがある。十分な補液と定期的な血算・尿検査を行う。
長期免疫抑制による日和見感染(肺炎球菌・ヘルペスウイルス等)の予防措置を講じる。
RCVSと誤診した場合、ステロイドや免疫抑制薬の投与がRCVSを悪化させる可能性があるため、投与前の鑑別診断が極めて重要である。
Q PACNSの治療はどのくらい続けるのか?
A 導入療法(ステロイド+CYC)は約6か月間行い、その後MMF等の維持療法へ移行する。再発リスクがあるため長期フォローが必要であり、治療期間は症例によって異なる。定期的な画像・臨床評価で治療反応をモニタリングしながら漸減する。
PACNSには3つの主要な組織病理学的亜型がある。
肉芽腫性
頻度 :最も一般的な亜型。
病理所見 :血管全層を侵す境界明瞭な肉芽腫。
βアミロイドとの関連 :最大50%の症例でβアミロイド沈着を伴い、炎症性脳アミロイドアンギオパチーとの重複が示唆される。
リンパ球性
病理所見 :リンパ球と形質細胞による血管壁浸潤。
小児での特徴 :小児PACNSではリンパ球性パターンが多い5) 。
壊死性
病理所見 :血管壁のフィブリノイド壊死。
まれな亜型 :好酸球性浸潤を示す例も報告されており、EGPAの病理所見を呈するが全身性EGPAの診断基準を満たさない7) 。
血管壁の炎症は免疫細胞浸潤とサイトカイン・ケモカインネットワークが中心的役割を担う5) 。
免疫細胞浸潤 :CD4陽性T細胞を主体とするリンパ球が血管壁に浸潤する。ケモカイン・サイトカイン :IL-6・IL-8・CXCL1・CXCL10などが炎症を増幅させる。粘膜類天疱瘡(マトリックスメタロプロテアーゼ)とTIMP :血管壁構造を破壊し、線維性肥厚による狭窄(→虚血)と血管壁脆弱化による動脈瘤形成(→出血)をもたらす。小児の特徴 :前循環優位で近位血管領域に好発する。小児ではvon Willebrand因子がバイオマーカーになりうる可能性が示唆されている5) 。
通常PACNSは両側性であるが(Mayo ClinicコホートFの95.6%が両側性)、片側のみに再発を繰り返す亜型が稀に報告されている。大脳半球間の免疫応答非対称性が原因として考えられており、これまで7例が報告されている10) 。
Vibhaら(2023)は、反復する局所性意識を保った発作のみを呈した35歳男性のPACNS例を報告した10) 。焦点性痙攣のみで発症し、生検で肉芽腫性血管炎が確認され、ステロイド+MMFで発作が消失した。
血管壁MRIはPACNSとRCVSの鑑別に有望な手法である。PACNSでは血管壁の増強効果(炎症性変化)が認められるのに対し、RCVSでは認められないことが多い。脳MRAの感度は90〜100%と報告されている1) 。
腫瘍様PACNSは全PACNSの約5%を占め、腫瘍との画像鑑別が困難である2) 。SWI(磁化率強調画像)とASL(動脈スピンラベリング)の組み合わせが鑑別に有用との報告がある。PACNSでは低灌流を、腫瘍では過灌流を示す傾向がある。
CNS血管炎の1.8%で水頭症合併が報告されており、院内死亡の主因となる3) 。PACNSに限ると極めてまれで報告は2例のみである。髄膜の線維瘢痕化によるCSF流通障害が機序として推定されている。
Levitら(2023)は補体 因子I(CF I)欠損による補体介在性CNS血管炎の1例を報告した9) 。CFIはC3bとC4bを不活化してC3転換酵素形成を抑制するが、その欠損により代替経路が異常活性化し好中球性血管炎が生じた。IL-1阻害薬アナキンラ投与後は20か月間再発を認めなかった。
Campos A, et al. Primary Central Nervous System Vasculitis: A Rare Cause of Stroke. Cureus. 2023;15(5):e39541.
Zhuo X, et al. A 5-year-old child presenting with tumor-like primary angiitis of the central nervous system. Pediatr Investig. 2022;6(2):140-143.
Lopes J, et al. Hydrocephalus: a rare complication of primary central nervous system vasculitis. BMJ Case Rep. 2023;16:e253187.
Thekkekarott Kuruvila A, et al. Primary Angiitis of the Central Nervous System: An Uncommon Cause of Stroke in the Young. Cureus. 2022;14(8):e27799.
Hassan A, Allinson K. Vertebrobasilar circulation hemorrhages in childhood primary angiitis of the central nervous system. Autops Case Rep. 2022;12:e2021391.
Sarhan FMA, et al. Right arm weakness and mouth deviation as a presentation of Primary Angiitis of the Central Nervous System treated with rituximab: A case-report. Ann Med Surg. 2022;79:104040.
Yamashita K, et al. Primary Angiitis of the Central Nervous System with Pathological Findings of Eosinophilic Granulomatosis with Polyangiitis. Intern Med. 2024;63:1939-1943.
Datyner E, et al. Small vessel childhood primary angiitis of the central nervous system with positive antiglial fibrillary acidic protein antibodies. BMC Neurol. 2023;23:57.
Levit E, et al. Pearls & Oy-sters: Homozygous Complement Factor I Deficiency Presenting as Fulminant Relapsing Complement-Mediated CNS Vasculitis. Neurology. 2023;101:e220-e223.
Vibha D, et al. Focal CNS vasculitis masquerading as new-onset focal aware seizures. BMJ Case Rep. 2023;16:e255535.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください