感染性因子
グラム陰性桿菌:緑膿菌(Pseudomonas)が代表的である。内毒素による副経路活性化で早期に免疫輪が出現する。
ヘルペスウイルス:単純ヘルペス(HSV)および帯状ヘルペス(VZV)の免疫性実質角膜炎で認められる。
アカントアメーバ:臨床経過が長期にわたるため免疫輪の出現も遅れる。
真菌:真菌性角膜炎およびPythium insidiosum角膜炎で報告されている。
その他:Moraxella atlantae、微胞子虫、非結核性抗酸菌。

Wessely免疫輪(Wessely immune ring)は、外来抗原に対する免疫反応の結果として生じる角膜実質内の無菌性輪状浸潤である。1911年にWesselyがウシやウマの血清タンパク質に曝露させたウサギ角膜において再現可能な免疫反応を記録し、「Wessely現象」として最初に報告した。
1956年にMorawieckiが免疫複合体を介した補体活性化の役割を提示した。その後、細菌の内毒素など他の抗原も抗体非依存的なプロペルジン介在性の補体副経路活性化を引き起こしうることが判明した。
感染性角膜炎の経過中に出現する場合と、非感染性の角膜反応として生じる場合がある。
Wessely免疫輪は多様な状況で出現する。感染性では緑膿菌、アカントアメーバ、ヘルペス、真菌などの角膜炎に伴い認められる。非感染性ではコンタクトレンズの慢性使用、エキシマレーザー治療後、点眼薬(ジクロフェナク等)、角膜化学外傷、ベーチェット病、再発性角膜上皮びらんなどで報告されている。いずれの場合も、外来抗原に対する角膜実質内の免疫反応が本態である。
Wessely免疫輪の自覚症状は基礎疾患に関連する。免疫輪自体が視力に重大な影響を与えることは通常ない。
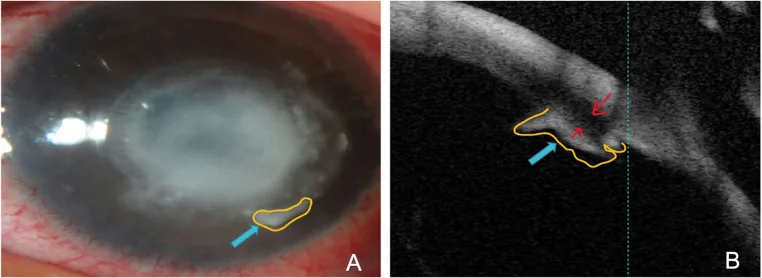
典型的なWessely免疫輪は、角膜輪部付近の周辺部に形成される角膜実質内の輪状浸潤である。感染の中心病巣から透明部分を挟んで離れた位置に目に見える輪を形成する。
免疫輪の出現時期は補体活性化経路により異なる。
| 活性化経路 | 出現時期 | 代表的な病因 |
|---|---|---|
| 古典経路 | 10〜14日後 | 一般的な感染性角膜炎 |
| 副経路 | 1〜5日以内 | 緑膿菌、既感作抗原 |
| 遅延型 | さらに遅れる | アカントアメーバ、微胞子虫 |
感染性因子
グラム陰性桿菌:緑膿菌(Pseudomonas)が代表的である。内毒素による副経路活性化で早期に免疫輪が出現する。
ヘルペスウイルス:単純ヘルペス(HSV)および帯状ヘルペス(VZV)の免疫性実質角膜炎で認められる。
アカントアメーバ:臨床経過が長期にわたるため免疫輪の出現も遅れる。
真菌:真菌性角膜炎およびPythium insidiosum角膜炎で報告されている。
その他:Moraxella atlantae、微胞子虫、非結核性抗酸菌。
非感染性因子
コンタクトレンズ:慢性使用に伴う細菌抗原(特にグラム陰性桿菌の内毒素)への免疫反応と考えられる。保存液の汚染も原因となりうる。
エキシマレーザー:PRKおよびPTK後に報告がある。熱ショックタンパク質と細菌HSPに対する循環抗体の交差反応が仮説として提唱されている。
点眼薬:ジクロフェナクなど。
その他:角膜化学外傷・熱傷、角膜内昆虫刺傷、パリトキシン(サンゴ由来毒素)、ベーチェット病、再発性角膜上皮びらん。
アカントアメーバ角膜炎では輪状浸潤と強膜炎が「重症炎症性合併症(SIC)」と定義される1)。SICの独立したリスク因子として以下が同定されている1)。
Wessely免疫輪は細隙灯顕微鏡による臨床所見から診断する。角膜実質内の輪状浸潤を認めた場合、感染性の輪状浸潤との鑑別が最も重要である。
輪状浸潤(ring infiltrate)は真菌性角膜炎やアカントアメーバ角膜炎でもよく認められる所見であり2)、HSV、水痘帯状疱疹ウイルス、EBウイルスも免疫学的介在性の角膜浸潤を生じ、細菌性・真菌性・アカントアメーバ角膜炎に類似しうる2)。
感染性の輪状浸潤(生存微生物による角膜組織への侵入)を示唆する徴候は以下の通りである。
一方、潰瘍境界の外側にあり、ステロイド点眼に反応する軽度の浸潤所見は、「純粋な」Wessely免疫輪の領域であることを示唆する。
感染性の輪状浸潤では疼痛、高度の結膜充血、上皮欠損、膿性分泌物、壊死、前房反応など炎症所見が顕著である。無菌性のWessely免疫輪は感染の中心病巣から透明帯を挟んで離れた位置に出現し、炎症所見が軽度でステロイド点眼に反応する。ただし、微生物性角膜炎の経過中に両者が同時に形成されることがあるため、輪状浸潤を認めた場合はまず感染性を疑い培養検査を行うことが原則である。
原因微生物に応じた抗微生物治療が優先される。感染がコントロールされれば免疫輪は消退する。
通常は特別な治療を必要としない。臨床的にはステロイド点眼薬が投与されることがある。「真に無菌性」の浸潤である場合、通常は迅速かつ完全に治癒する。
ブドウ球菌抗原に対するIII型アレルギー反応(補体活性化+好中球浸潤)により角膜周辺部に生じる無菌性浸潤であり、Wessely免疫輪と類似した病態を示す。抗菌薬と低濃度ステロイド点眼の併用が効果的で、長期管理には眼瞼縁の清拭と抗菌眼軟膏塗布が重要である。
Wessely免疫輪の病態の中心は、外来抗原と角膜輪部血管系から実質内へ拡散する抗体との相互作用である。
両経路の関与が症状発現から免疫輪出現までの期間のばらつきを説明しうる。
免疫輪が輪部周辺に輪状に形成される理由は、抗体が輪部血管から角膜中央に向けて拡散し、角膜実質内の抗原と等量比で結合する部位(等価帯)が輪部から一定距離の位置に生じるためである。この反応はArthus反応(局所的III型アレルギー反応)と類似した機序をとる。
抗体は輪部血管から角膜中央に向かって放射状に拡散する。一方、抗原は角膜中央の感染巣や外来物質から周辺に向かって拡散する。両者が最適な比率(等価帯)で結合する部位が輪部から一定距離の輪状ゾーンとなり、そこに免疫複合体が集中的に沈着する。補体活性化と好中球動員もこの部位に集中するため、結果として輪状の浸潤が形成される。
Moorfields Eye Hospitalにおける1991〜2012年のアカントアメーバ角膜炎コホート(培養または病理学的確認例)の後方視的解析では、輪状浸潤(ring infiltrate)と強膜炎が「重症炎症性合併症(SIC)」と定義された1)。SICの独立したリスク因子は34歳超(OR 2.36)とAAT前のステロイド使用(OR 2.56)であった1)。
層別解析では、強膜炎を伴わない患者群において輪状浸潤は予後不良の強い独立因子であった(OR 5.57; 95% CI 2.02–15.39; P=0.001)1)。一方、強膜炎が存在する場合は輪状浸潤の有無にかかわらず予後不良リスクが高く、輪状浸潤の追加的影響は小さかった1)。この結果から、強膜炎と輪状浸潤は関連するが病態生理が異なる可能性が示唆された1)。
PRKおよびPTK後にWessely免疫輪が報告されている。以前はレーザー切除ゾーン端の変性DNAタンパク質の遊離が原因と考えられていたが、近年では物理的ストレス後に産生される哺乳類の熱ショックタンパク質(HSP)が、過去の感染に由来する細菌HSPに対する循環抗体と交差反応するという仮説が提唱されている。
パリトキシン(PTX)産生サンゴの取り扱いに伴う稀な眼表面疾患として報告されている。PTXのNa-K ATPaseポンプへの作用により角膜上皮剥離、Wessely免疫輪形成、角膜周辺部の菲薄化を生じうる。軽度の眼表面障害から角膜融解・穿孔まで重症度は多岐にわたる。