角膜輪部 近傍に三日月状の破壊性炎症を呈する疾患群であり、角膜 穿孔に至りうる発症率は年間100万人あたり0.2〜3例であり、約50%に基礎疾患を認める8)
関節リウマチが最多の原因であり、PUK患者の34〜42%を占める2)
局所ステロイド 点眼は角膜融解を助長しうるため、全身的な免疫抑制療法 が治療の中心となる
膠原病内科・リウマチ科との多科連携が不可欠である
周辺部潰瘍性角膜炎(peripheral ulcerative keratitis: PUK)は、角膜輪部近傍の角膜実質 に三日月状の破壊性炎症を呈する疾患群である。角膜実質の変性・炎症細胞浸潤と上皮欠損を特徴とし、進行すると角膜菲薄化・デスメ膜瘤 ・穿孔に至る。
発症率は年間100万人あたり0.2〜3例と稀であり、男女差はない8) 。約50%に基礎となる全身疾患を認め、そのうち約20%が感染性である8) 。関節リウマチ(RA)が最も一般的な原因であり、PUK患者の34〜42%を占める2) 。
PUKは角膜抗原に対する自己免疫反応、循環免疫複合体の沈着、あるいは外来抗原に対する過敏反応によって発症すると考えられている。角膜周辺部の特殊性として、輪部には血管網・免疫系・神経系が密集しており、免疫複合体が沈着しやすい環境にある。
Mooren潰瘍は定義上、原因不明かつ全身性自己免疫疾患を伴わないものを指す。一方、PUKは全身疾患に伴って発症するものであり、両者の鑑別は治療方針を決定するうえで重要である。Mooren潰瘍では強膜炎 の合併は軽度であるが、膠原病に伴う周辺部潰瘍では上強膜炎 や強膜炎を伴うことが多い。
Q PUKとMooren潰瘍はどう違いますか?
A PUKは全身性自己免疫疾患(関節リウマチやANCA関連血管炎など)に伴って発症する角膜周辺部の潰瘍である。一方、Mooren潰瘍は全身疾患を伴わない特発性の角膜辺縁潰瘍であり、角膜抗原に対する自己抗体の関与が示唆されている。臨床的にはMooren潰瘍で強膜炎の合併は軽度であるが、PUKでは約36%に強膜炎を合併する。全身検索が鑑別の鍵となる。
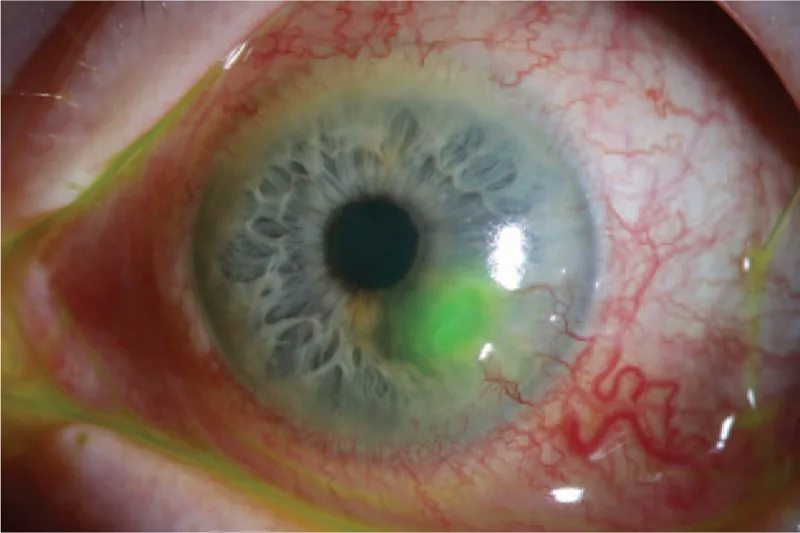
Peripheral Ulcerative Keratitis image Medicine (Baltimore). 2017 Dec 15; 96(50):e8997. Figure 1. PMCID: PMC5815707. License: CC BY.
周辺角膜の潰瘍性病変と菲薄化を伴う充血眼を示す臨床写真である。病変が角膜周辺部に集中することが、病態理解に直結する。
眼痛 :角膜潰瘍 に伴う強い疼痛を認める充血 :毛様充血を伴い、限局性のことが多い視力 低下羞明 ・流涙角膜上皮 障害に伴い出現する
PUKの角膜所見は角膜輪部近傍に限局する三日月状の実質破壊である。
角膜実質浸潤・潰瘍 :角膜輪部と平行に三日月状の浸潤・実質壊死を認める。潰瘍先端はunderminingと呼ばれる深い坑道状を呈する上皮欠損 :潰瘍部の上皮が脱落し、フルオレセイン染色 で陽性となる角膜菲薄化 :進行すると角膜実質が著明に菲薄化する。高度例では砂時計様角膜(hourglass cornea)を呈する4) デスメ膜瘤・穿孔 :極度の菲薄化によりデスメ膜 が突出し、穿孔に至る。穿孔例では梨状瞳孔 と虹彩 組織の脱出を認める3) 強膜炎合併 :PUK患者の36%に強膜炎を併発する角膜血管新生 :慢性例では表層性・深層性の血管侵入を認める5)
PUKは多岐にわたる全身疾患に続発する。大別すると自己免疫性、感染性、その他に分類される。
自己免疫性(最多)
関節リウマチ(RA) :PUK患者の34〜42%を占め、最も一般的な原因である2) 。重症RAや悪性関節リウマチに多く、急速に穿孔に至ることがある。
ANCA関連血管炎 :多発血管炎性肉芽腫症 (GPA)では角膜辺縁潰瘍や壊死性強膜炎を伴う。PR3-ANCA陽性率は約80%である。
結節性多発動脈炎 (PAN)
全身性エリテマトーデス (SLE)
再発性多発軟骨炎 :強膜炎やぶどう膜炎 を伴うことがある。
炎症性腸疾患(IBD) :IBD患者の2〜5%に上強膜炎・強膜炎・ぶどう膜炎などの眼症状を認める9) 。
感染性・その他
大血管炎 :巨細胞動脈炎(GCA)に伴うPUKの報告がある。FDG-PETが診断に有用であった2) 。
化膿性汗腺炎(HS) :まれな原因であるが、Th17経路の共有が示唆されている3) 7) 。HS患者の眼炎症は前部ぶどう膜炎が最多であり、PUKは稀である。
肉芽腫性酒さ :慢性炎症とTh17活性化が関連し、PUKを合併した症例がある1) 。
免疫チェックポイント阻害薬 5) 。
感染性 :Citrobacter koseri涙小管 炎がPUKを惹起した症例がある6) 。結核に伴うPUKの報告もある4) 。
Q どのような全身疾患がPUKを引き起こしますか?
A 最も多い原因は関節リウマチであり、PUK患者の約3分の1を占める。そのほかANCA関連血管炎(多発血管炎性肉芽腫症など)、結節性多発動脈炎、全身性エリテマトーデス、再発性多発軟骨炎、炎症性腸疾患などの膠原病・自己免疫疾患が主な原因となる。まれに化膿性汗腺炎、肉芽腫性酒さ、免疫チェックポイント阻害薬による免疫関連有害事象としても発症する。感染性の原因としては細菌性涙小管炎や結核が報告されている。
細隙灯顕微鏡検査 :角膜周辺部の浸潤・潰瘍・菲薄化の範囲と深度を評価する。上皮欠損の有無をフルオレセイン染色で確認する角膜擦過・培養 :感染性の原因を除外するために施行する眼球超音波検査(Bモード) :後部強膜炎の評価に用いる。PUK患者の36%に強膜炎を合併する前眼部OCT (AS-OCT)
急性期 :角膜上皮の消失、不均一な反射を伴う前部実質の構造破壊、病変部の角膜厚減少を認める治癒過程期 :再生途上の不整な上皮が低反射を呈し、実質の反射が均一化する治癒期 :低反射上皮と高反射実質の間に明瞭な境界線が形成され、瘢痕性の角膜肥厚と菲薄化の安定化を認める
基礎疾患の特定のため、以下の検査を系統的に行う。
検査項目 目的 RF・抗CCP抗体 関節リウマチ ANA SLE・膠原病 ANCA(PR3/MPO) ANCA関連血管炎 RP R・FTA-ABS梅毒 CXR・PPD/IGRA 結核・サルコイドーシス
そのほか末梢血検査、腎機能、尿検査、B型/C型肝炎ウイルス検査、仙腸関節X線、副鼻腔CTなどを必要に応じて追加する。大血管炎が疑われる場合はFDG-PETが有用であり、感度90%・特異度98%と報告されている2) 。
疾患 PUKとの相違点 Mooren潰瘍 全身疾患を伴わない。強膜炎なし〜軽度 Terrien角膜辺縁変性 炎症所見乏しく進行緩徐。上皮欠損なし。脂肪沈着を伴う カタル性角膜潰瘍 輪部との間に透明帯あり。ブドウ球菌に対するIII型アレルギー
カタル性角膜潰瘍はブドウ球菌の菌体外毒素に対するIII型アレルギー反応により角膜周辺部に生じる無菌性の浸潤・潰瘍である。2時・4時・8時・10時に好発し、輪部との間に1〜2mmの透明帯を認める点がPUKと異なる。
PUK治療の目的は炎症の制御、二次感染の防止、潰瘍の治癒促進、穿孔の防止である。
人工涙液・涙点プラグ :ドライアイ の治療と上皮化促進に用いる。防腐剤フリー製剤が推奨される抗菌薬点眼 :二次感染予防に使用するシクロスポリン 点眼局所ステロイド点眼 :角膜融解(keratolysis)を助長する可能性があるため、使用には細心の注意が必要であるドキシサイクリン 内服シアノアクリレート接着剤 :穿孔が切迫した場合に潰瘍底に塗布する5)
全身的な免疫抑制療法が治療の中心となる。
ステロイド全身投与 :プレドニゾロン1〜1.5mg/kg/日で開始する。メチルプレドニゾロンパルス療法(1g/日×3日間)を施行する場合もある免疫抑制薬(ステロイド温存薬) :穿孔切迫例・ステロイド不応例・RA合併例ではステロイド温存を目的に導入する。メトトレキサート 、アザチオプリン 、ミコフェノール酸モフェチル 、シクロスポリン、シクロホスファミドなどが選択される生物学的製剤 インフリキシマブ 、リツキシマブ 、アダリムマブ などの抗TNF -α抗体が使用される7) 。化膿性汗腺炎に伴うPUKではアダリムマブが有効であったとの報告がある7)
膠原病に併発する場合は原疾患の治療が最も重要であり、膠原病内科・リウマチ科と連携して治療を行う。
角膜穿孔または穿孔切迫例は外科的介入の適応となる。
層状角膜移植 (lamellar keratoplasty) :チェックポイント阻害薬関連PUKの穿孔例で層状ミニ角膜移植が施行された報告がある5) 結膜 切除術(Brown手術)角膜上皮形成術 :結膜切除後に露出した強膜 にドナー角膜の薄い上皮片を堤防状に縫着するTenon嚢スリンググラフト :進行したPUKで砂時計様角膜を呈する例に対し、修正Tenon嚢スリング環状パッチ移植が報告されている4) 。自家組織であり拒絶反応がない利点がある
結膜下デキサメタゾンインプラント(Ozurdex )の結膜下注射がPUKに対して奏効した症例が報告されている。全身的免疫抑制療法に耐えられない高齢患者において、3回の注射により11か月間にわたり強膜融解や眼圧 上昇なく炎症が制御された8) 。
Q PUKの治療でステロイド点眼は使えますか?
A 局所ステロイド点眼は角膜融解(keratolysis)を助長する可能性があるため、PUKの治療では慎重に使用する必要がある。治療の中心は全身的な免疫抑制療法であり、プレドニゾロンの全身投与やメトトレキサートなどの免疫抑制薬が用いられる。局所治療としてはシクロスポリン点眼やドキシサイクリン内服が推奨される。
視力予後は疾患の重症度と基礎疾患に依存する。周辺部角膜潰瘍や壊死性強膜炎を合併した場合、視力予後は不良であることが多い。全身疾患を伴う患者では血管系イベントによる生命予後にも注意が必要である。
化膿性汗腺炎に伴うPUKでは、治療中断後に穿孔した症例が報告されており3) 、治療の継続と多科連携の重要性が示されている。
PUKの病態は液性免疫と細胞性免疫の両方が関与する。自己免疫疾患における自己反応性抗体が産生する免疫複合体は、輪部血管に沈着して補体 系の古典経路を活性化する。補体活性化により好中球やマクロファージの走化性が誘導され、これらの炎症細胞がコラゲナーゼやプロテアーゼを放出する。
前炎症性サイトカイン(TNF-α、IL-6など)は角膜実質細胞(keratocyte)を刺激してマトリックスメタロプロテアーゼ(MMP)を産生させる1) 。粘膜類天疱瘡は角膜周辺部のコラーゲンを分解し、角膜菲薄化と潰瘍形成を進行させる。
近年、Th17細胞とIL-17の役割が注目されている1) 。TGF-β1・IL-6・IL-21などのサイトカインがTh17分化を促進し、IL-1がTh17の分化をさらに刺激する。Th17が分泌するIL-17は粘膜類天疱瘡産生を増強し、角膜実質の分解を促進する1) 。Th17の抑制がPUKの眼合併症を軽減するとの報告がある1) 。
肉芽腫性酒さでは表皮からIL-37が放出され、肥満細胞を活性化してキマーゼ・トリプターゼ・粘膜類天疱瘡などのプロテアーゼを放出させる1) 。この炎症微小環境がTh17偏向を促し、PUK発症につながると考えられている1) 。
角膜輪部は角膜上皮と結膜上皮の境界部であり、血管系・免疫系・神経系が密集した領域である。輪部にはランゲルハンス細胞が豊富に存在し、抗原提示に関与する。この解剖学的特性により、免疫複合体が沈着しやすく、免疫関連の角膜疾患が生じやすい。膠原病に伴う周辺部潰瘍では、免疫複合体が角膜輪部〜周辺部に沈着してIII型アレルギー反応を惹起し、浸潤した免疫細胞から放出される細胞外基質分解酵素が潰瘍形成に関与する。
Q なぜ角膜の周辺部に病変が生じるのですか?
A 角膜輪部は血管網・免疫系・神経系が密集した領域であり、ランゲルハンス細胞も豊富に存在する。中央角膜は無血管であるのに対し、周辺部は輪部血管網から免疫複合体や炎症細胞が供給されやすい。自己免疫疾患では免疫複合体が輪部血管に沈着して補体系を活性化し、好中球やマクロファージが集積して角膜実質を破壊するため、病変は周辺部に好発する。
免疫チェックポイント阻害薬(ICI)の普及に伴い、irAEとしてのPUKが報告されている。イピリムマブ(抗CTLA-4抗体)とニボルマブ(抗PD-1抗体)の併用療法では、irAEの発症率が90%超とされる5) 。ICI関連PUKは高用量ステロイド点眼やシクロスポリン点眼に抵抗性を示すことがあり、層状角膜移植が必要となった例も報告されている5) 。腫瘍治療の継続とirAE管理の両立が課題である。
全身的免疫抑制療法に耐えられない患者に対し、結膜下デキサメタゾンインプラント(Ozurdex)の結膜下注射が試みられている8) 。反復投与により長期的な炎症制御が達成され、強膜融解や眼圧上昇を認めなかった8) 。全身副作用を回避できる局所治療として今後の検証が期待される。
Th17/IL-17経路がPUKの病態に深く関与することから、Th17を標的とした治療が注目されている。肉芽腫性酒さに合併したPUKに対しイソトレチノインが奏効した症例では、イソトレチノインのTh17抑制作用と制御性T細胞促進作用が関与した可能性が示唆されている1) 。
進行したPUKに対する修正Tenon嚢スリンググラフトが報告されている4) 。自家組織であるため拒絶反応がなく、ドナー角膜が入手困難な状況でも施行可能である4) 。
Hsiao FC, Meir YJ, Hsiao CH, et al. Peripheral ulcerative keratitis in a patient with granulomatous rosacea. Taiwan J Ophthalmol. 2023;13(1):80-83.
Uchida S, Kaji Y, Ui M, et al. Peripheral ulcerative keratitis associated with large vessel vasculitis. Cureus. 2021;13(6):e15767.
Dallalzadeh LO, Ang MJ, Beazer AP, Spencer DB, Afshari NA. Peripheral ulcerative keratitis secondary to severe hidradenitis suppurativa. Am J Ophthalmol Case Rep. 2022;25:101403.
Anitha V, Ghorpade A, Ravindran M. A modified Tenon’s sling annular graft for advanced peripheral ulcerative keratitis with an hourglass cornea. Indian J Ophthalmol. 2022;70(2):655-657.
Aschauer J, Donner R, Lammer J, Schmidinger G. Bilateral corneal perforation in Ipilimumab/Nivolumab-associated peripheral ulcerative keratitis. Am J Ophthalmol Case Rep. 2022;28:101686.
Hsieh HH, Shen EP. Peripheral ulcerative keratitis secondary to chronic Citrobacter koseri canaliculitis. Taiwan J Ophthalmol. 2023;13(3):376-379.
Acharya I, Jalloh MI, Trevisan CD, Haas CJ. Hidradenitis suppurativa and peripheral ulcerative keratitis. J Community Hosp Intern Med Perspect. 2024;14(6):89-93.
Ghoraba HH, Or C, Ahluwalia A, et al. Subconjunctival dexamethasone implant (Ozurdex) for peripheral ulcerative keratitis. Am J Ophthalmol Case Rep. 2025;39:102379.
Campagne O, Vinet E, Engel L, et al. Ocular manifestations of inflammatory bowel disease. Ocul Surf. 2023;29:326-339.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください