先天性角膜混濁
Peters異常:角膜内皮・Descemet膜・実質の一部が欠損し、中央部に円板状混濁を呈する。約80%が両眼性であり、50〜70%に緑内障を合併する。
強膜化角膜:角膜周辺部または全体が強膜様に白濁する先天異常である。
CHED:先天性遺伝性角膜内皮ジストロフィ。出生時から両眼性の角膜浮腫・混濁を認める。
PPMD:後部多形性角膜ジストロフィ。小児期に発症し、20〜30%で角膜浮腫を生じる。

小児全層角膜移植術(pediatric penetrating keratoplasty: PKP)は、18歳未満の患者に対して行われる全層角膜移植術である。混濁した角膜全層をドナー角膜に置換し、視力の改善または眼球構造の維持を目的とする。
米国眼球バンク協会(EBAA)のデータによると、小児の角膜移植では角膜拡張症・菲薄化が最も多い適応であり、次いで先天性混濁が多い。一方、世界的には感染性角膜炎や化学・機械的外傷が主要な適応となっている。
視覚発達の臨界期は生後2〜6か月であり、片眼性の混濁では臨界期がさらに短い。小児角膜専門医の間では、生後1〜3か月での手術介入が推奨されている。ただし、生後0〜90日と3〜12か月で手術した群を比較した研究では、視力と移植片生着率に有意差を認めなかったとの報告もある。
近年では、特定の疾患に対してDSEK(デスメ膜剥離角膜内皮移植術)やDALK(深層前部層状角膜移植術)が小児にも成功裏に施行されており、全層移植に代わる選択肢が拡大しつつある。
小児は成人と比べて強膜の剛性が低く術中の眼球虚脱リスクが高い。術後の炎症反応も強く、組織収縮による縫合糸の緩みが生じやすい。移植片不全率は成人より高く、弱視管理も必要となる。また全身麻酔が必須であり、術後の点眼コンプライアンスの確保も課題である。
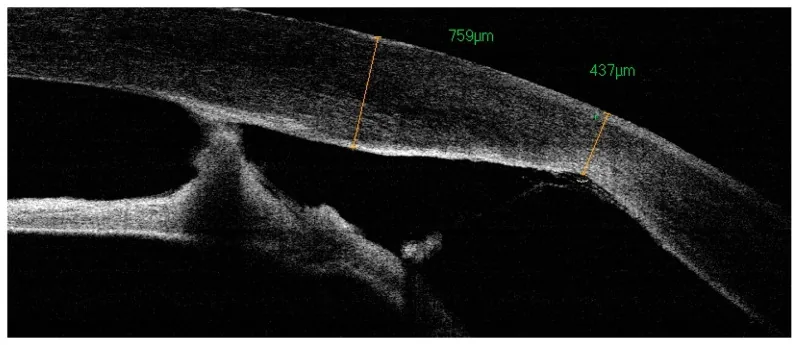
角膜混濁の範囲・深度・原因により所見は多彩である。
先天性角膜混濁
Peters異常:角膜内皮・Descemet膜・実質の一部が欠損し、中央部に円板状混濁を呈する。約80%が両眼性であり、50〜70%に緑内障を合併する。
強膜化角膜:角膜周辺部または全体が強膜様に白濁する先天異常である。
CHED:先天性遺伝性角膜内皮ジストロフィ。出生時から両眼性の角膜浮腫・混濁を認める。
PPMD:後部多形性角膜ジストロフィ。小児期に発症し、20〜30%で角膜浮腫を生じる。
後天性角膜混濁
外傷性:裂傷後の瘢痕、角膜血染。小児の角膜外傷は予後不良となりやすい。
感染性:単純ヘルペスウイルス角膜炎、細菌性・真菌性角膜炎による混濁。薬物治療に抵抗する場合が適応となる。
非感染性:円錐角膜(進行例)、Stevens-Johnson症候群、神経栄養性角膜炎。
分娩時外傷:鉗子分娩によるDescemet膜破裂。通常は片眼性(左眼に多い)で、垂直方向の線状混濁と乱視を残す。
| 疾患 | 特徴 |
|---|---|
| 先天緑内障 | 巨大角膜、Haab線条を伴う |
| 分娩時外傷 | 片眼性の垂直線状Descemet膜破裂 |
| 先天白内障 | 水晶体混濁。角膜は透明 |
全層角膜移植術の利益がリスクを上回るかを慎重に評価する。代替術式(角膜内皮移植術、深層層状角膜移植術)や部分虹彩切除術の可能性を検討する。
片眼性の角膜混濁では、手術を行わず経過観察とする選択肢もある。術後管理の困難さと成功率の低さから、片眼性疾患には手術を推奨しない外科医もいる。一方で、両眼視の機会を確保する意義を重視する見解もある。
保護者には術後に頻回(最初の数日間は1時間おき)のステロイド点眼が必要であること、頻回の通院が求められることを十分に説明する。
| 課題 | 対策 |
|---|---|
| 低い強膜剛性 | Flieringa ring使用 |
| 高い後方圧 | 頭部挙上、眼球マッサージ |
| 柔軟な組織 | 小さなドナー(5.5〜7 mm) |
ドナーグラフトはホスト角膜より0.5〜1 mm大きく作成する。縫合は10-0ナイロンによる結節縫合・連続縫合またはその組み合わせを用いる。全身麻酔下で施行し、スキサメトニウムやケタミンの使用は避ける。
小児は成人より強い炎症反応を示す。フィブリン放出の増加により虹彩角膜癒着が生じうる。組織収縮に伴う縫合糸の緩みは、縫合糸膿瘍や新生血管の原因となり、拒絶反応や移植片不全につながる。
術後早期は最低でも週2〜3回、その後数か月間は週1回の通院が必要である。保護者はペンライトで毎日角膜を観察し、縫合糸の緩みや新しい浸潤を発見したら速やかに受診する。ステロイド点眼は指示通りに継続し、自己判断で中止しないことが重要である。眼をこすらないよう注意し、弱視治療も並行して行う。
小児全層角膜移植術の予後は慎重であり、成人より成功率が低い。移植片不全の主な原因は拒絶反応と感染である。移植片が透明に維持されても、弱視による視力不良が高率に生じる。
先天性角膜混濁は後天性と比べて予後不良であり、特にPeters異常・強膜化角膜・子宮内感染に対する移植では、1年後の透明生着率が約3分の1にとどまる。手術時年齢が高いほど予後は良好であり、1歳未満の乳児では1年後の透明生着率が25%にすぎないとの報告がある。4歳以上の小児では約3分の2が1年後に透明を維持する。
小児PKの成功率は原因疾患と手術時年齢に大きく依存する。後天性角膜混濁では70〜87%の透明生着率が報告されているが、先天性角膜混濁では29〜60%と低い。特にPeters異常などの先天性疾患では1年後の透明生着率が約3分の1にとどまる。また、移植片が透明でも弱視により視力改善が得られないことがあり、視能訓練が極めて重要である。
Peters異常は胎齢6週以降の神経堤細胞の遊走異常に起因する。角膜内皮、Descemet膜、角膜実質の一部が欠損し、中央部に円板状の混濁を生じる。角膜虹彩癒着(1型)や角膜水晶体癒着(2型・3型)を伴う。約50〜70%に緑内障を合併する。
強膜化角膜は発生期における角膜と強膜の分化異常に起因する。角膜周辺部または全体が強膜様組織を呈し、輪部が不明瞭となる。
CHEDは角膜内皮細胞の機能異常により、出生時から両眼性の角膜浮腫・混濁を生じる。
小児の移植片不全率が成人より高い理由は以下の通りである。
小児の免疫応答は成人より活発であり、内皮型拒絶反応の頻度が高い。内皮型拒絶反応では移植片内に限局する角膜後面沈着物やKhodadoust line(拒絶反応線)を認め、実質浮腫を伴う。発見が遅れると移植片機能が不可逆的に喪失する。
加えて、小児では組織の創傷治癒が活発であるため、移植片とホストの接合部で組織収縮が生じやすい。この収縮が縫合糸の緩みを引き起こし、緩んだ縫合糸が感染巣や拒絶反応の誘因となる。