臨床検査
細隙灯顕微鏡検査:Vogtの柵の消失を直接観察できる1)。フルオレセイン染色で渦巻き状上皮症や結膜化の範囲を評価する1)。
印象細胞診:セルロースアセテートフィルターで眼表面上皮を採取する1)。杯細胞の存在は結膜化を示す1)。LSCDの診断における一つの基準とされるが、標本品質にばらつきがある1)。

角膜輪部同種移植(keratolimbal allograft:KLAL)は、輪部幹細胞欠損症(limbal stem cell deficiency:LSCD)を治療するための眼表面幹細胞移植(OSST)の一種である。死体ドナーから提供された角膜強膜キャリアに付着した同種輪部組織を移植し、角膜上皮の恒常性を回復させる。
LSCDでは角膜上皮幹細胞が障害され、角膜上皮が結膜上皮に置換される1)。この結膜化により角膜の透明性が失われ、視力低下・瘢痕化・新生血管が生じる1)。角膜移植単独ではLSCDの治療は無効であり、反復する表面破綻と上皮治癒障害によりグラフト不全に至る2)。
KLALは以下の症例に適応される。生体ドナーのいない両眼性LSCD。片眼性LSCDで健眼がドナーとして不適当な場合。無虹彩症やコンタクトレンズ関連LSCDなど、結膜の関与が少ないLSCD。
歴史的には、1984年にThoftが角膜上皮移植術を報告した。1990年にTurgeonとThoftが輪部組織を含む改良術式を報告し、これが記録に残る最初のKLALである。
自家移植(CLAu、SLET)は片眼性LSCDに対し健眼から輪部組織を採取するため、免疫抑制が不要であることが利点である。一方、KLALは死体ドナーの同種組織を使用するため全身免疫抑制が必要となるが、両眼性LSCDや健眼がドナーに適さない症例でも施行可能である。系統的レビューでは、自家CLAuの解剖学的成功率は81%、SLETは78%であった2)。
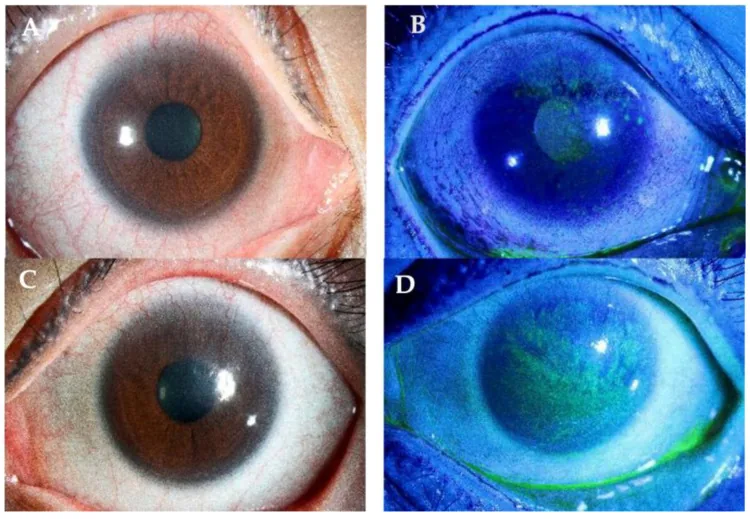
LSCDの患者は視力低下を主訴とする。角膜の結膜化と瘢痕化による透明性喪失が原因である。持続性角膜上皮欠損を生じた場合は眼痛を伴う。羞明や流涙も認められる。
LSCDの臨床像は重症度により異なる1)。
| LSCD重症度 | 臨床所見 |
|---|---|
| 軽度 | 渦巻き状上皮症 |
| 中等度 | 表在性新生血管・パンヌス |
| 重度 | 全周性結膜化 |
軽度のLSCDではフルオレセイン染色で渦巻き状(whorl-like)の上皮症を認める1)。中等度では表在性角膜新生血管と周辺部パンヌスが出現する1)。重度では全周性の結膜化により角膜全体が結膜上皮に置換される1)。
LSCDの重症度分類では、臨床グレーディングに基づき軽度(2〜4点)、中等度(5〜7点)、重度(8〜10点)に分類される1)。基底上皮細胞密度はコントロール眼で9,252 cells/mm²であるのに対し、重度LSCD眼では2,821 cells/mm²まで低下する1)。
LSCDは輪部幹細胞が障害されることで発生する。最も多い原因は無虹彩症(30.9%)であり、化学熱傷(20.6%)、コンタクトレンズ(16.8%)、SJS(10.4%)が続く1)。片眼性の場合は化学熱傷が最多である1)。
| 原因カテゴリ | 代表的疾患 |
|---|---|
| 外傷性 | 化学熱傷、CL使用 |
| 免疫性 | SJS、粘膜類天疱瘡、GVHD |
| 遺伝性 | 無虹彩症 |
緑内障手術はLSCDのリスク因子である1)。線維柱帯切除術や房水シャント手術による直接的な機械的外傷が輪部幹細胞を損傷する1)。代謝拮抗薬(マイトマイシンC、5-FU)の併用も輪部微小環境に影響する1)。LSCD患者の35%が緑内障または高眼圧症を合併していたと報告されている1)。
化学熱傷では輪部角結膜に存在する角膜上皮幹細胞が障害される。Vogtの柵(palisades of Vogt)の消失は角膜上皮幹細胞の障害程度を反映する。
LSCDの診断は臨床所見と画像検査の組み合わせによる1)。
臨床検査
細隙灯顕微鏡検査:Vogtの柵の消失を直接観察できる1)。フルオレセイン染色で渦巻き状上皮症や結膜化の範囲を評価する1)。
印象細胞診:セルロースアセテートフィルターで眼表面上皮を採取する1)。杯細胞の存在は結膜化を示す1)。LSCDの診断における一つの基準とされるが、標本品質にばらつきがある1)。
画像検査
生体共焦点顕微鏡:角膜上皮と結膜上皮の形態学的違いを観察できる1)。角膜上皮は大型多角形の扁平細胞であり、結膜上皮は立方形で高反射性の細胞質を有する1)。
前眼部OCT(AS-OCT):非接触で迅速な評価が可能である1)。角膜の結膜化の範囲や上皮厚の変化を評価できる。
全身麻酔または球後麻酔下で施行する。360°の輪部結膜切開(peritomy)を行い、角膜表面から線維血管性パンヌスと異常上皮を除去する。2つのドナー角膜強膜リムから中心角膜を切除し、三日月形の輪部組織(クレセント)を4つ作製する。各クレセントの後面半分を層状剥離で除去し、通常3つのクレセントを受容体角膜の周囲に配置する。10-0ナイロン糸と組織接着剤で固定する。
ドナー組織選択の基準として、60歳未満の若年ドナー、死亡から保存までの時間の最小化、死亡から5日以内の移植が推奨される。
KLAL後のグラフト長期生存には全身免疫抑制が不可欠である。Cincinnati OSSTPプロトコルでは、経口タクロリムス4 mg 1日2回とMMF 1 g 1日2回を手術1〜2週間前から開始する。術後に経口プレドニゾン1 mg/kg/日を追加し、1〜3か月で減量する。眼表面が安定した患者では、術後12〜18か月からタクロリムスを、術後3年からMMFを段階的に減量する。
KLAL転帰
安定した眼表面:適切な3剤併用免疫抑制下で73〜77%が達成される。平均4.5〜4.7年のフォローアップでの報告である。
グラフト不全の分類:一次不全(術後1週以内の上皮化不全)、部分不全(結膜化と健常上皮が混在)、全不全(全周性LSCD再発)、後期不全(慢性拒絶反応に起因)がある。
不全のリスク因子:角化、ドライアイ、瞼球癒着、慢性炎症、過去の拒絶反応が挙げられる。
自家LSCT術式比較
CLAu(結膜輪部自家移植):解剖学的成功率81%、機能的成功率74.4%2)。KenyonとTsengにより1989年に初めて報告された2)。
SLET(簡易輪部上皮移植):解剖学的成功率78%、機能的成功率68.6%2)。CLAuと同等の成績であった2)。
CLET(培養輪部上皮移植):解剖学的成功率61.4%、機能的成功率53%であり、CLAuとSLETに劣った2)。
全身免疫抑制は通常、術後12〜18か月からタクロリムスを、術後3年からMMFを段階的に減量する。眼表面が安定し拒絶反応の既往がなければ、最終的に中止できる場合がある。しかし拒絶反応の既往がある場合は低用量の免疫抑制を無期限に継続する必要がある。臓器移植の専門医との連携が推奨される。
KLALの主な目的は安定した眼表面の確立であり、直接的な視力改善ではない。しかし角膜表面が安定した後に光学的角膜移植(PKPまたはDALK)を追加することで、視力の回復が期待できる。KLAL後のDMAK+allo-SLET施行例では矯正視力が20/200から20/40に改善した報告がある3)。
輪部幹細胞は輪部基底層のVogtの柵に存在する1)。これらの幹細胞は求心性に移動し、まず基底上皮細胞に分化した後、増殖して表面方向へ移動して脱落する1)。輪部はまた、結膜の角膜への侵入に対するバリアとしても機能する1)。
LSCDでは輪部幹細胞の障害により角膜上皮が結膜上皮に置換され、角膜の透明性が失われる。わずか7%の輪部幹細胞が残存していれば、現代の手術手技により角膜上皮を再増殖させることが可能である。1)
長期の眼疾患では、炎症性サイトカインと粘膜類天疱瘡の複合作用により輪部幹細胞の微小環境が変化する1)。水疱性角膜症に合併するLSCDでは、角膜新生血管のない眼では上皮化まで約6日であるのに対し、新生血管のある眼では約29日を要する1)。
角膜上皮と結膜上皮は形態学的に異なる1)。正常角膜上皮は大型多角形の扁平細胞で構成され、基底層は低反射性の細胞質と明瞭な境界を有する1)。結膜上皮は立方形でより高反射性の細胞質を有し、杯細胞を含む1)。サイトケラチン3は角膜上皮に、サイトケラチン19は結膜上皮に特異的とされる1)。
KLAL不全後の救済として、脱細胞化デスメ膜を用いた前層角膜移植(DMAK)と同種簡易輪部上皮移植(allo-SLET)の併用が報告されている3)。デスメ膜はヒト羊膜(HAM)と比較して分解に対する抵抗性が高く、高濃度コラゲナーゼ浸漬で24時間以上耐えるのに対しHAMは30分で分解される3)。
デスメ膜上で培養された輪部幹細胞は、HAM上と比較して幹細胞マーカー(ABCG2、p63)の発現がより良好であったと報告されている3)。自己免疫性多腺症候群に伴うLSCDでKLAL拒絶後にDMAK+allo-SLETを施行した症例では、矯正視力が20/200から20/40に改善し、1.5年間上皮欠損の再発なく経過した3)。
デスメ膜は透明性・耐久性・輪部幹細胞培養基質としての優位性を有し、KLAL不全後の救済手段として有望である。ただし、長期的な有効性と免疫応答についてはさらなる検討が必要である。3)
LSCDの診断においても進歩がみられる1)。生体共焦点顕微鏡とAS-OCTの精度向上により、LSCD重症度の客観的評価と治療効果のモニタリングが改善されつつある1)。無虹彩症においては遺伝子解析の進展が予後予測と管理に寄与する可能性がある1)。