
共焦点顕微鏡(生体角膜共焦点顕微鏡)
ひとめでわかるポイント
Section titled “ひとめでわかるポイント”1. 共焦点顕微鏡とは
Section titled “1. 共焦点顕微鏡とは”共焦点顕微鏡は、照明光と観察光が同一の焦点面を共有する光学原理に基づく高解像度顕微鏡である。1957年にMarvin Minskyがその原理の特許を取得した7)。眼科領域では1990年にCavanaghらが初めてヒト生体角膜の共焦点観察を報告し、臨床応用が始まった7)。
現在臨床で使用される主な機器は以下の2系統である。
レーザー走査型(HRT III-RCM):Heidelberg Engineering社製。670 nmダイオードレーザーを光源とし、対物レンズ63倍、観察視野400×400 μmである。側方分解能1〜2 μm、深度分解能約4 μmと高い解像力を持つ1)2)。PMMA製ディスポーザブルキャップ(TomoCap)と眼科用ジェルを介して角膜に接触させて使用する。
スリットスキャン型(Confoscan 4):Nidek社製。ハロゲン光源を用い、非接触でも使用可能である。自動スキャン機能を備え操作が比較的容易だが、深度分解能は25〜27 μmにとどまる。現在は製造中止となっている。
IVCMは3つの撮像モードを備える。セクションスキャンは単一深度の静止画を取得する。ボリュームスキャンは2 μm間隔で30〜40枚の連続断面を取得する。シーケンススキャンは同一深度で最大100フレームの動画を取得し、動的変化の観察に適する。
IVCMは専用機器と操作に習熟した検者を要するため、大学病院や専門眼科施設を中心に導入されている。すべての眼科で受けられる検査ではないが、角膜感染症や角膜ジストロフィの診断に特に有用であり、必要に応じて紹介される。
2. 主な所見と臨床的意義
Section titled “2. 主な所見と臨床的意義”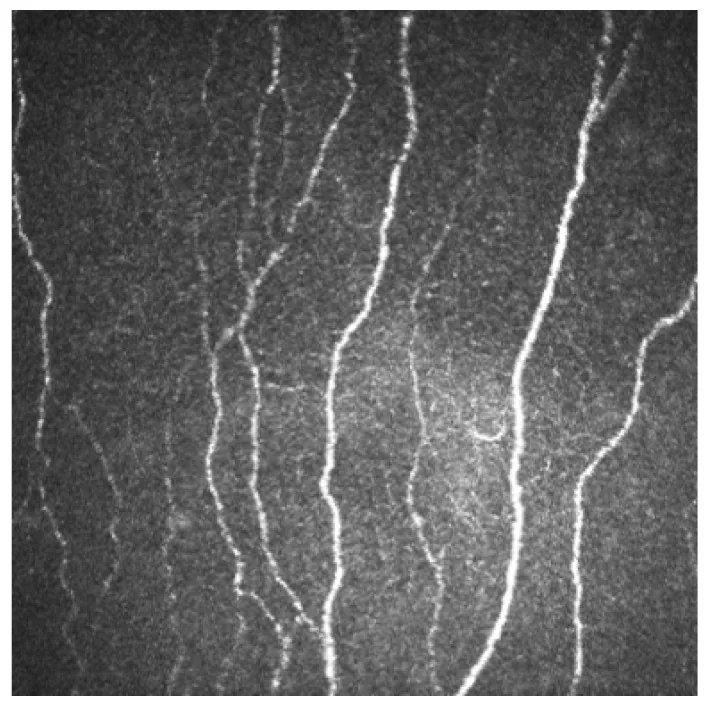
正常角膜の所見
Section titled “正常角膜の所見”IVCMでは角膜の各層を個別に観察できる。
角膜上皮:表層細胞は多角形で40〜50 μm。翼細胞は20〜30 μmで明るい細胞境界を持ち、約5,000 cells/mm²である。基底細胞は8〜10 μmで暗い細胞質と明るい境界(デスモソーム)を示し、蜂巣状パターンを呈する。基底細胞密度は3,600〜8,996 cells/mm²である。
ボーマン膜:厚さ約10 μmの無構造灰白色の層として観察される。神経束が走行する。
角膜実質:角膜実質細胞(ケラトサイト)が不活性状態では暗く、活性化状態では明るいアメーバ状に観察される。前方実質ほど細胞密度が高い。
デスメ膜:厚さ6〜10 μmの霧状の層として認められる。細胞構造は通常識別できない。
角膜内皮:六角形の細胞がモザイク状に配列する。細胞径約20 μm、密度は2,550〜2,720 cells/mm²で加齢に伴い年間約0.6%減少する。
サブベーサル神経叢:ボーマン膜直下に走行するビーズ状の曲線構造として観察される3)。角膜中心の約1〜2 mm鼻下方に渦巻き状パターン(whorl pattern)を形成する。線維径は0.52〜4.6 μmである。
樹状細胞(ランゲルハンス細胞):角膜中央で34 ± 3 cells/mm²、周辺で98 ± 8 cells/mm²に分布する。免疫応答の指標となる。
角膜感染症:真菌性角膜炎では実質内にフィラメント状の菌糸が明瞭に観察される8)。アカントアメーバはシスト(二重壁構造の球形)として検出されるが、炎症細胞との鑑別には経験を要する8)。細菌は個々の菌体が小さすぎるため直接の可視化は困難である5)。
角膜ジストロフィ:Avellino角膜ジストロフィ(GCD2)では基底上皮層に高輝度顆粒状沈着、浅層〜中層実質に不整形の高輝度クラスターが認められる1)。格子状角膜ジストロフィI型では網状の沈着物と分岐する線維が特徴的である1)。斑状角膜ジストロフィでは境界不明瞭な沈着物がみられ、Schnyder結晶状角膜ジストロフィでは針状結晶が観察される1)。
角膜拡張症:円錐角膜ではケラトサイト密度の低下がみられ、重症度と相関する。ボーマン膜の断裂も認められる。PRK後角膜拡張ではボーマン膜の欠損と前方ケラトサイトの減少が特徴であり、円錐角膜とは異なるIVCMパターンを示す2)。
3. 検査手技と方法
Section titled “3. 検査手技と方法”IVCMの検査手順は以下のとおりである。
前処置:点眼麻酔(オキシブプロカインなど)を施行する。ディスポーザブルTomoCap(PMMA製)に眼科用ジェルを塗布し、対物レンズ先端に装着する。
検査実施:CCDカメラでレンズ−角膜間の接触状況をモニタリングしながら角膜をアプラネーションする。手動でフォーカスを調整し、角膜表層(0 μm)から深層へ順次観察する。固視は非常に重要で、被検者の協力が不可欠である。検査時間は5〜15分程度である。
合併症:角膜上皮擦過、感染(既存の上皮欠損がある場合にリスクが高い)がまれに生じうる。
| 項目 | HRT III-RCM | Confoscan 4 |
|---|---|---|
| 光源 | ダイオードレーザー | ハロゲン光 |
| 深度分解能 | 4 μm | 25〜27 μm |
| 接触 | 要(TomoCap) | 不要も可 |
点眼麻酔を行うため、検査中の痛みはほとんどない。角膜にキャップが軽く接触する感覚がある程度である。検査後に一時的な異物感を生じることがあるが通常は速やかに消退する。
4. 光学原理と装置の特徴
Section titled “4. 光学原理と装置の特徴”共焦点顕微鏡の基本原理は「共焦点性(confocality)」にある7)。照明系と検出系の両方がピンホール開口部を持ち、対物レンズの焦点面からの反射光のみを選択的に検出する。焦点面外からの散乱光はピンホールで遮断されるため、高いコントラストと深度分解能が得られる。
レーザー走査型(HRT III-RCM)では670 nmダイオードレーザーが点光源として機能し、角膜上を点ごとに走査して画像を構築する。焦点面の厚さ(光学切片厚)は約4 μmときわめて薄く、細胞レベルの鮮明な断面像を提供する。
スリットスキャン型(Confoscan 4)ではスリット状の光線で走査するため、スリットに垂直な方向でのみ真の共焦点性が得られる。そのため深度分解能は25〜27 μmとなり、レーザー走査型に比べ画像の鮮鋭度は劣る。
IVCMの限界として、グレースケール画像のみ(カラー観察不可)、細胞内構造の分解不能、高度角膜混濁例での観察困難、観察部位の正確な位置特定が困難、検者の技量への依存が挙げられる。
5. 主な臨床応用
Section titled “5. 主な臨床応用”IVCMの臨床応用は多岐にわたる。
角膜感染症の診断補助:培養検査の補助として有用である。真菌の菌糸やアカントアメーバのシストを検出できるが、観察所見の判読には専門的知識が必要である8)。ヘルペス角膜炎では角膜神経の変化を捉えることができる8)。サイトメガロウイルス角膜内皮炎ではowl’s eye封入体を認めることがある。
角膜ジストロフィの鑑別:各ジストロフィに特徴的なIVCM所見がありパターン認識による非侵襲的な鑑別が可能である1)。遺伝子検査や生検に先立つスクリーニングとして有用性が高い。治療(PTK、DALKなど)後の効果判定にも応用できる1)。
輪部幹細胞疲弊症(LSCD)の評価:Vogtの柵状構造の消失、結膜上皮による角膜上皮の置換、杯細胞の出現が診断の根拠となる6)。基底上皮細胞密度の測定でLSCDの重症度を定量評価できる6)。
角膜浮腫・内皮疾患の評価:IVCMは中等度の角膜浮腫を通しても内皮細胞を観察できるため、スペキュラーマイクロスコピーが撮影困難な症例で特に有用である7)。Fuchs角膜内皮ジストロフィ(FECD)では内皮細胞の評価に加え、神経密度の低下や樹状細胞密度の変化も捉えられる7)。
角膜神経の評価:サブベーサル神経叢の定量評価は神経栄養性角膜症の診断と治療効果判定に用いられる3)。角膜神経移植術(surgical corneal neurotization)後の神経再生評価では、IVCMで術後6か月〜1年で再生所見が確認される3)。
全身性自己免疫疾患の早期発見:Sjögren症候群では角膜中央の神経線維密度低下と活性化樹状細胞の増加が臨床発症に先行して検出されうる4)。中央角膜に3本以上の突起を持つ活性化樹状細胞が2個以上存在する場合、全身性免疫疾患に対する感度60%・特異度77%と報告されている4)。
術後評価:LASIK、PRK後のフラップ断端やボーマン膜の変化、神経再生の経過観察に利用される2)。角膜移植後の拒絶反応の早期検出にも応用がある。
6. 最新の研究と今後の展望
Section titled “6. 最新の研究と今後の展望”自動画像解析:ACCMetricsソフトウェアなど、サブベーサル神経線維の自動定量システムが開発されている2)。神経線維密度・分岐密度・屈曲度などのパラメータを客観的に算出し、検者間ばらつきを低減する。
疾患の前臨床段階の検出:Sjögren症候群の症例では、抗体陽性化や臨床症状出現の数年前にIVCM異常が検出された報告がある4)。IVCMが自己免疫疾患のスクリーニングツールとなる可能性が示唆されている。
ドライアイのサブタイプ分類:樹状細胞の形態と分布パターンの解析により、免疫介在性ドライアイと蒸発亢進型ドライアイを鑑別できる可能性がある4)。
術後神経再生のモニタリング:角膜神経移植術や角膜クロスリンキング後の神経再生過程をIVCMで経時的に追跡する研究が進んでいる3)。将来的には治療効果の客観的エンドポイントとしての活用が期待される。
人工知能の統合:深層学習を活用したIVCM画像の自動分類・自動診断システムの開発が進められており、感染症の迅速診断や角膜ジストロフィの自動鑑別への応用が期待される。
7. 参考文献
Section titled “7. 参考文献”
Ozturk HK, Ozates S, Ozkurt ZG, et al. In Vivo Confocal Microscopy in Avellino Corneal Dystrophy. Cureus. 2024;16(9):e68561.
Alvani A, Hashemi H, Pakravan M, et al. Corneal ectasia following PRK: a confocal microscopic case report. Arq Bras Oftalmol. 2024;87(6):e2023-0072.
Rathi VM, Basti S, Sangwan VS, et al. Neurotization of the human cornea – an overview with a detailed review of neurotization using direct nerve transfer. Indian J Ophthalmol. 2022;70(8):2773-2782.
Mercado CL, Galor A, Felix ER, et al. Confocal Microscopy Abnormalities Preceding Antibody Positivity and Manifestations of Sjogren’s Syndrome. Ocul Immunol Inflamm. 2023;31(5):1004-1009.
Austin A, Lietman T, Rose-Nussbaumer J. Update on the management of infectious keratitis. Ophthalmology. 2024;131(1):e51-e64.
Deng SX, Borderie V, Chan CC, et al. Global consensus on the definition, classification, diagnosis, and staging of limbal stem cell deficiency. Cornea. 2019;38(3):364-375.
Aggarwal S, Kheirkhah A, Cavalcanti BM, et al. In vivo confocal microscopy in Fuchs endothelial corneal dystrophy: a review. Eye Contact Lens. 2020;46(5):S46-S52.
日本眼感染症学会. 感染性角膜炎診療ガイドライン(第3版). 日眼会誌. 2023.
