BCS1型(ZNF469変異)
原因遺伝子:ZNF469(16q24)の単一エキソン遺伝子であり、3,953アミノ酸をコードする1)
報告患者数:53例(24種の変異が同定済み)1)
主な変異型:ホモ接合型のフレームシフト変異またはナンセンス変異が多い1)
特記事項:ヘテロ接合型変異は円錐角膜との関連が報告されている2)

脆性角膜症候群(Brittle Cornea Syndrome: BCS; OMIM 229200, 614170)は、進行性の角膜菲薄化と青色強膜を特徴とする稀な常染色体劣性遺伝の結合組織疾患である。1968年にSteinらにより初めて報告された2)。有病率は100万人あたり1人未満と推定されている1)。2021年時点で累計86例が報告されており、近親婚の家族歴を有する症例が多い1)。
BCSは原因遺伝子により2型に分類される1)。いずれの型も細胞外マトリックスの恒常性維持に関与する転写因子をコードする1)2)。コラーゲン沈着と線維集合の障害が角膜実質の構造的脆弱性を引き起こす1)。
BCS1型(ZNF469変異)
原因遺伝子:ZNF469(16q24)の単一エキソン遺伝子であり、3,953アミノ酸をコードする1)
報告患者数:53例(24種の変異が同定済み)1)
主な変異型:ホモ接合型のフレームシフト変異またはナンセンス変異が多い1)
特記事項:ヘテロ接合型変異は円錐角膜との関連が報告されている2)
BCS2型(PRDM5変異)
原因遺伝子:PRDM5(4q27)の16エキソン遺伝子であり、630アミノ酸をコードする1)
報告患者数:33例(14種の変異が同定済み)1)
主な変異型:すべてホモ接合型変異として報告されている1)
特記事項:網膜微小血管やブルッフ膜の発達にも関与する1)
BCSは以前、脊柱後側弯型エーラス・ダンロス症候群(EDS VI型)の一部と考えられていた。しかし分子遺伝学的解析により別の疾患であることが確認された1)。EDS VIはPLOD1遺伝子変異によるリシルヒドロキシラーゼ欠損が原因である。尿中のデオキシピリジノリン/ピリジノリン比上昇で鑑別でき、BCSではこの比率は正常である1)。EDS VIでは動脈破裂による生命予後の不良があるが、BCSの平均余命は正常とされている。
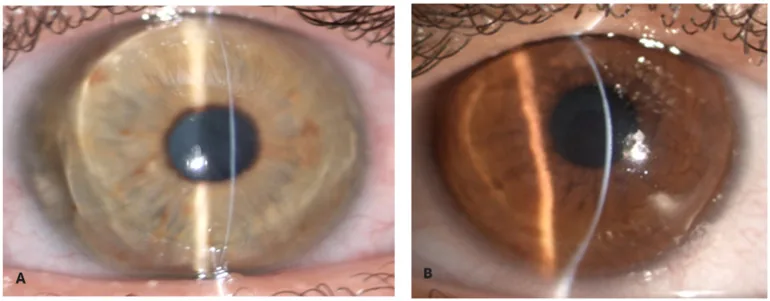
進行性の近視や不正乱視による視力低下が主訴となる3)。角膜穿孔時には突然の疼痛と視力喪失を来す5)。難聴による聴覚障害を自覚することもある1)。
角膜全体(輪部から輪部まで)の菲薄化が最も特徴的である。中心角膜厚(CCT)はしばしば400μm未満となる1)。3兄弟の報告では中心角膜厚が243〜304μmであった5)。アルバニア人姉弟では189μmおよび157μmであった3)。ニュージーランドの2兄弟ではそれぞれ167μmおよび149μmと極度の菲薄化が確認されている4)。
角膜穿孔は平均4.3歳で発症する(範囲1.5〜19歳)1)。報告症例の3分の2以上で眼球穿孔が認められている1)。半数以上で永続的な視力喪失が生じている1)。青色強膜は最も高頻度の眼所見であり、78例中72例で認められた1)。
| 系統 | 主な所見 | 頻度 |
|---|---|---|
| 眼 | 角膜菲薄化・穿孔、青色強膜 | >90%1) |
| 関節 | 小関節過可動性 | 64/78例1) |
| 聴覚 | 感音性・伝音性・混合性難聴 | 32/78例1) |
関節過可動性は最も高頻度の眼外所見である1)。先天性股関節形成不全、側弯症、扁平足も報告されている1)。難聴は高音域がより高度に障害される傾向がある1)。鼓膜の過コンプライアンスが特徴的である1)。皮膚は柔軟で過伸展性を示し易出血性を伴う1)。
骨脆弱性の報告も近年増加している。ZNF469複合ヘテロ変異の2兄弟で10回以上の骨折歴と骨減少症が認められた4)。BCS患者の約16%に骨脆弱性が存在する可能性が示唆されている4)。骨生検では皮質骨の菲薄化と皮質骨孔隙率の著明な低下が認められた4)。
BCSは2つの遺伝子の両アレル変異により発症する常染色体劣性遺伝疾患である1)。
ZNF469は前房と角膜の正常な発達に関与する1)。ゲノムワイド関連解析では中心角膜厚との関連が示されている4)。PRDM5は線維性コラーゲン遺伝子の転写を直接調節する4)。両遺伝子とも機能喪失型変異(フレームシフト変異・ナンセンス変異)が高頻度を占める1)。
ZNF469のヘテロ接合型変異は中心角膜厚の減少と関連する2)。しかし必ずしも角膜菲薄化を来すわけではない。64歳の中国人男性症例ではヘテロ接合型ZNF469変異で角膜厚が正常(約550μm)であったが、角膜混濁と上皮欠損を呈した2)。
近親婚は重要なリスク因子であり、ホモ接合型変異の発症確率を高める1)。トルコ系の3例ではPRDM5 c.17T>G, p.(Val6Gly)変異が共通しており、創始者変異の可能性が指摘されている1)。
角膜全体の菲薄化(中心角膜厚 400μm未満)と青色強膜に加え、関節過可動性や難聴などの全身症状により臨床診断を行う3)。角膜パキメトリーおよびPentacam等による角膜形状解析が不可欠である3)。前眼部OCTは角膜構造の詳細な評価に有用である2)3)。
確定診断にはZNF469およびPRDM5の遺伝子検査が必要である3)。全エクソーム解析(WES)は病原性バリアントの同定に有効である3)。遺伝カウンセリングと家族計画にも有用な情報を提供する3)。保因者では近視や軽度の角膜菲薄化を発症することがある2)。
| 鑑別疾患 | BCSとの相違点 |
|---|---|
| 脊柱後側弯型EDS | 動脈破裂リスク、尿中リシルピリジノリン比上昇1) |
| 骨形成不全症 | 繰り返す骨折が主徴、歯牙形成不全4) |
| マルファン症候群 | 大動脈解離、高身長、水晶体偏位 |
BCSでは脊柱後側弯型EDS(kEDS-PLOD1)との鑑別が特に重要である。kEDS-PLOD1で眼球破裂が生じる場合は角膜よりも強膜が破裂しやすい1)。kEDS-PLOD1では側弯症、筋緊張低下、血管合併症がより顕著である1)。
角膜穿孔の平均発症年齢は4.3歳であり、穿孔後の外科的修復は極めて困難である5)。報告症例の半数以上で永続的な視力喪失が生じている1)。早期診断により保護眼鏡の着用と外傷予防教育を講じることが可能となる1)。兄弟姉妹のスクリーニングも早期発見に重要である5)。
BCS管理の最重要項目は角膜穿孔の予防である1)。ポリカーボネート製保護眼鏡の常時着用が推奨される5)。予防的な眼圧降下薬の投与も考慮される。コンタクトレンズは角膜菲薄化と外傷リスクのため制限される1)。
全層角膜移植術(PKP)
適応:高度角膜菲薄化または穿孔後の視力回復に施行される3)
術式:8.0mmトレフィン使用、16本の10-0ナイロン断続縫合3)
成績:アルバニア人姉弟で最高矯正視力(BCVA)20/200→20/30および20/25に改善3)
経過:7年間合併症なく経過した3)
深層層状角膜移植術(DALK)
利点:内皮温存により拒絶反応リスクを低減できる3)
制限:実質の脆弱性により術中穿孔リスクがある3)
報告例:1例で術中に中心部内皮穿孔が生じPKPに変更された3)
選択基準:十分な実質厚とデスメ膜の健全性が必要である3)
角膜穿孔の修復術では組織の極度な脆弱性が問題となる。3兄弟の報告では長い縫合バイトの使用、シアノアクリレート接着剤とバンデージコンタクトレンズの併用が有効であった5)。強角膜トンネルの慎重な作成により合併症を軽減できる5)。64歳のBCS患者ではPKPが施行され退院時矯正視力は0.2であった2)。
中心角膜厚 280μm未満の小児BCS患者2例で経上皮CXL(角膜厚に応じたUV照射量調整)が施行された3)。視力改善と内皮細胞密度の維持が報告されている3)。ただし標準的なドレスデンプロトコルでは中心角膜厚 400μm以上が必要であり、200μm未満の極薄角膜では適応外となる3)。プロトコル修正により適用範囲の拡大が期待されるが、現時点では限定的である。
ZNF469およびPRDM5はいずれも転写因子をコードする1)。ZNF469はC末端に3つのC2H2型ジンクフィンガードメインを有する1)。細胞外マトリックス遺伝子(CLU、GPC6、PCOLCE2、THBS1)の発現を制御する1)。PRDM5はPR SETドメインを持ち、コラーゲン遺伝子の転写をRNAポリメラーゼIIとの結合を介して直接調節する4)。Wntシグナル経路の調節にも関与している。
これらの遺伝子変異により、角膜実質におけるコラーゲン沈着と線維集合が障害される1)。ZNF469変異ではI型コラーゲン(COL-I)の発現低下と構造変化が生じる2)。PKP後の角膜組織の免疫蛍光染色ではCOL-Iの減少とIII型コラーゲンの増加が実証された2)。マッソン染色でもコラーゲン線維量の明確な減少が認められている2)。
共焦点顕微鏡では前部角膜実質に高反射の線条状組織が網状に認められる2)。炎症細胞浸潤は伴わない2)。これはBCSの角膜病変がコラーゲン構造の一次的な異常に起因することを示唆する。
骨組織においてもPRDM5はI型コラーゲン遺伝子のエキソンDNAに結合する4)。骨生検では皮質骨の菲薄化と皮質骨孔隙率の著明な低下(1.3%;正常値6.3±0.6%)が認められた4)。28遺伝子の骨脆弱性パネルでは他の病原性変異は検出されず、ZNF469変異自体が骨脆弱性の原因である可能性が示唆されている4)。
ZNF469とPRDM5は全身の結合組織における細胞外マトリックスの転写調節に関与する1)。コラーゲン線維の構造異常は角膜に限定されず、強膜(青色変色)、関節(過可動性)、皮膚(過伸展性)、骨(骨減少症)、鼓膜(過コンプライアンス)など全身の結合組織に影響を及ぼす4)。骨減少症と骨折の報告もあり、BCSが骨脆弱性の表現型を有する可能性が指摘されている4)。
遺伝子治療の進歩がBCSに新たな可能性をもたらしつつある。CRISPRゲノム編集やRNA干渉(RNAi)は角膜菲薄化の安定化・改善を目的とした治療法として期待されている3)。
生体工学的角膜インプラント(BPCDX)は医療用ブタコラーゲンから作成された無細胞の透明ハイドロゲルである3)。フェムト秒レーザーで作成した2〜3mmの実質内ポケットに挿入する低侵襲手法である3)。24か月の観察で角膜厚の増加、最大ケラトメトリーの18D平坦化、矯正視力の改善が報告されている3)。拒絶反応なく安定した成績が得られている3)。
間葉系幹細胞の角膜実質内注入も研究されている3)。脂肪由来および骨髄由来幹細胞をフェムト秒レーザーによる層状切開部に注入する手法であり、PKPの延期を可能にする可能性がある3)。現時点では円錐角膜患者での使用にとどまるが、BCS患者への応用が期待される3)。