初期
放射状角膜神経炎:輪部から角膜中央へ向かう神経に沿った線状浸潤。アカントアメーバ角膜炎にきわめて特異的な所見である。
上皮・上皮下浸潤:点状・斑状・線状の混濁が集簇する。
偽樹枝状病変:フルオレセイン染色で辺縁がギザギザした不整な線状病変を認める。ヘルペスの樹枝状病変(terminal bulbあり)との鑑別が重要。
毛様充血と輪部浮腫:角膜病変が軽くても認められる。

アカントアメーバ角膜炎(Acanthamoeba keratitis; AK)は、土壌や淡水に広く生息する自由生活アメーバであるアカントアメーバが角膜に感染して発症する疾患である。1973年に初めて報告され、本邦では1988年に石橋らによる最初の症例報告がある。
原因となるのは主に Acanthamoeba castellanii と A. polyphaga の2種で、遺伝子型ではT4型が全症例の94.3%を占める4)。微生物角膜炎全体に占めるアカントアメーバ角膜炎の割合は約1.5%、発生率は100万人あたり約2.3眼と推定される。
アカントアメーバ角膜炎は重症のコンタクトレンズ(CL)関連角膜炎の主要原因の一つであり、患者の85〜90%がCL装用者である。ある症例対照研究では、再利用可能なデイリーケアレンズの使用はワンデーレンズに比べてアカントアメーバ角膜炎発症リスクが約3.8倍高いことが示された(OR 3.84; 95% CI 1.75–8.43)1)。アカントアメーバ角膜炎症例の約半数が視力障害に至るとされ、コンタクトレンズ使用者における重篤な角膜感染症として公衆衛生上の課題となっている1)。
CL装用者が大多数を占めるが、外傷や汚染された水への曝露を契機に非CL装用者でも発症する。インドなどでは外傷関連の症例が多い。
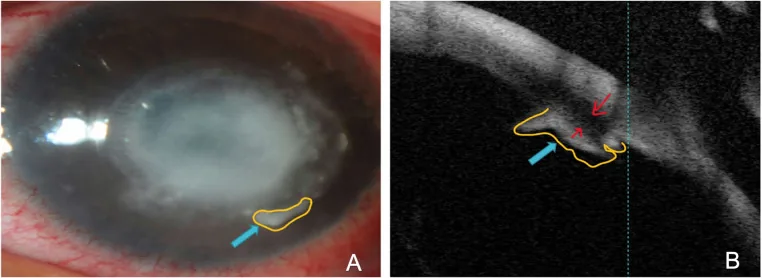
アカントアメーバ角膜炎の最も特徴的な症状は、臨床所見に不相応な激しい眼痛である。
アカントアメーバ角膜炎は緩徐に進行し、病期によって特徴的な臨床所見を呈する。本邦では初期・移行期・完成期の3期に分類されている。
初期
放射状角膜神経炎:輪部から角膜中央へ向かう神経に沿った線状浸潤。アカントアメーバ角膜炎にきわめて特異的な所見である。
上皮・上皮下浸潤:点状・斑状・線状の混濁が集簇する。
偽樹枝状病変:フルオレセイン染色で辺縁がギザギザした不整な線状病変を認める。ヘルペスの樹枝状病変(terminal bulbあり)との鑑別が重要。
毛様充血と輪部浮腫:角膜病変が軽くても認められる。
完成期
アカントアメーバは土壌、淡水、水道水、プール、シャワー水など至る所に存在する自由生活アメーバである。栄養体(活動形態)とシスト(二重壁を持つ休眠形態)の2つの形態をとり、シストは冷凍・加熱・放射線照射・各種薬剤に対して強い耐性を持つ。
CL装用に関連するリスク要因は以下の通りである。
多目的溶剤(MPS)のアカントアメーバに対する消毒効果はきわめて低い。アカントアメーバの増殖には餌となる細菌が必要であるため、こすり洗いの徹底による細菌汚染の予防が感染予防の鍵となる。
ワンデーレンズは再利用レンズに比べリスクは低い。しかし、シャワー中の装用やレンズの再利用といった行為があればリスクは上昇する1)。正しい使用法の遵守が不可欠である。
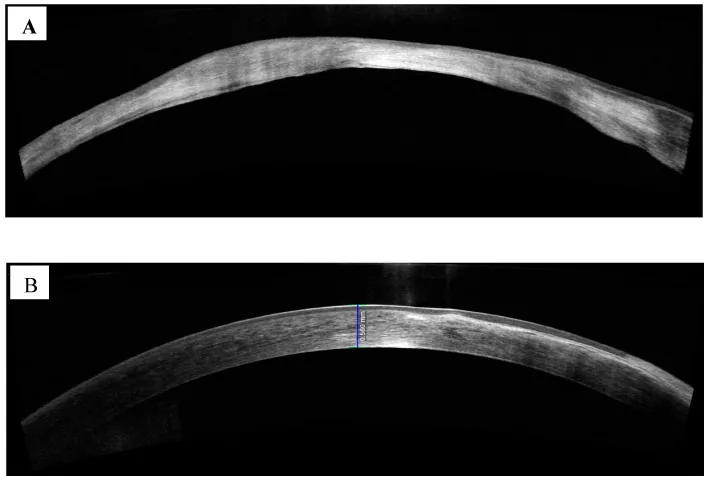
アカントアメーバ角膜炎の診断は困難であり、しばしば遅れる。ドイツのレジストリによれば、アカントアメーバ角膜炎症例の47.6%がヘルペス角膜炎と誤診されていた4)。正確な診断には臨床所見の正しい読み取りと微生物学的検査の組み合わせが不可欠である。
細隙灯顕微鏡所見による診断が重要である。病期に応じた特徴的所見(「臨床所見」の項参照)を把握し、CL装用歴や水への曝露歴と合わせて臨床的に疑うことが第一歩となる。
フルオレセイン染色所見は鑑別に有用であり、ヘルペスの樹枝状病変ではterminal bulb(末端の丸み)を形成するのに対し、アカントアメーバ角膜炎の偽樹枝状病変ではこれを欠き、隆起せず不整な線の集簇として観察される。
主な検査法の特性を以下に示す。
| 検査法 | 感度 | 特異度 |
|---|---|---|
| 培養(大腸菌塗布非栄養寒天培地) | 33〜50% | 100%(ゴールドスタンダード) |
| 共焦点顕微鏡(IVCM) | 約90% | 91.1〜100% |
| PCR(18S rRNA遺伝子) | 71〜84% | 100% |
初期の臨床所見がヘルペス角膜炎に類似し、偽樹枝状病変が樹枝状潰瘍と誤認されやすい。実際にアカントアメーバ角膜炎症例の約半数がヘルペスと誤診されたとの報告がある4)。CL装用者の治療抵抗性角膜炎ではアカントアメーバ角膜炎を積極的に疑い、早期に培養や共焦点顕微鏡を実施すべきである。
アカントアメーバ角膜炎の治療は困難であり、長期間を要する。アカントアメーバに保険適用のある薬剤は存在せず、治療には自家調整点眼液を使用する必要がある。日本の感染性角膜炎診療ガイドライン(第3版)では、自家調整剤点眼の使用を「強く推奨する」(エビデンスレベルB)としている。
わが国では、病巣掻爬・抗アカントアメーバ薬の局所投与・抗真菌薬の全身投与を組み合わせた三者併用療法が基本である。
治療において最も重要な手技である。その意義は以下の通りである。
アカントアメーバが寄生する角膜上皮は基底膜との接着が脆弱であり、一見健常に見える上皮も軽く擦過するだけで剥がれる。そのような上皮はすべて除去する。
第一選択薬はビグアナイド系消毒薬であり、以下のいずれかを自家調整して使用する。
これらは栄養体だけでなくシストにも効果を有するが、組織移行性は不良である。
補助的薬剤として以下が併用されることがある。
初期の集中治療では1時間ごとの頻回点眼を行い、臨床反応に応じて漸減する。治療は数ヶ月にわたることがほとんどである。
抗真菌薬の全身投与を併用する。イトラコナゾール内服が用いられるが、その効果は補助的である。
薬物治療に抵抗する症例や角膜穿孔を生じた症例では、治療的角膜移植(全層角膜移植術; PKP)が必要となることがある。可能であれば炎症が沈静化した後に施行するのが望ましい。活動性感染が残存する場合は術後に抗アメーバ治療を継続する必要がある。角膜移植後の再発リスクは高く、移植片不全も報告されている8)。
Carntら(2018)は194例の後方視的研究で、抗アメーバ治療開始前のステロイド使用が予後不良リスクを約4倍に高めることを報告した2)。予後不良例の25%は外来受診55回以上、経過観察58ヶ月以上を要した。
日本のガイドラインではアカントアメーバ角膜炎に対するステロイド点眼は推奨されていない。治療前のステロイド使用は予後不良因子である2)。ただし、炎症が持続する一部の症例では、抗アメーバ治療を十分に行った後に限定的に使用される場合がある。
アカントアメーバのライフサイクルには栄養体とシストの2段階がある。栄養体は運動性を持ち、角膜上皮表面のマンノシル化糖タンパクに接着して侵入を開始する。CL装用による角膜上皮の微小外傷がこの接着を促進する。シストは二重壁構造を持ち、冷凍・加熱・放射線照射・薬物に対して強い耐性を示す。このシストの耐性がアカントアメーバ角膜炎治療を困難にしている最大の要因である。
感染の進行過程は以下の通りである。
Kurbanyanらの共焦点顕微鏡を用いた研究では、活動性アカントアメーバ角膜炎において角膜神経の密度・長さ・分岐が有意に低下していることが報告されている4)。この神経変化が無痛性アカントアメーバ角膜炎の一因となる可能性がある。
オルソケラトロジー(OK)レンズに関しては、通常のRGPレンズよりもアカントアメーバ角膜炎発症リスクが高い。OKレンズ特有のリバースジオメトリーデザインが角膜上皮菲薄化と表面細胞障害を惹起し、夜間装用による角膜低酸素とリバースカーブ下の涙液プーリングが病原体のコロニー形成を促進すると考えられている3)。
従来の0.02% PHMBに対し、4倍濃度の0.08% PHMBを用いた単剤療法の検討が進んでいる。
Di Zazzoら(2024)は、0.02% PHMB+プロパミジン0.1%の標準療法に4〜6週間抵抗した2例に対し、0.08% PHMB単剤を世界で初めて臨床使用した5)。プロトコールは、最初の5日間は1時間ごと(日中のみ16滴/日)、以後段階的に減量する方式である。いずれの症例も15〜30日で感染が消退し、7ヶ月以上再発は認められなかった。
ODAK試験(Dartら2024)では、PHMB 0.08%単剤療法とPHMB 0.02%+プロパミジン0.1%併用療法の治癒率がいずれも約86%であったことが報告されている5)。
リボフラビンと紫外線A(UVA)を用いたクロスリンキングを感染性角膜炎に応用する手法である。
Watsonら(2022)は、最大限の薬物治療(ミルテフォシン、ボリコナゾール、PHMB、クロルヘキシジンを含む)に抵抗した難治性アカントアメーバ角膜炎の1例にPACK-CXLを施行し、4週間で疼痛が完全に消失し、10週間にわたり浸潤が縮小したことを報告した6)。
ただし、in vitro・in vivo実験ではリボフラビン/UVA照射のアメーバ・シスト殺傷効果は確認されていない6)。コラーゲン安定化による組織保護やアメーバ増殖抑制、上皮デブリドマンによるアメーバ量の減少、角膜神経密度低下による除痛効果などの間接的機序が推察されている。
アルキルフォスフォコリンに分類される薬剤で、栄養体とシストの双方に活性を有する。2016年に米国FDAからアカントアメーバ角膜炎治療の孤児薬指定を受けた。標準治療に4〜6週間抵抗した難治例に対する補助療法として位置づけられている6)7)。
Smithら(2022)の4症例シリーズでは、ミルテフォシンを含む多剤併用療法と角膜移植を組み合わせ、いずれの症例も最終的に病勢コントロールが得られた7)。しかし忍容性の問題(消化器症状)により途中で中止を要した症例もあった。
ミルテフォシンの主な副作用は消化器症状(悪心、嘔吐)、催奇形性、腎毒性であり、まれにStevens-Johnson症候群や重篤な血小板減少が報告されている7)。投与中は肝機能の定期的なモニタリングが必要とされる。