外因性眼内炎
急性術後型:白内障手術後が最多。術後6週以内に発症する。
遅発型(慢性術後型):手術後数週〜数ヶ月以上を経て発症。P. acnes などが原因となる。
外傷性:眼球穿孔創から病原体が直接侵入。成人の発生率0.9〜18%、小児では5〜54%に達する。2)
濾過胞関連・硝子体内注射後:抗VEGF薬投与後の発生が増加傾向にある。

眼内炎(Endophthalmitis)は、硝子体腔や前房を含む眼内液に炎症細胞が大量浸潤した化膿性炎症の総称である。進行が速く、適切な治療が遅れると短期間で不可逆的な視力障害に至る眼科救急の代表疾患である。
発症経路から大きく外因性と内因性の2つに分類される。
外因性眼内炎
急性術後型:白内障手術後が最多。術後6週以内に発症する。
遅発型(慢性術後型):手術後数週〜数ヶ月以上を経て発症。P. acnes などが原因となる。
外傷性:眼球穿孔創から病原体が直接侵入。成人の発生率0.9〜18%、小児では5〜54%に達する。2)
濾過胞関連・硝子体内注射後:抗VEGF薬投与後の発生が増加傾向にある。
内因性眼内炎
細菌性:菌血症の0.04〜0.5%に合併する。1) 肺・肝・心内膜炎など他臓器感染巣からの血行性播種。
真菌性:カンジダ属が多く、免疫抑制患者や長期中心静脈カテーテル留置例に発症しやすい。
K. pneumoniae関連:台湾での12年間データではEEの55.8%を占める。1) 糖尿病・肝膿瘍との関連が深い。
内因性眼内炎(Endogenous Endophthalmitis; EE)は菌血症症例の0.04〜0.5%に発症し1)、高病毒性型 K. pneumoniae(hvKP)による肝膿瘍(PLA)合併例では EE 発生率が3.4〜12.6%に達する。3)
白内障手術後が最も多いが、外傷・抗VEGF薬硝子体内注射・濾過胞関連など多様な外因性経路がある。さらに全身の感染巣から血液を介して眼内に播種する内因性眼内炎も存在し、糖尿病患者や免疫抑制患者では特に注意が必要である。
Endophthalmitis Vitrectomy Study(EVS)における術後眼内炎の症状頻度を以下に示す。
| 症状 | 頻度(EVS) |
|---|---|
| 霧視 | 94.3% |
| 充血 | 82.1% |
| 眼痛 | 74% |
| 眼瞼腫脹 | 34.5% |
EVSのデータでは眼痛は74%に認められるが、25%以上の症例では疼痛がない。術後や注射後に急激な視力低下・充血が生じた場合は、疼痛がなくても眼内炎を積極的に疑って受診する必要がある。
主要な臨床所見の頻度(EVS)を以下に示す。
| 所見 | 頻度(EVS) |
|---|---|
| 前房蓄膿 | 85% |
| 透光体混濁(硝子体炎) | 79% |
| 光覚弁以下の視力 | 26% |
EVS(白内障術後眼内炎)での培養陽性例の菌種分布:
610眼を対象とした多施設研究では、高毒性菌による感染で重度視力低下(LP以下)のオッズ比が4.48、網膜剥離または眼球摘出のオッズ比が1.90であった。4)
予後不良因子:
ESCRSのデータでは、白内障術後眼内炎の発生率は経時的に減少しており、0.097%から0.063%まで低下している。8) セフロキシム前房内投与などの感染予防策の普及がこの低下に寄与していると考えられる。
受診時視力の評価が治療方針決定で最重要である。EVSの知見から、光覚弁(LP)以下か手動弁(HM)以上かの区別が治療選択の分岐点となる(「標準的な治療法」の項参照)。
前房蓄膿の程度・角膜浮腫・フィブリン析出などを評価する。隅角鏡を用いると隅角内の蓄膿(angle hypopyon)を検出できる。
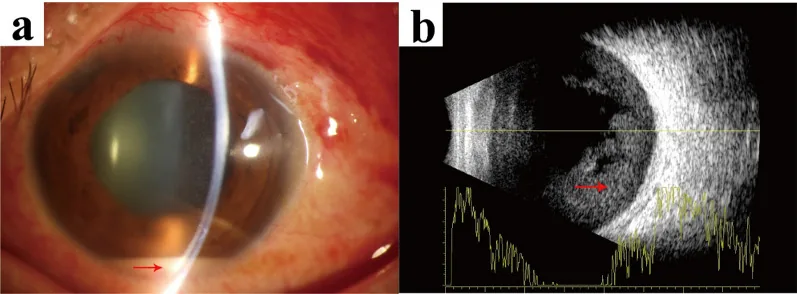
硝子体炎や角膜浮腫で眼底が透見困難な場合に、硝子体内エコーの評価・網膜剥離の有無の確認に必須の検査となる。
術後早期の前房炎症においてTASSとの鑑別が重要である。5)
TASSは手術翌日(12〜24時間以内)に発症し、硝子体炎を伴わない点が眼内炎との主要な鑑別点である。5) TASSはステロイド点眼に反応するが、眼内炎では抗菌薬の早期投与が不可欠であり、両者の見分けは治療方針に直結する。疑わしい場合は硝子体穿刺による検体採取を行う。
EVSの推奨に基づく治療選択(白内障術後・二次眼内レンズ挿入後眼内炎):5)
Tap & Inject
適応:受診時視力が手動弁(HM)以上の症例。
処置:硝子体穿刺(tap)+硝子体内抗菌薬注入(inject)を行う。
EVSでは視力HM以上の群で、即時硝子体切除術とTap&Injectの最終視力に有意差なし。侵襲の少ない治療として第一選択となる。
即時硝子体切除術
適応:受診時視力が光覚弁(LP)以下の症例。
効果:硝子体切除術群で20/40以上の視力を達成した割合が33%、Tap群では11%。5)
即時の硝子体手術により硝子体内の起炎菌・炎症物質を除去する。日本では視力予後の改善を期待して早期硝子体手術を行う施設も多い。
投与量の標準的なプロトコールを以下に示す。
| 薬剤 | 硝子体内投与量 |
|---|---|
| バンコマイシン | 1.0 mg/0.1 mL |
| セフタジジム | 2.25 mg/0.1 mL |
| アムホテリシンB | 5〜10 μg/0.1 mL |
| ボリコナゾール | 50〜100 μg/0.1 mL |
ESCRSガイドライン(2024)では以下を推奨している:8)
全身感染症の管理が最優先となる。IDSA推奨では K. pneumoniae 肝膿瘍(PLA)合併EEに対し、抗菌薬を4〜6週間投与する。1) 眼局所治療(硝子体内抗菌薬注入・硝子体手術)と全身治療を並行して行う。
硝子体手術と硝子体内抗菌薬注入による眼局所治療に加え、原疾患(肝膿瘍・菌血症など)の全身抗菌薬治療を4〜6週間継続するのが標準的である。1) 糖尿病や免疫抑制状態など基礎疾患の管理も並行して行い、感染内科との連携が不可欠となる。
手術中または外傷時に眼周囲の常在菌が眼内に侵入し、免疫学的に隔絶された硝子体腔・前房内で急速に増殖する。眼内はブドウ球菌などの防御機構が乏しいため、少量の菌でも感染が成立する。
高毒性菌は緑内障手術後・硝子体手術後に相対的に多く見られるが、これはこれらの手術による結膜バリアの破綻が口腔内常在菌や環境菌の侵入を促進するためと考えられる。4)
他臓器の感染巣(肝膿瘍・肺炎・心内膜炎など)から血行性に眼内へ病原体が播種される。通常、網膜血管を通じて後眼部から感染が始まり、ブドウ膜・硝子体へと波及する。
hvKP(高病毒性 K. pneumoniae)の毒性因子:
糖尿病では高血糖による血管透過性の亢進がhvKPの網膜血管への侵入を促進し3)、かつ好中球の機能低下が感染防御を弱める。これが糖尿病患者においてPLA合併EEの頻度が高い理由の一つと考えられる。
Grillitschら(2024)は610眼を対象とした多施設研究で、高毒性菌(口腔内細菌・Streptococcus等)による眼内炎は低毒性菌と比較して、重度視力低下(LP以下)のOR 4.48、網膜剥離または眼球摘出のOR 1.90であることを報告した。4) 培養陽性率は48.5%(296/610眼)であった。この知見は、受診時の起炎菌推定(術式・受傷機転・臨床経過)が予後予測に寄与することを示している。
IRIS Registryを用いた研究(2025)では、抗VEGF薬硝子体内注射後眼内炎1044例において、早期硝子体切除術と硝子体内抗菌薬注入のみを比較した場合、最終視力に有意差がないことが報告された。6) 受診時視力が良好な症例ではTap&Injectが過剰な侵襲を避けうる可能性を示唆している。
Blanchら(Ophthalmology)は8497眼を含む系統的レビューで、開放性眼球損傷における一次縫合の早期実施と遅延実施を比較し、眼内炎発生率への影響を検討した。7) 早期縫合による眼内への病原体侵入防止が感染リスク低減の観点から推奨される。
Luら(2025)は Paenibacillus 属による全身感染と眼内炎の症例を報告し、培養では同定困難であったこの稀な菌種をmNGS(メタゲノム次世代シークエンス)により同定した。2) mNGSは培養陰性眼内炎の原因究明において有望な技術として注目されている。