早期〜中期所見
後極部・乳頭周囲のドルーゼン:血管弓に沿った早期発症のドルーゼン。放射状配列が特徴的。1)
2種類のドルーゼン形態:大きな円形ドルーゼンと小さな放射状ドルーゼンの2種類が認められる。2)
OCT所見:RPE/ブルッフ膜複合体のびまん性変化を示す。神経感覚層は比較的保たれる。ドルーゼン様PED・ダブルレイヤーサインが確認される。1)2)

ドイン蜂巣状網膜ジストロフィ(Doyne Honeycomb Retinal Dystrophy; DHRD)は、後極部・乳頭周囲に白色のドルーゼン様沈着物が放射状に配列する常染色体優性遺伝の網膜ジストロフィである。別名「マラッティア・レベンティネーゼ(Malattia Leventinese; MLVT)」「家族性優性ドルーゼン」とも呼ばれる。OMIM番号は#126600である。1)
1899年、英国の眼科医Robert Doyneが4姉妹にこの所見を認め、「蜂巣状パターン」として初めて記載した。1925年にはスイスのVogtがLeventine渓谷で同一表現型を報告し、「マラッティア・レベンティネーゼ」と命名した。1999年、StoneらはDHRDとMLVTの両家系においてEFEMP1遺伝子の同一変異(R345W)を同定し、両者が同一疾患であることを証明した。
原因遺伝子は染色体2p16.1に位置するEFEMP1(EGF-containing fibulin-like extracellular matrix protein 1)で、fibulin 3タンパク質をコードする。2) このミスセンス変異Arg345Trp(R345W)がブルッフ膜と網膜色素上皮(RPE)の間に異常沈着物を引き起こし、ドルーゼン形成をもたらす。1) 加齢黄斑変性とドルーゼン・ブルッフ膜肥厚・RPE萎縮・補体活性化を共通の病態として持つ。1)
加齢黄斑変性は加齢を主因とする多因子疾患で、高齢者に発症する。一方DHRDはEFEMP1のR345W変異という単一遺伝子変異が原因で、若年から中年(40〜50代)に症状が出現し、家族歴を伴う常染色体優性遺伝をとる。ドルーゼンの分布は後極部・乳頭周囲の放射状配列が特徴的である。両者はドルーゼン形成・ブルッフ膜変化・RPE萎縮という共通の病態経路を持つため、DHRDは加齢黄斑変性の研究モデルとしても注目されている。
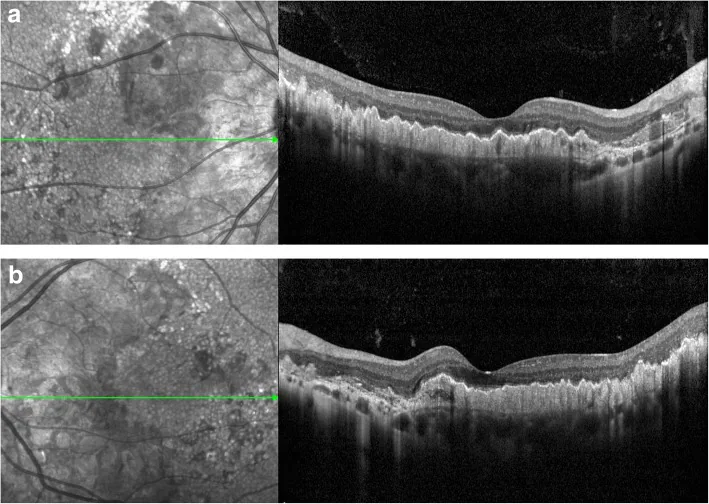
初期は無症状で経過することが多い。40〜50代になると以下の症状が出現する。
早期〜中期所見
後極部・乳頭周囲のドルーゼン:血管弓に沿った早期発症のドルーゼン。放射状配列が特徴的。1)
2種類のドルーゼン形態:大きな円形ドルーゼンと小さな放射状ドルーゼンの2種類が認められる。2)
OCT所見:RPE/ブルッフ膜複合体のびまん性変化を示す。神経感覚層は比較的保たれる。ドルーゼン様PED・ダブルレイヤーサインが確認される。1)2)
進行期所見
マルチモーダルイメージングによる評価が診断と経過観察に有用である。2) 眼底自発蛍光(FAF)では、ドルーゼン部に高自発蛍光、RPE萎縮部に低自発蛍光を認める。2) フリッカー閾値検査(FDT)では視野感度の低下が検出される。1)
同一家系内でも重症度には差がある。一部の症例では進行期まで良好な視力が維持される一方、CNVMを合併した症例では急激な視力低下をきたすことがある。定期的な眼底検査によるCNVMの早期発見が重要である。
DHRDは単一遺伝子変異による常染色体優性遺伝疾患である。以下に遺伝子情報を示す。
遺伝子情報の概要を以下に示す。
| 項目 | 内容 |
|---|---|
| 原因遺伝子 | EFEMP1(2p16.1) |
| 変異 | エクソン10・R345W |
| 遺伝形式 | 常染色体優性 |
| コードタンパク | fibulin 3 |
EFEMP1はEGF含有フィブリン様細胞外マトリックスプロテイン1をコードし、ブルッフ膜の細胞外マトリックス成分として機能する。R345W変異によりタンパク質の折りたたみ異常が生じ、RPEとブルッフ膜の間に基底層沈着物が蓄積する。1) また、EFEMP1変異はEGFRシグナルの抑制を通じてコレステロール排出に関わるCES1を阻害し、脂質蓄積を促進すると考えられている。加齢黄斑変性とDHRDのマウスモデルでは補体活性化の亢進も認められる。1)
DHRDの診断は若年発症・家族歴・特徴的なドルーゼン分布のパターン認識から始まる。2) マルチモーダルイメージングによる評価と遺伝子検査の組み合わせが確定診断に有用である。2)
類似した眼底所見を示す疾患との鑑別が重要である。
| 疾患 | 特徴 | 鑑別ポイント |
|---|---|---|
| 加齢黄斑変性 | 高齢発症・多因子 | 発症年齢・家族歴なし |
| Sorsby変性 | TIMP3変異 | 網状ドルーゼン |
| スターガルト病 | ABCA4変異 | 黄斑部フレック |
| II型MPGN | 全身性疾患 | 腎機能異常を伴う |
臨床所見が典型的な場合(若年発症・両眼対称性の後極部ドルーゼン・家族歴)は、遺伝子検査なしでも臨床診断は可能である。しかし確定診断・家族スクリーニング・遺伝カウンセリングを目的とする場合には、EFEMP1のR345W変異確認が推奨される。
DHRDには現時点で確立された疾患修飾療法はない。治療方針はCNVM合併の有無によって異なる。
抗VEGF硝子体内注射がCNVM合併例に対する治療選択肢となる。ラニビズマブ(0.5mg)の硝子体内注射が用いられ、注射後に視力改善と漿液性網膜剥離(SRF)の消失が報告されている。2)
Parameswarappa and Raniが報告した44歳女性(DHRD)は、1型脈絡膜新生血管膜を合併し、ラニビズマブ1回注射後にBCVAが20/40から20/30に改善し、SRFの消失を認めた。2) 光線力学療法(PDT・verteporfin)によるCNVM治療の報告もある。2)
2RT(ナノ秒パルスレーザー)はDHRDに対する新規治療として症例報告で機能改善が報告されているが、現時点では研究段階の治療であり、標準治療として確立されていない。詳細は「最新の研究と今後の展望」の項を参照されたい。
EFEMP1(EGF-containing fibulin-like extracellular matrix protein 1)はブルッフ膜の細胞外マトリックス成分として機能する。1) R345W変異によりタンパク質の異常折りたたみが生じ、RPEとブルッフ膜間に基底層沈着物が蓄積する。1) この沈着物がドルーゼン形成の基盤となる。
DHRDと加齢黄斑変性は以下の病態経路を共有する。1)
EGFRシグナルへの影響として、EFEMP1 R345W変異はEGFR経路を過剰抑制し、コレステロール排出に関わるCES1の発現を低下させる。これにより脂質蓄積が促進され、ドルーゼン形成につながると考えられている。
電気生理学的検討では、全視野網膜電図で振幅低下が認められ、桿体・錐体双方の機能障害が示唆される。1) FDT視野検査では視野感度の有意な低下が確認される。1)
DHRDは加齢黄斑変性と同一の分子・病態経路(ブルッフ膜変化・RPE萎縮・補体活性化)を持ちながら、単一遺伝子変異(R345W)によって発症するため、病態の因果関係を明確に解析できる。加齢黄斑変性はゲノム・環境の多因子疾患であり機序解析が困難だが、DHRDモデルはその共通機序を研究するのに適したシステムとなる。
2RT(2-minute Retina Treatment)は超低エネルギーのナノ秒パルスレーザー(400μm径・3ナノ秒・532nm・0.15〜0.45mJ)を用いる非侵襲的治療法である。RPEのデブリドマンと創傷治癒反応を介した層再形成を促進する機序が想定されている。1)
Cusumanoら(2023)は、DHRD患者3例(41〜46歳)を対象に2RT治療を施行し、最長30ヶ月のフォローアップを報告した。1) 主な結果は以下の通りであった。
- 視力:Case 1で2〜10文字の改善を認めた
- FDT視野感度:Case 2でOD MD −12dBからの改善、Case 3でOS MD −9dBからの改善を認めた
- 全視野網膜電図振幅:Case 1・2で有意な増加が確認された
- 安全性:治療関連有害事象は認められなかった(ただしCase 1の24ヶ月時に嚢胞様黄斑浮腫が出現)
また、桿体特異的な網膜電図改善(全視野ERG改善あり・多焦点網膜電図変化なし)が認められ、桿体系を主標的とした作用機序が示唆される。1) さらに未治療の僚眼にも機能改善が見られた症例があり、全身的な間接誘導効果の可能性が考察されている。1)
本報告はケースシリーズ(3症例)のエビデンスレベルにとどまり、大規模RCTは未実施である。繰り返しレーザーセッションの有効性・最適プロトコールの確立が今後の課題とされている。1)