眼局所因子
重症の増殖糖尿病網膜症:糖尿病網膜症の重症度が高いほどリスク上昇1)
広範な線維血管増殖:活動性新生血管と広範な硝子体網膜癒着2)
既存のTRD:発症前からTRDが存在する場合
輪状線維血管膜:特に高リスク2)
広範な虚血領域:周辺虚血の範囲が広いほど危険

クランチ症候群(crunch syndrome)は、抗VEGF(血管内皮増殖因子)薬の硝子体内注射後に、増殖性網膜症眼で牽引性網膜剥離(TRD)が新たに発症または急速に進行する病態である。1)2)3)
「crunch(クランチ)」の名称は、顎が噛み砕くように網膜剥離が黄斑に向かって閉じ込める様子に由来する。3)
主に増殖糖尿病網膜症で報告されるが、網膜中心静脈閉塞症、未熟児網膜症(ROP)、Eales病、家族性滲出性硝子体網膜症(FEVR)、Coats病など他の増殖性網膜症でも生じうる。3)
発症率は1.5〜18.4%と報告により幅があり、最も一般的には約5%とされる。1) 発症時期は抗VEGF注射後1〜6週間で、平均13日(範囲3〜31日)である。1)2) 80%以上の症例で初回注射後5日以内に発症する。1)
重症の増殖糖尿病網膜症や既存のTRD、広範な線維化がある患者では発症率が高い。なお、牽引性+裂孔原性網膜剥離の合併は通常0.05〜0.5%に止まるが、輪状線維血管増殖膜が存在する場合は最大43%に達するとされる。
発症率は1.5〜18.4%と報告により幅があり、最も一般的には約5%とされる。1) 重症の増殖糖尿病網膜症や既存のTRD、広範な線維化がある場合にリスクが上昇する。注射後1〜6週間以内(平均13日)に発症することが多く、80%以上の症例では初回注射後5日以内に発症する。
主な画像検査所見を以下に示す。
| 検査 | 評価できる所見 |
|---|---|
| OCT | TRD範囲・黄斑浸潤・網膜浮腫 |
| OCTA | 新生血管・虚血領域 |
| 超音波 | 硝子体出血時のTRD評価 |
OCTはTRDの範囲と黄斑への浸潤・網膜浮腫の評価に有用である。1)3) OCTAは新生血管と虚血領域の定量的評価に用いられる。2) 硝子体出血により眼底が観察困難な場合は超音波検査によるTRD評価を行う。4)5)
抗VEGF薬の硝子体内注射がクランチ症候群のトリガーとなる。1)2)3) 最も多い原因薬剤はベバシズマブであり、1)2) ペガプタニブおよびラニビズマブでも報告されている。2) コンベルセプトによる発症はLi & Zhang(2025)が初報告例である。2) アフリベルセプトとの関連報告は現時点で存在しない。2)
抗VEGF薬だけでなく、汎網膜光凝固(PRP)も単独または抗VEGFとの併用でクランチを誘発しうる。炎症・熱によるコラーゲン収縮が機序として考えられており、抗VEGFと汎網膜光凝固/冷凍凝固の併用は牽引を相乗的に悪化させる可能性がある。3)
抗VEGF薬別のクランチ報告状況を以下に示す。
| 薬剤名 | クランチ報告 |
|---|---|
| ベバシズマブ | 最多報告 |
| ラニビズマブ | 報告あり |
| コンベルセプト | 初報告(2025年)2) |
| アフリベルセプト | 報告なし |
眼局所因子
重症の増殖糖尿病網膜症:糖尿病網膜症の重症度が高いほどリスク上昇1)
広範な線維血管増殖:活動性新生血管と広範な硝子体網膜癒着2)
既存のTRD:発症前からTRDが存在する場合
輪状線維血管膜:特に高リスク2)
広範な虚血領域:周辺虚血の範囲が広いほど危険
全身・治療因子
血糖コントロール不良:糖尿病罹患期間が長い場合もリスク増加2)
抗VEGF注射回数増加:繰り返し投与による線維化促進
フォロー中断・間隔延長:治療の継続性が失われた場合にリスク上昇3)
汎網膜光凝固/冷凍凝固との併用:牽引悪化の相乗効果3)
通常は注射後1〜6週間以内で、平均13日(範囲3〜31日)とされる。1)2) 80%以上の症例は初回注射後5日以内に発症し、最短で注射後3日の報告もある。発症リスクが高い患者では注射後早期からの厳重な経過観察が必要である。
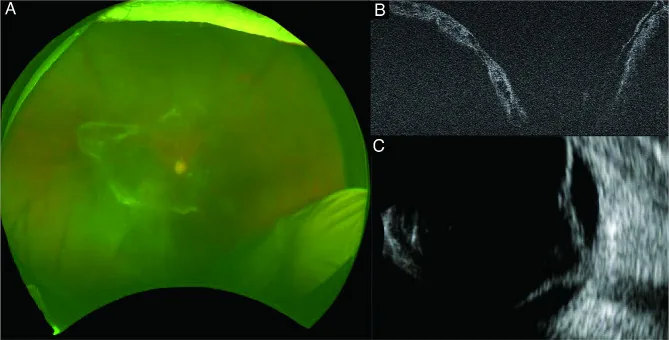
診断は主に病歴と眼底所見・画像検査によって行う。
クランチ症候群が発症した場合、緊急硝子体手術(PPV)が標準治療である。1)2)3)
Li症例ではシリコーンオイルタンポナーデが施行され、2) Bromeo症例ではシリコーンオイルタンポナーデ後6か月で除去と白内障手術が同時施行された。3)
緊急手術(標準治療)
硝子体手術+増殖膜除去:線維血管膜の慎重な剥離による牽引解除
エンドレーザー汎網膜光凝固:術後の新生血管活動性を抑制
シリコーンオイル/ガスタンポナーデ:網膜復位の維持
手術不能例の代替
抗VEGF定期注射:8〜12週間隔での定期投与による安定化
適応の限定:心疾患など手術リスクが高い症例に限る例外的選択肢1)
注意点:注射間隔の延長は硝子体出血再発のリスクとなる
術前の抗VEGF投与は手術時間の短縮、網膜裂孔数の減少、術中出血量の減少に寄与するというエビデンスがある。4)5) Cochrane系統的レビューでは、術前・術中ベバシズマブ投与が術後硝子体出血を減少させることが示されている。4)5)
心疾患などで手術リスクが極めて高い症例では、抗VEGF単独療法による管理が例外的に選択される。Yuan症例では心疾患により手術不可の患者に対し、ベバシズマブ8〜12週間隔の定期注射を1.5年以上継続し、TRD安定・中心窩付着維持が報告されている。1)
早期発見・早期手術介入が重要だが、視力予後は必ずしも良好でない。Li症例では硝子体手術後の視力は指数弁にとどまり、2) Bromeo症例では6か月後に20/400と報告されている。3) 手術不能例でも抗VEGF単独療法でTRD安定・中心窩付着維持の報告はあるが、1) 予後の改善には早期介入が鍵となる。
増殖糖尿病網膜症では、VEGFのアップレギュレーションが血管新生を引き起こし、後部硝子体皮質への血管増殖が生じる。その後、線維組織が形成・収縮し、TRDへと進行する。1) 増殖糖尿病網膜症は時間経過とともに血管新生優位の段階から線維化優位の段階へ移行するが、抗VEGF投与はこの進行を加速させる可能性がある。2)
Li & Zhang(2025)は、抗VEGF投与後のクランチ誘発機序として、新生血管の急速な退縮による牽引力の急激な変化に加え、VEGF減少とTGF-β(トランスフォーミング増殖因子-β)増加の連動による線維化促進・網膜硬化を挙げている。強力なVEGF阻害薬はより顕著な線維化反応を誘発する可能性がある。2)
Bromeoら(2021)はin vitro実験として、ベバシズマブがRPE細胞・グリア細胞でTGF-β2、CTGF(結合組織増殖因子)、CNTF(毛様体神経栄養因子)を上方制御し、線維化を加速させることを報告した。3)
既存の硝子体網膜癒着パターンと長期の線維血管増殖による生体力学的ストレスが、抗VEGF投与後の急激な代償不全に寄与すると考えられている。2)
汎網膜光凝固は周辺RPE細胞と視細胞を破壊し、外層の酸素消費量を低減させる。これにより内層への酸素拡散が増加し、VEGF産生刺激が減少してさらなる血管新生が抑制される。6) 一方、汎網膜光凝固による炎症・熱はコラーゲン収縮を誘発し、牽引を悪化させる可能性もある。3)
増殖糖尿病網膜症では脆弱な新生血管が液体・蛋白漏出を引き起こし、黄斑浮腫・出血をきたす。異常血管が線維化して網膜を牽引するとTRDが生じる。6)
一部の症例では、抗VEGF注射後に新生血管が退縮し、硝子体網膜牽引が解除されてTRDが改善する現象が知られ、「favorable crunch(好ましいクランチ)」と呼ばれる。
Leeらの報告では、4眼中3眼でTRDが平坦化・解消したとされている。1)
抗VEGF注射後に新生血管が退縮し、硝子体網膜牽引が解除されてTRDが改善する現象を指す。通常のクランチ(牽引悪化型)とは逆の転帰をたどる。Leeらの報告では4眼中3眼でTRDが平坦化・解消したとされており、1) 全症例がクランチにより悪化するわけではないことを示している。
DRCR.net Protocol Sではラニビズマブと汎網膜光凝固を比較し、増殖糖尿病網膜症におけるTRD発症率に統計学的有意差は認められなかった。しかし、増殖糖尿病網膜症患者が抗VEGF注射中にフォローアップから脱落した場合、汎網膜光凝固を受けた患者と比較して視力・解剖学的転帰が不良であった。4)5)
この結果は、抗VEGF単独療法がフォローアップを確実に継続できる患者に限り考慮可能であることを示唆している。4)5)
コンベルセプトによるクランチ症候群の初報告が2025年に公表された。2) アフリベルセプトやコンベルセプトなど強力なVEGF阻害薬がより顕著な線維化反応を誘発するかどうかは今後の研究課題として残されている。2)
TGF-βを含むサイトカインプロファイルの変化がクランチ症候群の発症に関与する可能性が示唆されており、2) 分子レベルでの機序解明が今後の治療戦略につながると期待される。
抗VEGF薬の硝子体内注射に伴う全身動脈血栓塞栓イベントリスクについては、現時点の臨床試験では確定的な結論が得られていない。7)
Yuan M, Hoyek S, Kim LA, Chaaya C, Patel N. Antivascular endothelial growth factor injections for the chronic treatment of macula-off, fovea-on diabetic tractional retinal detachment with vitreous hemorrhage. J VitreoRetin Dis. 2025;9(2):236-240.
Li Z, Zhang Y. Anti-vascular endothelial growth factor crunch syndrome in proliferative diabetic retinopathy. JCEM Case Rep. 2025;3:luaf083.
Bromeo AJ, Veloso A, Lerit SJ, Gomez MC. Tractional retinal detachment (‘crunch’ phenomenon) from intravitreal anti-vascular endothelial growth factor injection in central retinal vein occlusion. BMJ Case Rep. 2021;14:e240506.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. 2nd ed. AAO; 2019.
American Academy of Ophthalmology. Diabetic Retinopathy Preferred Practice Pattern. AAO; 2024.
O’Leary F, Campbell M. The blood-retina barrier in health and disease. FEBS J. 2023;290(4):878-891.
American Academy of Ophthalmology. Retinal Vein Occlusions Preferred Practice Pattern. AAO; 2024.