血管性(CRAO)
非動脈炎性CRAO:全CRAOの約95%を占める。塞栓の種類はコレステロール塞栓74%、血小板フィブリン塞栓15.5%、カルシウム塞栓10.5%である2)。頸動脈疾患が70%以上に合併する(EAGLE study)1)。
動脈炎性CRAO:巨細胞動脈炎(GCA)が主原因。両側性CRAOの場合は必ず除外する10)。
感染性心内膜炎由来CRAO:敗血性塞栓による。塞栓性合併症はIE患者の22〜50%に生じる9)。

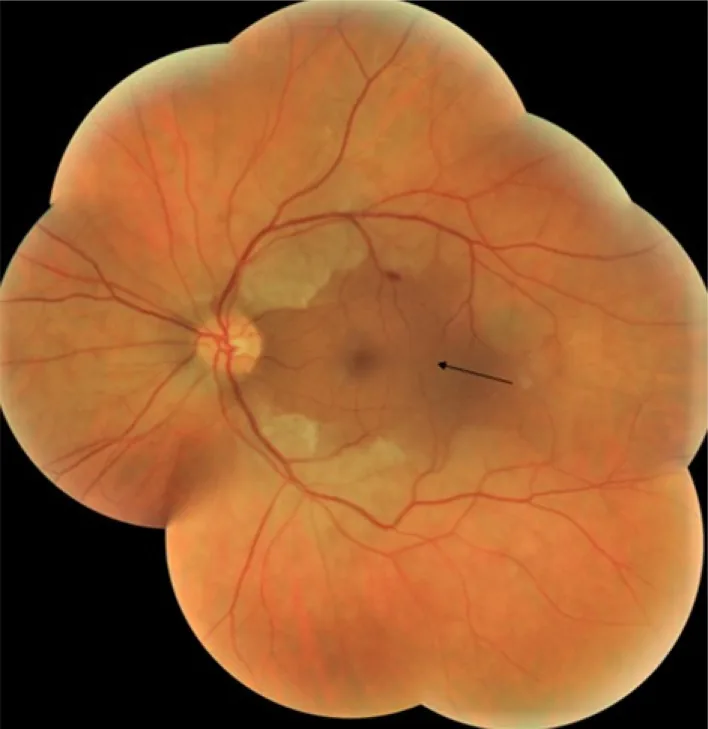
チェリーレッドスポット(cherry-red spot; CRS)は、後極部の眼底所見の一つである。網膜の白濁した混濁の中で、中心窩(foveola)部分だけが赤い色調として浮かび上がる外観がサクランボの赤い実に似ることから命名された。日本語では「桜実紅斑」とも呼ばれる。
この所見は1887年にBernard Sachsが「家族性黒蒙性白痴」(現在のテイ・ザックス病)の眼底所見として初めて記載した。現在ではCRAOや各種リソソーム蓄積症など多彩な疾患で出現する、臨床的に重要な徴候として広く認知されている。
CRAOの発生率は10万人に約1人とされる1)。CRAOの1〜2%は両側性であり、その場合は巨細胞動脈炎(GCA)などの血管炎を示唆する10)。また、眼動脈閉塞(OAO)の約60%にもCRSが出現する9)。
人種によって見え方が異なり、白人では鮮やかな赤色を呈するが、非白人では茶色や黒色調になることがある。これは脈絡膜の色素量の違いによる。代替用語として「perifoveal white patch(傍中心窩白色斑)」も提案されている。
CRSは単一の疾患ではなく、複数の異なる病態から生じる臨床徴候である。原因は大きく「血管性」「代謝性蓄積症」「薬物・毒性」「外傷・その他」の4群に分類される。
血管性(CRAO)
非動脈炎性CRAO:全CRAOの約95%を占める。塞栓の種類はコレステロール塞栓74%、血小板フィブリン塞栓15.5%、カルシウム塞栓10.5%である2)。頸動脈疾患が70%以上に合併する(EAGLE study)1)。
動脈炎性CRAO:巨細胞動脈炎(GCA)が主原因。両側性CRAOの場合は必ず除外する10)。
感染性心内膜炎由来CRAO:敗血性塞栓による。塞栓性合併症はIE患者の22〜50%に生じる9)。
代謝性蓄積症
テイ・ザックス病:ヘキソサミニダーゼA欠損。CRS出現頻度75〜90%。
GM1ガングリオシドーシス1型:β-ガラクトシダーゼ欠損。CRS出現頻度約50%。
シアリドーシス1型:ノイラミニダーゼ(NEU1)欠損。ほぼ全例にCRSが出現する3)5)。ただしNEU1の軽症変異の両アレルではCRS欠如も報告されている5)。
薬物・毒性
PDE5阻害薬(シルデナフィル等):シルデナフィル100mg×2錠の過量服用後にCRAOが発症した症例報告がある6)。FDAにもPDE5阻害薬関連の眼血管閉塞報告が多数蓄積されている。
その他:キニーネ中毒、一酸化炭素(CO)中毒など。
外傷・その他
網膜震盪症(commotio retinae):眼球打撲後に後極部の網膜白濁が生じ、擬似的なCRSを呈する。
COVID-19ワクチン後CRAO:Covaxin(インド産不活化ワクチン)接種後のCRAO報告が世界で初めて記載された8)。
鎌状赤血球形質+糖尿病:酸化ストレスによる鎌状赤血球化がCRAOの原因となりうる1)。
代謝性蓄積症別のCRS出現頻度をまとめる。
| 疾患名 | 欠損酵素 | CRS頻度 |
|---|---|---|
| テイ・ザックス病 | ヘキソサミニダーゼA | 75〜90% |
| GM1ガングリオシドーシス1型 | β-ガラクトシダーゼ | 約50% |
| シアリドーシス1型 | ノイラミニダーゼ(NEU1) | ほぼ全例 |
小児ではリソソーム蓄積症が主原因となる。テイ・ザックス病では75〜90%の症例でCRSが出現する5)。ミオクローヌス・運動失調・痙攣などの神経症状と組み合わせて小児のCRSを診た場合は、代謝性蓄積症の精査が必要である。
CRAO(血管性)の場合:
リソソーム蓄積症の場合:
眼底所見:
その他の眼科的所見:
画像検査所見:
眼科的検査
眼底検査:散瞳下でのCRS確認と網膜動脈の評価。塞栓子の有無を確認する。
RAPD評価:スウィングライトテストによる求心性瞳孔障害の確認。
視力・視野測定:閉塞の範囲と重症度の把握。
画像検査
OCT:内層網膜の急性期高反射と慢性期菲薄化を評価。リソソーム蓄積症では通常の眼底検査より早期変化を捉えられる場合がある5)。
OCTA:血流消失領域を非侵襲的に把握6)。
FA:動脈充盈遅延パターンの確認1)。自家蛍光(FAF)はリソソーム蓄積症の評価に有用5)。
全身検査
心臓超音波(TEE):経食道心エコーは感度91〜100%。経胸壁心エコー(TTE)の感度44〜63%と比較して優れる2)。
頸動脈エコー:頸動脈狭窄・プラークの評価4)。
CTA/MRI(脳):同時脳梗塞の確認4)。
凝固系検査・Hb電気泳動:血栓素因・鎌状赤血球形質の評価1)。
代謝性蓄積症が疑われる場合:
CRAOの場合は脳卒中と同等の緊急事態である。不可逆的な網膜障害は発症後約4時間で生じ7)、入院患者の12.9%が脳卒中、3.7%が心筋梗塞を合併する4)。発症に気づいた時点で即座に眼科・神経内科の救急受診が必要である。
CRAOに対して有効性が確立された標準治療は現時点では存在しない9)。以下の治療が試みられるが、いずれもエビデンスは限定的である。
CRAO発症後に自然改善するのは無治療例の約22%のみである7)。不可逆的な網膜障害が生じるまでの時間は約4時間とされる7)。
急性期に試みられる治療法をまとめる。
| 治療法 | 具体的な方法 | エビデンス |
|---|---|---|
| 眼球マッサージ | 指圧による断続的加圧 | 確立されていない9) |
| 前房穿刺 | 前房液排出による眼圧低下 | 確立されていない9) |
| 硝子体切除術 | 眼圧低下+動脈圧上昇 | 症例報告レベル7) |
硝子体切除術については、眼圧を3mmHg未満に低下させつつアドレナリン0.1mg静注による動脈圧上昇を併用する術式が報告されている。Okonkwoらは非動脈炎性CRAO2症例に本術式を施行し、それぞれ視力6/60および6/36+1への改善を報告した7)。
虚血再灌流傷害(IRI)はCRAO後約7日で発生するとされる7)。
二次予防:
確立された治療法はなく、無治療例でも約22%は自然改善する7)9)。硝子体切除術の症例報告では視力6/60や6/36+1への回復が記録されているが7)、大規模な比較試験はない。発症後の早期対応と全身合併症の管理が重要である。
黄斑部では、神経節細胞層が複数層に積み重なった厚い構造をなしている。網膜中心動脈(CRA)の閉塞により内層網膜への血流が途絶すると、神経節細胞が急速に虚血・細胞腫脹を起こし、後極部の網膜は乳白色に混濁する。
一方、中心窩(foveola)では神経節細胞層が存在しない。このため、中心窩は脈絡膜循環から直接栄養を受けて透明性を保つ。結果として、白濁した周囲の中に中心窩の赤い(脈絡膜の赤色)色調が浮かび上がる——これがCRSの成因である。
15〜25%の眼では毛様網膜動脈が存在する。この動脈はCRAとは独立した脈絡膜循環から分岐するため、CRAO時にも中心視力が温存される場合がある10)。
網膜は約97分間の虚血に耐えうるが、4時間を超えると不可逆的な障害が生じる7)。虚血再灌流傷害(IRI)はCRAO後約7日で生じるとされる7)。
リソソーム酵素欠損により、未分解の脂質(ガングリオシド、シアル化糖タンパクなど)が神経節細胞内に蓄積する。この蓄積が細胞体を膨化させ、黄斑部の神経節細胞層が白濁する。中心窩には神経節細胞がないため、CRAOと同一の機序でCRSが出現する。
シアリドーシスではNEU1遺伝子の変異によりノイラミニダーゼが欠損し、シアル化糖タンパクが蓄積する3)5)。CRSは蓄積量が増加するにつれて遅れて出現する場合があり、逆に神経節細胞死が進むとCRSが不明瞭になる5)。NEU1の軽症変異が両アレルに存在する場合はCRSを欠如することがある5)。
PDE5阻害薬はcGMPを上昇させ、全身血圧低下による脳血流(CBF)低下をきたす可能性がある6)。さらに長期的なcGMP上昇は内皮透過性を変化させ、血小板の接着・血栓形成を促進するとされる6)。
NEU1遺伝子の軽症変異が両アレルに存在する場合、CRSが欠如することが報告されている5)。CRSが不明瞭な症例でもOCTや自家蛍光(FAF)がより鋭敏に異常を検出できることがある5)。CRSの欠如だけで蓄積症を除外してはならない。
白人では鮮やかな赤色として認識されるが、非白人(アジア人・アフリカ系等)では茶色〜黒色調に見える場合がある。これは脈絡膜の色素量の差によるものであり、所見の解釈には注意が必要である。
硝子体切除と眼圧・動脈圧操作を組み合わせた外科的CRAO治療が報告されている。
Okonkwoら(2021)は非動脈炎性CRAO2症例に硝子体切除術(眼圧3mmHg未満への低下+アドレナリン0.1mg静注による動脈圧上昇)を施行し、それぞれ視力6/60、6/36+1への改善を報告した7)。発症後の時間が短いほど視機能回復の可能性が高いと考えられている。
AHA/ASAは2021年のガイドラインでCRAOを脳卒中と同等に扱い、72時間以内の神経学的精査を推奨している。
Zhong Yangら(2024)はCRAOと同時脳梗塞を合併した1例を報告し、CRAO患者の入院後脳卒中リスク12.9%・心筋梗塞リスク3.7%・合計心血管イベントリスク19%を示した4)。脳卒中専門チームと眼科の連携が求められる。
Thakarら(2022)は、Covaxin(不活化COVID-19ワクチン)接種後にCRAOを発症した世界初の症例を報告した8)。ワクチン関連の血管合併症として注目されており、因果関係の解明が今後の課題である。
Sahooら(2023)はシアリドーシスの新規NEU1変異(c.544T>A、p.Y182N)を同定し、CRSと筋クローヌスを主徴とする臨床像を報告した3)。Neerajaら(2021)はNEU1軽症変異を持つシアリドーシス1型例でCRSが欠如した症例を報告し、OCTと自家蛍光が診断に有用であることを示した5)。遺伝子型と表現型の相関解析が進んでいる。