網膜中心静脈閉塞症 は糖尿病網膜症 に次いで2番目に多い網膜 血管疾患である。篩状板 レベルで網膜中心静脈が閉塞し、4象限すべてに出血・浮腫が生じる。非虚血型(約75〜80%)と虚血型に分類され、虚血型は視力 予後が不良である。
虚血型の約50%が発症2〜4ヶ月以内に虹彩新生血管 を生じ、血管新生緑内障 (「90日緑内障」)に至るリスクがある。
黄斑浮腫 の第一選択治療は抗VEGF硝子体内注射 であり、毎月の投与から開始する。高血圧・高脂血症・糖尿病・緑内障が主要な全身リスク因子である。
50歳未満の発症では、凝固異常や全身疾患の精査が必要である。
網膜中心静脈閉塞症(Central Retinal Vein Occlusion; CRVO)は、視神経 内の篩状板レベルで網膜中心静脈が閉塞する疾患である。閉塞により静脈内圧が上昇し、4象限すべての網膜に火炎状出血・乳頭浮腫 ・黄斑浮腫が生じる。
網膜静脈閉塞症(網膜静脈閉塞症)全体は糖尿病網膜症に次ぐ2番目に多い網膜血管疾患である9)10) 。2015年時点での世界的な網膜静脈閉塞症有病率は約0.77%、推定患者数は30〜89歳で約2800万人とされる10) 。網膜中心静脈閉塞症は網膜静脈分枝閉塞症の6〜7分の1の頻度であり10) 、40歳未満では比較的まれで、60〜70歳代に多い9)10) 。
網膜中心静脈閉塞症は灌流型(非虚血型)と非灌流型(虚血型)に分類される。また、上方または下方2象限のみが障害される**半側網膜中心静脈閉塞症(hemi-CRVO)**も存在する9)10) 。
Q 網膜中心静脈閉塞症と網膜静脈分枝閉塞症はどう違いますか?
A 網膜中心静脈閉塞症は視神経内で主幹静脈が閉塞し、網膜全体(4象限)に出血が生じる。網膜静脈分枝閉塞症は網膜内の分枝静脈が閉塞し、障害は1象限〜2象限にとどまる。網膜静脈分枝閉塞症は網膜中心静脈閉塞症の6〜7倍多い10) 。
網膜中心静脈閉塞症の症状は閉塞のタイプによって異なる。
非虚血型 :軽度の霧視 ・視力低下。急性発症だが比較的軽度のことも多い。虚血型 :突然かつ重篤な視力障害。高度の視力低下(20/200未満)を呈することが多い。いずれも無痛性 である点が特徴的である。血管新生緑内障を合併すると眼痛・頭痛が出現する。
網膜中心静脈閉塞症の臨床所見は虚血の程度によって大きく異なる。下表に非虚血型と虚血型の鑑別要点を示す。
特徴 非虚血型 虚血型 視力 20/200以上 20/200未満 RAPD 軽度/消失 明瞭 予後 比較的良好 不良
非虚血型
頻度 :全網膜中心静脈閉塞症の約75〜80%を占める。
出血 :4象限の火炎状出血(比較的浅い)。
浮腫 :乳頭浮腫・黄斑浮腫を伴う。
新生血管
虚血型
出血 :4象限の広範かつ深い出血。
RAPD :求心性瞳孔 障害(RAPD)が明瞭。
新生血管 :約50%で虹彩新生血管が2〜4ヶ月以内に出現。
定義 :毛細血管無灌流域10乳頭面積以上(CVOS基準)9)10) 。
非虚血型は4ヶ月以内に約15%が、3年以内に約34%が虚血型へ移行する。虚血型では約25%の網膜中心静脈閉塞症患者が虹彩新生血管を発症し9)10) 、血管新生緑内障(「90日緑内障」)へ進行するリスクがある。
Matsuo T ら(2025)は、71歳男性の両側性網膜中心静脈閉塞症症例を報告した1) 。右眼の網膜中心静脈閉塞症は発症4ヶ月後に眼圧 35mmHgの血管新生緑内障へ進行し、最終的に光覚喪失に至った。左眼の網膜中心静脈閉塞症は抗VEGF治療と保存療法で視力を維持した。心臓手術後の右心機能不全が両側性発症の誘因と考察されている。
Q 網膜中心静脈閉塞症と診断されたら、どのくらいの頻度で通院が必要ですか?
A 非虚血型は発症4〜6週後に再評価を行う。虚血型は血管新生緑内障のリスクが高いため、6ヶ月間は月1回の受診が必要である9) 。抗VEGF治療中は黄斑浮腫の評価のためにほぼ毎月のOCT検査 が推奨される。
網膜中心静脈閉塞症の病態はウィルヒョーの3要素(血管損傷・血流停滞・凝固亢進)で説明される。篩状板後方では網膜中心動脈と静脈が共通外膜を共有しており、動脈硬化性変化により静脈が圧迫されて閉塞が生じる。
主要リスク因子を下表に示す。
リスク因子 頻度・関連 加齢 最重要:90%超が55歳以上 高血圧 50歳以上の最大73%9)10) 高脂血症 主要リスク因子7)
その他の重要なリスク因子を以下に示す。
糖尿病・緑内障・高眼圧 :いずれも独立したリスク因子である9)10) 。全身性自己免疫疾患 :SLE 患者では網膜中心静脈閉塞症発生率が対照の3.5倍とされる9)10) 。心血管リスク :網膜静脈閉塞症患者は心血管イベント・全死因死亡率が上昇する9)10) 。PDE5阻害薬(シルデナフィルなど) :FDAへの報告で網膜静脈閉塞症 82例・RAO 24例が集積されており、全身血圧低下下での網膜静脈怒張誘発が機序として推察されている2) 。COVID-19感染 :サイトカインストームによる血管内皮障害・凝固亢進が機序とされる3)4) 。COVID-19ワクチン :VITT(ワクチン誘発性血栓性血小板減少症)機序が提唱されており、ChAdOx1(AstraZeneca)接種後の血栓発症率は1.13/10万回とされる5)6) 。MTHFR遺伝子変異 :高ホモシステイン血症による凝固亢進3)4) 。右心機能不全 :静脈ドレナージ障害による静脈圧上昇1) 。
50歳未満での発症では全身精査が強く推奨される9)10) 。
高血圧・糖尿病・高脂血症の管理が最も重要な予防策です。定期的な内科受診を継続してください。
喫煙は血管疾患全般のリスクを高めます。禁煙を心がけましょう。
PDE5阻害薬(シルデナフィルなど)を使用している場合は、眼科・内科の両方に伝えてください。
突然の視力低下・霧視が起きた場合は、すぐに眼科を受診してください。
Q 若い人でも網膜中心静脈閉塞症になることはありますか?
A 40歳未満での発症はまれだが起こりうる。凝固異常・MTHFR遺伝子変異・COVID-19感染・ワクチン後VITT・PDE5阻害薬などが原因となりうる2)3)4)5)6) 。50歳未満では血液凝固検査・自己抗体検査などの全身精査が推奨される9)10) 。
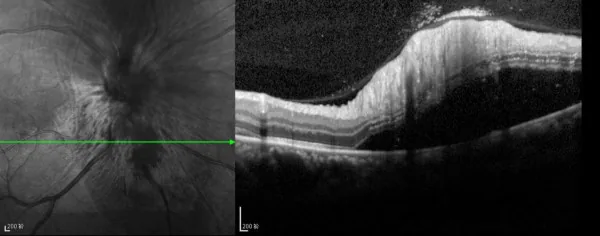
Central Retinal Vein Occlusion image Anushavan Karapetyan; Pingbo Ouyang; Luo Sheng Tang; Jiexi Zeng; Michele Dominique Li Ying. Detection of underdiagnosed concurrent branch retinal artery occlusion in a patient with central retinal vein occlusion using spectral domain optical coherence tomography. BMC Ophthalmol. 2014 Jul 12; 14:91 Figure 3. PMCID: PMC4113125. License: CC BY.
SD-OCT image taken at presentation. Detached peripappillary retina below the optic disk.
診断は病歴・視力・眼底所見を組み合わせて行う。
病歴聴取 :視力低下の経過・内服薬(抗凝固薬・PDE5阻害薬)・既往歴(高血圧・糖尿病・血液疾患)9)10) 。視力・RAPD :虚血型判定の重要な指標。細隙灯・眼底検査 :4象限の出血・乳頭浮腫・黄斑浮腫の評価。眼圧・隅角 鏡 :虚血型では月1回×6ヶ月の隅角鏡検査 で虹彩新生血管を確認9) 。
以下に各検査の役割を示す。
検査 目的 OCT 黄斑浮腫の評価9)10) FA (蛍光眼底造影)虚血範囲の評価9)10) OCTA 非侵襲的な毛細血管無灌流検出9)
OCT(光干渉断層計) :黄斑浮腫の定量評価に極めて有用であり、治療効果のモニタリングにも使用する9)10) 。FA(蛍光眼底造影) :CVOS基準(毛細血管無灌流域10乳頭面積以上)による虚血型の診断に不可欠9)10) 。OCTA(光干渉断層血管撮影) :造影剤不使用で毛細血管無灌流域を検出できる9) 。
全患者 :血圧・ESR・CBC・血糖・コレステロール・腎機能を評価する。50歳未満 :凝固異常スクリーニング(プロテインC/S・抗トロンビンIIIなど)・自己抗体(抗リン脂質抗体・抗核抗体)を追加する9)10) 。
抗VEGF療法
位置づけ :黄斑浮腫に対する第一選択治療9)10) 。
CRUISE試験 :ラニビズマブ 0.5mg群で6ヶ月後に平均14.9文字改善(sham群は0.8文字)。47.7%が15文字以上改善。
ベバシズマブ 4) 。
投与方法 :毎月投与から開始し、OCTで浮腫改善を確認しながら間隔を調整する。
ステロイド療法
DEXインプラント(Ozurdex ) :デキサメタゾン0.7mgの徐放性硝子体 内インプラント。抗VEGFが無効・不適な場合に使用9)10) 。
注意点 :ステロイド 点眼・注射は眼圧上昇・白内障 リスクに注意。眼内炎 発症率は抗VEGFの約6.92倍(0.13% vs 0.019%)との報告がある8) 。
眼内炎リスク :DEXインプラント後の遅発性眼内炎も報告されており、異物感・充血・視力低下には早急に対応が必要8) 。
汎網膜光凝固(PRP)
適応 :虚血型における虹彩新生血管・血管新生緑内障の予防9) 。
タイミング :高度虚血例には直ちにPRP を施行する。80歳以上の高齢者でも早期PRPが推奨される。
目的 :新生血管の退縮・進展抑制。視力改善効果はない。
ワクチン関連網膜中心静脈閉塞症 :ステロイドパルス療法 (メチルプレドニゾロン1g×3日間)の有効性が報告されており、中心窩 厚が823μmから166μmへ改善し、視力も2/60から6/9へ回復した症例がある6) 。硝子体手術 硝子体出血 を合併した症例では、出血除去と同時に光凝固が可能である。抗凝固療法 :視力予後を悪化させる可能性があり、推奨されない4) 。
非虚血型:4〜6週後に再評価。以後は経過に応じて間隔を調整する。
虚血型:発症後6ヶ月間は月1回の受診が必要。虹彩新生血管の監視が必須9) 。
血管新生緑内障は不可逆的な視野障害をきたすため、虚血型では6ヶ月間の月1回フォローを絶対に欠かさないこと。
DEXインプラント後は、眼圧上昇と遅発性眼内炎のリスクに注意する。異常を感じたら早急に受診が必要8) 。
抗凝固療法・血栓溶解療法は眼底出血を増悪させる可能性があり、推奨されない4) 。
PDE5阻害薬を内服中の場合は眼科・担当科に申告し、服薬継続の可否を相談すること2) 。
Q 抗VEGF注射は何回くらい必要ですか?
A CRUISE試験では毎月6回の投与が行われ、視力改善が確認された。実際には毎月投与から開始し、OCTで黄斑浮腫の改善を確認しながら間隔を延長していく。再発した場合は再投与が必要となるため、長期にわたる定期受診が不可欠である。
篩状板後方では網膜中心動脈と静脈が共通の外膜(結合組織鞘)を共有している。動脈硬化に伴う動脈壁の肥厚・硬化が静脈を圧迫し、血管内皮障害→血栓形成→閉塞へと至る9)10) 。これはウィルヒョーの3要素(血管損傷・血流停滞・凝固亢進)すべてが関与する過程である。
静脈閉塞→静脈内圧上昇→血漿成分の漏出→網膜浮腫と出血が生じる。網膜虚血→低酸素状態→VEGF(血管内皮増殖因子)の過剰産生→黄斑浮腫の悪化と新生血管形成(虹彩新生血管・網膜新生血管)が起こる9)10) 。この機序が抗VEGF療法 の理論的根拠となっている。
COVID-19関連 :サイトカインストームによる血管内皮障害・プロトロンビン状態・直接的な血管内皮細胞への感染が複合的に凝固亢進を招く3) 。VITT(ワクチン後血栓症) :血小板第4因子(PF4)に対する自己抗体が形成され、血小板が活性化して血栓が形成される5) 。PDE5阻害薬 :全身血圧低下下で網膜静脈の怒張・血流速度低下を誘発し、静脈血栓リスクを高める2) 。右心機能不全 :右心系の静脈ドレナージ障害が眼静脈圧を上昇させ、両側性網膜中心静脈閉塞症の誘因となりうる1) 。
Q なぜ「90日緑内障」と呼ばれるのですか?
A 虚血型網膜中心静脈閉塞症では、低酸素による大量のVEGF産生が虹彩新生血管を誘発する。この新生血管が隅角を閉塞して血管新生緑内障を引き起こす。発症後2〜4ヶ月(約90日)以内に約50%で虹彩新生血管が出現することから「90日緑内障」と呼ばれる9)10) 。早期発見・早期治療(PRP・抗VEGF)が視力予後を左右する。
COVID-19感染後の網膜静脈閉塞症リスクについて報告が蓄積している。
RiaziEsfahani H ら(2024)は、COVID-19罹患歴のある若年患者における半側網膜中心静脈閉塞症症例を報告した3) 。感染後数ヶ月を経ても網膜静脈閉塞症リスクが持続する可能性が示唆された。
ワクチン後網膜静脈閉塞症の20例レビューでは、7例が40歳未満の若年者であった6) 。ChAdOx1(AstraZeneca)接種後の血栓発症率は1.13/10万回とされ、VITT機序による凝固亢進が提唱されている5)6) 。
Torkashvand A ら(2023)は、シルデナフィル服用後に網膜中心静脈閉塞症と網膜中心動脈閉塞の両方を合併した症例を報告した2) 。OCTAによる血管密度の低下が記録され、PDE5阻害薬が網膜循環に与える影響が注目されている。
ファリシマブ (二重特異性抗体)広角FA・OCTA :広角撮影技術の進歩により周辺部の虚血範囲評価が精緻化されており、治療適応の判断精度向上が期待される9)10) 。両側性網膜中心静脈閉塞症と右心機能不全 :両側性網膜中心静脈閉塞症を契機に右心機能不全が発見される症例が報告されており、心臓外科・循環器内科との連携の重要性が示されている1) 。
Matsuo T, et al. Sequential bilateral central retinal vein occlusion with differential long-term outcomes following cardiac surgery. Cureus. 2025;17(12):e100045.
Torkashvand A, et al. Central retinal vein and artery occlusion associated with sildenafil. J Med Case Rep. 2023;17:399.
RiaziEsfahani H, et al. Hemicentral retinal vein occlusion in a patient with COVID-19 history. J Med Case Rep. 2024;18:50.
Staropoli PC, et al. Central retinal vein occlusion associated with COVID-19 and MTHFR mutation in a 15-year-old male. Am J Ophthalmol Case Rep. 2022;26:101522.
Sonawane NJ, et al. Central retinal vein occlusion post-COVID-19 vaccination. Indian J Ophthalmol. 2022;70:308-9.
Dutta Majumder P, et al. Retinal venous occlusion following COVID-19 vaccination: third dose and review. Indian J Ophthalmol. 2022;70:2191-4.
Zhao J, et al. Chylous aqueous humor caused by hyperlipidemia. Medicine. 2023;102:e34972.
Tripathi AN, et al. Atypical delayed-onset endophthalmitis following intravitreal dexamethasone implant. Rom J Ophthalmol. 2024;68(4):343-8.
Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2020;127:P288-P320.
Flaxel CJ, et al. Retinal Vein Occlusions Preferred Practice Pattern. Ophthalmology. 2024;131:P288-P332.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください