桿体優位型
主な症状:夜盲・視野狭窄・輪状暗点
代表的抗体:抗リカバリン抗体
進行速度:急速(数週〜数ヶ月)
特徴:急激な重度視力低下。傍中心〜赤道部の暗点が典型的。

癌関連網膜症(Cancer Associated Retinopathy; CAR)は、悪性腫瘍に伴って生じる自己免疫性の網膜変性疾患である。腫瘍随伴症候群(paraneoplastic syndrome)の眼科的表現型の一つとして位置づけられる1)。
1976年にSawyerらによって初めて報告され、1983年にKeltnerらが自己免疫機序を提唱した。腫瘍細胞が網膜タンパク質と交差反応する抗原を異所発現し、これに対する自己抗体が産生されて視細胞を障害する。
自己免疫性網膜症(Autoimmune Retinopathy; AIR)の分類では、腫瘍関連型(tumoral AIR)と非腫瘍関連型(non-tumoral AIR; npAIR)に大別される。腫瘍関連型にはCARと黒色腫関連網膜症(MAR)が含まれる1)。
最も頻度の高い原因腫瘍は小細胞肺癌(SCLC)であり、次いで消化器癌・婦人科癌・乳癌・腎癌・膵癌・リンパ腫が続く。発症年齢は40〜85歳で、性差は明確ではない。Adamusらの209例シリーズでは女性優位が報告されている。
免疫チェックポイント阻害薬(ICI)によるCAR/MARの誘発も報告されており3)、ICI使用の拡大に伴い新たな患者層が生じている。
多くの症例では眼症状が癌の診断に先行する。比較的稀な疾患ではあるが、眼科的診断が全身癌の発見につながることがある。50歳以上で網膜色素変性(RP)に類似した眼底所見があり家族歴がない場合は、CARを疑って全身検索を行うことが勧められる4)。
CARの自覚症状は亜急性・両側性(しばしば非対称)の無痛性視力低下を特徴とする。数週〜数ヶ月で進行する。
原因抗体によって症状の特徴が異なる。抗リカバリン抗体陽性例では急速かつ重篤な視力低下を呈し、傍中心〜赤道部の暗点を形成することが多い。抗エノラーゼ抗体陽性例では比較的緩徐で非対称な中心視力低下を示す傾向がある。
代表的な症例として、以下の報告がある1)。
Bordinら(2023)の症例1:58歳女性。右肺腫瘍の葉切除後に進行性の視力低下と視野狭窄、両眼の暗点を訴えた。最良矯正視力は20/40。 症例2:66歳男性。1.5年前に腎腫瘍の腎摘除術を受けた既往があり、進行性の無痛性視力低下を呈した。右眼20/200、左眼手動弁。
ICI投与によって誘発された症例では、ペンブロリズマブ開始後2週間で急速に両眼手動弁に至った70歳男性の報告がある3)。
桿体優位型
主な症状:夜盲・視野狭窄・輪状暗点
代表的抗体:抗リカバリン抗体
進行速度:急速(数週〜数ヶ月)
特徴:急激な重度視力低下。傍中心〜赤道部の暗点が典型的。
錐体優位型
主な症状:羞明・中心暗点・色覚異常
代表的抗体:抗エノラーゼ抗体
進行速度:比較的緩徐・非対称
特徴:中心視力が早期に障害される。
早期には眼底所見がほぼ正常に見えることがあり、診断を困難にする。
以下の表に自己抗体別の主な臨床的特徴を示す。
| 自己抗体 | 主な症状 | 進行速度 |
|---|---|---|
| 抗リカバリン | 急激な重度視力低下 | 急速 |
| 抗エノラーゼ | 非対称な中心視力低下 | 緩徐 |
腫瘍細胞が正常では免疫特権を持つ網膜タンパク質を異所発現し、これに対する自己抗体が産生される。分子擬態(molecular mimicry)が重要な役割を担う1)。主要な自己抗体は以下の通りである。
CTLA-4阻害薬は非特異的なT細胞増殖・制御性T細胞(Treg)抑制・B細胞活性化を引き起こす。PD-1阻害薬はオリゴクローナルなT細胞刺激とメモリーT細胞活性化を経て、持続的なB細胞クローン増殖と自己抗体産生をもたらす3)。また、RPE細胞はB細胞活性化を抑制する機能を持つが、ICI誘発のT細胞障害がこれを破綻させる可能性がある3)。
小細胞肺癌が最多であり、乳癌・消化器癌・婦人科癌・腎癌・膵癌・リンパ腫が続く。MARの場合は悪性黒色腫が主な原因腫瘍となる。
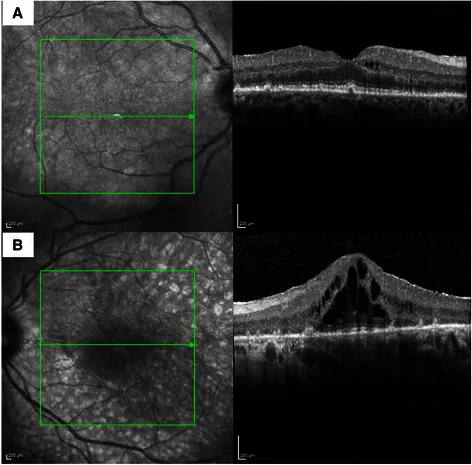
確立された診断基準はなく、臨床所見・電気生理学的検査・自己抗体検査・全身の癌スクリーニングを組み合わせて診断する。
診断上最も重要な検査である。CARとMARの鑑別にも不可欠である。
APECED(自己免疫性多内分泌腺症-カンジダ症-外胚葉形成不全症)に関連した2歳児の報告では、網膜電図が記録不能で、OCTにてELM・EZの消失が確認されている2)。
網膜自己抗体は健常者やnpAIRでも陽性となることがあり、単独での確定診断は不可能である。抗体価は変動するため3回以上の測定が推奨される。
全身の癌精査として胸部X線・CT・血液検査・腹部CT・PET・大腸内視鏡・乳房・泌尿生殖器の評価を行う。50歳以上でRP類似の眼底所見があり家族歴がない場合は積極的に全身検索を実施する4)。
以下の表にCAR・MARの主な鑑別点を示す。
| 特徴 | CAR | MAR |
|---|---|---|
| 障害細胞 | 視細胞 | 双極細胞 |
| 網膜電図所見 | a波・b波低下 | negative 網膜電図 |
| 原因腫瘍 | 肺癌など多様 | 悪性黒色腫 |
抗網膜自己抗体陽性のみではCARの確定診断とならない。健常者やnpAIRでも陽性となることがあり、抗体価も変動する。網膜電図・OCT・FAFなどの電気生理学的・形態学的所見、および全身の悪性腫瘍の有無を総合して判断する必要がある。
網膜電図所見が最大の鑑別点である。CARでは桿体・錐体系ともにa波・b波が低下するのに対し、MARではnegative 網膜電図(a波正常・b波著減)を呈する。また、MARでは悪性黒色腫が原因腫瘍となることが多く、CARでは小細胞肺癌などが多い。障害される細胞もCARが視細胞、MARが双極細胞と異なる。
確立された治療ガイドラインは存在しない。治療の目標は完全回復ではなく機能の安定化であり、進行を抑制することに主眼が置かれる1)。
Bordinら(2023)の報告では、経口ステロイドおよびテノン嚢下ステロイドが無効であり、全身性免疫抑制薬が忍容不能であった症例に対し、Ozurdexを6ヶ月ごとに投与した結果、機能的な安定化が得られた1)。
Ozurdexは3〜4ヶ月にわたる持続的な薬剤放送により局所炎症を制御し、血液網膜関門(BRB)の再構築に寄与すると考えられる。抗リカバリン抗体価のモニタリングでも、Ozurdex投与後に抗体価の低下が確認された1)。
抗IL-6受容体抗体(トシリズマブ・サリルマブ)は、難治性の嚢胞様黄斑浮腫を伴うnpAIRへの応用が報告されている1)。
原発腫瘍の切除・化学療法・放射線治療を行っても、すでに体内に循環している自己抗体のため視力の改善は得られないことが多い1)。腫瘍治療は全身管理として実施するが、それのみで眼病変の改善を期待するのは困難である。
APECED関連の網膜症例では、免疫抑制療法を行っても網膜変性の進行が止まらなかったことが報告されている2)。
原発腫瘍を治療しても、すでに体内で産生・循環している自己抗体は消失しにくいため、視力の回復は得られないことが多い1)。腫瘍治療は全身管理として不可欠だが、眼病変への改善効果は限定的である。治療の目標は視機能の安定化に置くべきとされている。
腫瘍細胞が正常では免疫特権部位(網膜)にのみ発現するタンパク質を異所発現すると、免疫系がこれを認識して自己抗体を産生する。この分子擬態が網膜障害の起点となる1)。
抗リカバリン抗体は細胞内に侵入し、カルシウムホメオスタシスを障害してカスパーゼ依存性のアポトーシスを誘導する。CARでは桿体・錐体の両視細胞が同時に障害される4)。
MARは異なる機序を持ち、双極細胞の膜タンパク(TRPM1)に対する自己抗体が関与する。障害細胞の違いが前述の網膜電図所見の差異(CARはa+b波低下、MARはnegative ERG)として現れる。
CTLA-4阻害薬は非特異的なT細胞増殖とTreg抑制を引き起こし、B細胞を活性化して自己抗体産生をもたらす。PD-1阻害薬はオリゴクローナルなT細胞刺激とメモリーT細胞活性化を経て、持続的なB細胞クローン増殖と自己抗体産生を誘導する3)。
RPE細胞はB細胞活性化を通常は抑制しているが、ICI誘発のT細胞障害がこの制御機構を破綻させ、眼内での自己免疫応答が増幅される可能性がある3)。
全身性免疫抑制療法が困難な症例に対する局所治療の選択肢として、Ozurdexが注目されている。Bordinら(2023)の症例報告では、6ヶ月ごとの反復投与で機能の安定化が得られ、抗リカバリン抗体価の低下も確認された1)。投与後の自己抗体モニタリングを組み合わせることで、治療反応の評価が可能となる可能性がある。
ICIの普及に伴い、薬剤誘発性のCAR/MAR症例が増加している3)。Lainsら(2025)はICIによる網膜障害の分類・診断・管理フレームワークの確立を提唱しており、早期診断と適切な介入プロトコールの整備が急務とされている3)。
トシリズマブ・サリルマブなどの抗IL-6受容体抗体が、難治性嚢胞様黄斑浮腫を伴うAIRに対して使用されており、CARへの応用も検討されている1)。
CARラットモデルにおいてカルシウムチャネル遮断薬が有効であることが示されており、抗リカバリン抗体によるカルシウムホメオスタシス障害への介入として今後の研究が期待される。
AIRE遺伝子変異に起因するAPECEDでは、幼少期から自己免疫性網膜症を発症する症例が報告されている2)。Sakaguchiら(2021)の報告では2歳時に網膜電図が記録不能となっており、早期介入の重要性が示唆されるが、有効な治療法は未確立である2)。