基底層ドルーゼン(キューティキュラードルーゼン)は加齢黄斑変性 スペクトラムの一型であり、網膜色素上皮 (RPE)基底膜とブルッフ膜 の間に多数の小型黄色ドルーゼン が蓄積する。
典型的AMDより若年(平均57.9歳)に発症し、患者の60〜92.1%が女性である。1)
蛍光眼底造影 (FA)での”stars-in-the-sky”パターン、OCT での”saw-tooth”(鋸歯状)パターンが特徴的な所見である。1) CF H遺伝子変異(p.Tyr402His)との強い関連があり、補体 代替経路の異常が病態の基盤となる。1) ドルーゼンそのものの治療法はなく、合併症(脈絡膜新生血管 ・地図状萎縮 )の早期発見と適切な治療が鍵となる。
若年患者では膜性増殖性糸球体腎炎(MPGN)などの腎疾患を合併することがあり、全身的評価が必要な場合がある。1)
基底層ドルーゼン(basal laminar drusen; BLD)は、1977年にGassが眼底に多数の小型黄色ドルーゼンが散在するとして初めて記述した疾患概念である。蛍光眼底造影(FA)上の”stars-in-the-sky”パターンが特徴とされる。1)
当初はRPE基底膜の結節状肥厚として”basal laminar drusen”と命名されたが、その後の研究によりRPEの基底膜とブルッフ膜内膠原層の間に沈着すること、すなわち通常の軟性ドルーゼンと同じ局在にあることが明らかとなった。これにより”cuticular drusen”(キューティキュラードルーゼン)という名称が現在は推奨されている。1)
加齢黄斑変性(AMD)スペクトラムに属するが、典型的加齢黄斑変性と異なる以下の特徴を持つ。
発症年齢 :平均57.9 ± 13.4歳と比較的若年性差 :患者の60〜92.1%が女性。女性である確率は通常加齢黄斑変性比で約5倍1) ドルーゼンの大きさ :50〜75μm径の小型で均一なドルーゼン1) 分布 :後極部から周辺部、乳頭周囲に及ぶことがある
Q 基底層ドルーゼンと加齢黄斑変性は同じ病気か?
A 加齢黄斑変性スペクトラムの一部ではあるが、比較的若年・女性優位の発症、特徴的な”stars-in-the-sky”や”saw-tooth”のイメージング所見、CFH遺伝子変異との強い関連など、独自の特徴を持つ。加齢黄斑変性の前駆病変としても位置づけられており、長期観察で黄斑 合併症に進行することがある。1)
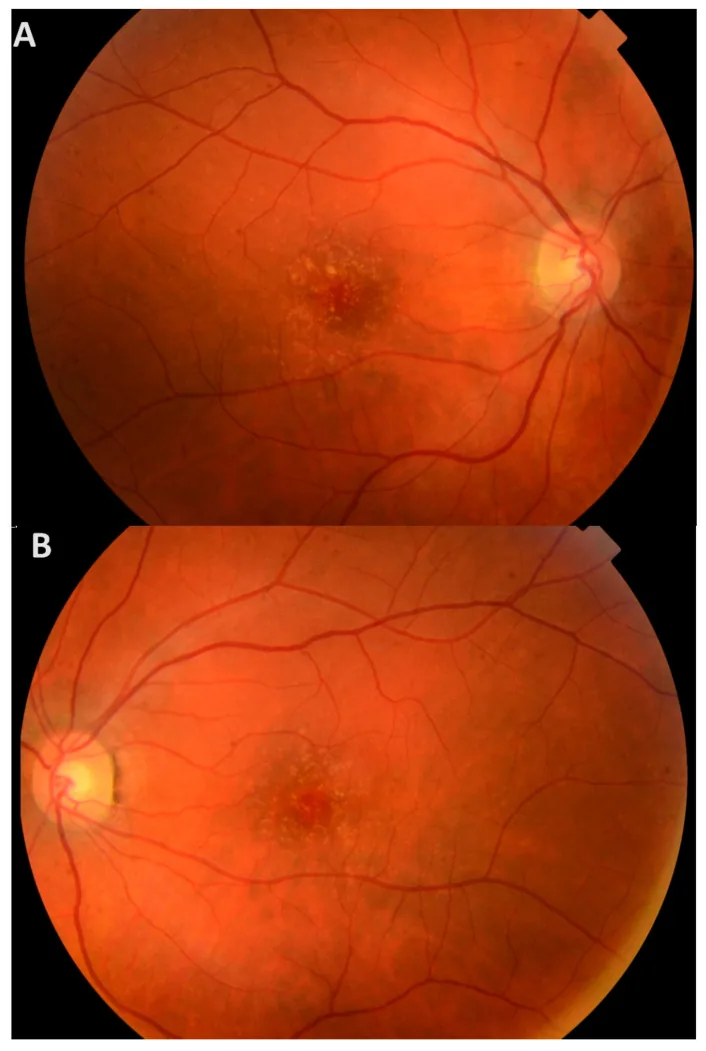
Basal Laminar Drusen image Egle Preiksaitiene; Viktorija Gurskytė; Violeta Mikštienė; Rasa Strupaitė-Šileikienė; Ramūnas Dzindzalieta; Gunda Petraitytė. Evidence for the Pathogenicity of a CFH Variant in a Multigenerational Family with Cuticular Drusen. Medicina (Kaunas). 2025 Sep 11; 61(9):1649 Figure 2. PMCID: PMC12472062. License: CC BY.
Fundus photographs of the proband’s right eye (A) and left eye (B) show numerous small, hard, yellow drusen in the posterior poles.
初期には自覚症状に乏しく、ほとんどの患者は晩年まで無症状のまま経過する。黄斑部にドルーゼンが存在しても、網膜 外層の障害が生じなければ無症状である。
長期にわたりドルーゼンが存在すると、RPE機能障害から網膜外層障害へと進行する。中心窩 に及ぶと以下の症状が出現する。
視力 低下変視症 (ゆがみ)中心暗点
散瞳 下眼底検査 では、網膜全体に多数の小さな黄色いドルーゼンが観察される。RPEの下に複数の硬性の隆起した黄白色ドルーゼンとして認識される。
臨床表現型は3つに分類される。1)
Phenotype 1
分布 :黄斑部に集中する型。
合併症リスク :GAの5年推定発生率12.9%と3型中最も低い。
Phenotype 2
分布 :後極部に散在し、末梢・鼻側へ拡大する型。
合併症リスク :GAの5年推定発生率38.7%。MNVリスクも高い。
Phenotype 3
分布 :大型ドルーゼン(>200μm)が混在する型。
合併症リスク :GAの5年推定発生率43.6%と最も高い。
主な臨床所見を以下に示す。
大型ドルーゼン(>200μm)の合併 :25〜59.3%に認め、60歳以上では色素異常を伴う1) 乳頭周囲への進展 :63.3〜75.3%に認められる1) 色素性RPE変化 :最も一般的な合併所見(47.5%)OCT所見 :RPE-BLの三角形の隆起、“saw-tooth”(鋸歯状)パターンが特徴的1)
OCTでは3つのタイプに分類される。1)
Type 1(33%) :浅いRPE-BL隆起Type 2(49%) :鋸歯状パターン(most typical)Type 3(18%) :mound(丘状)パターン
基底層ドルーゼンの病因は完全には解明されていない。現在明らかとなっているリスク要因を以下に示す。
遺伝的要因
CFH遺伝子 p.Tyr402His変異 :最も強い関連が確認されている。histidine allele頻度はcuticular drusen加齢黄斑変性患者で70%と、通常加齢黄斑変性(55%)より高い1) CFH遺伝子の稀なバリアント :患者の8.8%に同定される。p.Arg1210Cysはcuticular drusenに特異的と推定される1) FBLN5遺伝子変異 :関連が報告されている1) 加齢黄斑変性共通の高リスクSNPs :CFH, ARMS 2, CFB, C2, C3, APOEとの関連がある1)
性差・家族歴
患者の60〜92.1%が女性であり、女性であることが独立したリスク因子となる1)
BLD患者の44〜53%に加齢黄斑変性の家族歴がある
全身疾患との関連
MPGN(膜性増殖性糸球体腎炎)type II :補体代替経路の異常が眼と腎臓の両方で類似した沈着物を引き起こす。長期のMPGN患者(>16ヶ月)全員にdrusen様沈着が認められる1) C3糸球体腎炎 :類似の眼所見が報告されている1) 緻密沈着物病(dense deposit disease)患者の80%にcuticular drusenが認められる
視力に変化がなくても、若年(50歳代)から定期的な眼底検査を受けてください。
AMDや基底層ドルーゼンの家族歴がある場合は、特に早期からの眼科的フォローアップが重要です。
腎疾患(MPGNなど)の診断がある場合は、眼科的検査も受けることをお勧めします。
自宅でのアムスラーチャートによるセルフモニタリングが、合併症の早期発見に有用です。
Q 腎臓の病気と関連があるのはなぜか?
A CFH遺伝子変異による補体代替経路の異常が、眼(RPE-ブルッフ膜間)と腎臓(糸球体基底膜)の両方に類似の沈着物を形成するためである。特に若年患者(5〜30歳)ではMPGNや非典型溶血性尿毒症症候群(aHUS)のスクリーニングが推奨される。1)
診断には複数のイメージングモダリティを組み合わせる。眼底写真(CFP)・SD-OCT・FA・眼底自発蛍光 (FAF)のうち3つ以上での確認が推奨される。1)
各検査の典型的所見を以下に示す。
検査法 典型的所見 特記事項 眼底写真(CFP) 多数の小黄色ドルーゼン 後極〜周辺に散在 FA ”starry-sky”パターン 動静脈相に多数の過蛍光点1) FAF 中心低自発蛍光+過蛍光リム 存在例62%、非存在例100%の正確な同定率1) SD-OCT RPE-BLの三角形隆起・“saw-tooth” 3タイプに分類1)
ICG造影 (ICGA )1)
鑑別診断のポイント
硬性ドルーゼン・軟性ドルーゼン :大きさや形状、OCT所見で鑑別。硬性ドルーゼンは均一で辺縁が明瞭、軟性ドルーゼンはより大型で辺縁不明瞭1) 網状偽ドルーゼン(reticular pseudodrusen) :OCT・FAFでの分布パターンが異なる常染色体優性ドルーゼン :家族歴と遺伝子検査で鑑別パターン黄斑ジストロフィ・Best病 :電気生理検査や遺伝子検査が有用色素上皮剥離(PED )との鑑別 :OCTで隆起RPE内部が低反射→色素上皮剥離、高反射→ドルーゼン
ドルーゼンそのものを消失させる治療法は確立されていない。孤立性の基底層ドルーゼンに対しては治療適応がなく、定期的な経過観察が基本となる。
合併症の発生頻度として以下が報告されている。1)
脈絡膜新生血管(MNV/CNV) :12.5%に検出。76.7%が1型MNV。Phenotype 2, 3でリスクが高い地図状萎縮(GA) :18.5〜25%。60歳以下でも9.2%に発生卵黄状病変 :白人24.2%、アジア人1.2%。MNV合併30%
合併症別の治療方針を以下に示す。
CNV合併時
抗VEGF薬 硝子体内注射 ラニビズマブ ・アフリベルセプト ・ブロルシズマブ などを使用。
光動力学的療法(PDT ) :抗VEGF薬が無効または適応外の場合に考慮。
GA合併時
有効な治療法なし :進行を止める確立した方法はない。
継続観察 :CNV発現の早期発見を目的に定期検査を継続する。
卵黄状病変
経過観察 :自然消退することがある。
CNV合併例 :抗VEGF薬の適応を検討。
サプリメントについて
基底層ドルーゼン患者に対するAREDS(Age-Related Eye Disease Study)サプリメントの有効性は確立されていない。一般的なAREDS処方例として、オキュバイトプリザービジョン2(3錠 分3)やサンテルタックス20+ビタミン&ミネラル(3錠 分3)などがある。
自己モニタリング
アムスラーチャートを使った日常的なモニタリングにより、変視症・中心暗点の変化を早期に検出できる。
ドルーゼンそのものの治療法がないため、合併症(脈絡膜新生血管・GA)の早期発見が最重要である。
MNVはPhenotype 2, 3で特にリスクが高く、これらの表現型では観察間隔を短縮することを検討する。1)
若年患者(60歳以下)でもGAは9.2%に発生するため、年齢による油断は禁物である。1)
若年発症例(5〜30歳)ではMPGNやaHUSのスクリーニング検査も推奨される。
Q 治療法はあるのか?
A ドルーゼンそのものを消失させる治療法は現時点では存在しない。CNVが合併した場合は抗VEGF薬硝子体内注射や光動力学的療法(PDT)が適応となる。GAには確立された治療法がなく、継続的な経過観察が重要である。詳細は「標準的な治療法」の項 を参照。
基底層ドルーゼンは、RPE基底膜とブルッフ膜内膠原層の間に蓄積する多形性物質である。その構成成分は膜様残渣物・非エステル化コレステロール・補体などからなる。
形成メカニズム
RPEはリポ蛋白の排泄機能を担うが、加齢とともにその代謝回転が悪化する。変性した細胞外基質が蓄積し、ドルーゼンの基盤が形成される。CFH遺伝子変異(特にTyr402His)による補体カスケードの過剰活性化がこの過程を加速させる。1)
ドルーゼンのライフサイクル
Cuticular drusenは動的な存在であり、成長・癒合・退縮のサイクルを繰り返す。1)
成長・癒合期 :個々のドルーゼンが拡大し、隣接するドルーゼンと融合する退縮期 :RPEの異常が蓄積し、ドルーゼンが消退→RPE萎縮→地図状萎縮へと進行血管新生 :Bruch膜の破綻をきっかけに脈絡膜 からの新生血管 が侵入(CNV形成)
卵黄状病変の経過
卵黄状病変(vitelliform lesion)は以下の順序で進行する。1)
Vitelliform material形成
脈絡膜血管の過透過性亢進
RPE萎縮
脈絡膜菲薄化
Q なぜ若い人にも発症するのか?
A CFH遺伝子の稀なバリアント(p.Arg1210Cysなど)の保有者はより若年で発症する傾向がある。CFH遺伝子変異による補体代替経路の慢性的な過剰活性化が、通常のAMDより早期にドルーゼン形成を引き起こすと考えられている。1)
補体経路を標的とした治療
CFH遺伝子変異による補体代替経路の異常が病態基盤であることから、補体経路を標的とした化合物が活発に研究されている。全身投与は副作用リスクが高いため、局所(眼内)投与が有望なアプローチとして注目されている。
マルチモーダルイメージングによる予後予測
マルチモーダルイメージングの進歩により、合併症リスクの高い患者の早期同定が可能となりつつある。1) Phenotype分類(1〜3)は予後予測に有用であり、Phenotype 2, 3はGAおよびMNVの高リスク群として特に厳重な経過観察が求められる。1)
個別化医療の可能性
遺伝子解析の進歩により、CFH遺伝子をはじめとするAMD関連遺伝子のバリアントに基づいた個別化医療の実現が期待されている。特に稀なバリアント(p.Arg1210Cys等)の保有者では、早期スクリーニングや介入のターゲットとなりうる。
Fragiotta S, Fernandez-Avellaneda P, Breazzano MP, Scuderi G. Clinical manifestations of cuticular drusen: current perspectives. Clin Ophthalmol. 2021;15:3877-3887.
記事の全文をコピーして、お好みのAIに貼り付けて質問できます
下のAIを開いて、チャット欄に貼り付け(ペースト) してください