眼底検査
萎縮域:境界鮮明な低色素域。扇形(scalloped)の辺縁を持つ。
周囲所見:ドルーゼン・色素変化が病変周囲に認められる。
病変表現型:境界明瞭なRPEおよび/または脈絡膜毛細血管板の萎縮ゾーン2)。

アバシンカプタド ペゴル(Avacincaptad pegol; ACP)は、補体C5に結合するペグ化RNAアプタマーである。商品名はIZERVAY(アイザーヴェイ)。アステラス製薬が開発し、硝子体内注入液として提供される。2023年8月に米国FDAが加齢黄斑変性に続発する地図状萎縮(GA)の治療薬として承認した1)。GAに対する薬剤としては、補体C3/C3b阻害薬のペグセタコプラン(Syfovre)に次ぐ2番目の承認薬である2)。
GA(地図状萎縮)は加齢黄斑変性の進行型であり、網膜色素上皮(RPE)・視細胞・脈絡膜毛細血管板の萎縮による不可逆的な視力喪失を引き起こす1)。GAの世界有病率は約8.7%で、世界で約500万人(米国で100〜160万人)が罹患する1)。55歳以上の中心視力喪失の主要原因であり、75歳での有病率は3.5%、90歳以上では約22%に達する1)。米国における法的失明症例の約20%、英国では約26%がGA由来とされる3)。わが国では50歳以上の男女(男性:女性≒3:1)に発症し、変視・中心暗点に始まり、進行すると矯正視力0.1未満に至る。
補体C5を阻害するペグ化RNAアプタマーである。2023年にFDAが承認した地図状萎縮治療薬で、GA病変の拡大を遅らせるが、萎縮した組織を回復させたり視力を改善させたりする効果は現時点で示されていない。詳細は「標準的な治療法」の項を参照。
GAの主な自覚症状は以下の通りである1)。
GAは滲出型加齢黄斑変性よりも視力低下が緩徐であるが、長期的な視機能への影響は大きい2)。2年間で約75%の患眼が5文字喪失、約50%が10文字(3行)喪失、約25%が15文字(6行)喪失を経験する3)。GA進行はQOL(視覚関連・健康関連の双方)に悪影響を及ぼし、独立した生活や精神的健康の困難を伴う3)。うつ・不安の増加も報告されている4)。
2年間で約75%の眼が5文字(1行)、約50%が10文字(3行)、約25%が15文字(6行)の視力を失う3)。中心窩を侵す単一病変では視力低下リスクが高く、多発病変では拡大速度が速いが視力への影響は比較的緩徐である4)。
眼底検査
萎縮域:境界鮮明な低色素域。扇形(scalloped)の辺縁を持つ。
周囲所見:ドルーゼン・色素変化が病変周囲に認められる。
病変表現型:境界明瞭なRPEおよび/または脈絡膜毛細血管板の萎縮ゾーン2)。
FAF・OCT
眼底自発蛍光(FAF):リポフスチン欠如による濃い低自発蛍光。周囲の高自発蛍光パターンがGA拡大速度を予測する。
OCT(外層網膜):外顆粒層・エリプソイドゾーン(EZ)・インターディジテーションゾーン喪失、RPE喪失、脈絡膜への透過性亢進(choroidal hypertransmission)。EZ完全性が視力予後予測に有用4)。
GAは加齢黄斑変性の進行型であり、そのリスク因子は加齢黄斑変性全体のリスク因子と重なる。
非修正リスク因子:
修正リスク因子:
病態的背景:ドルーゼン蓄積が光受容体・RPE変性を誘発し萎縮へと進行する1)。補体系の異常活性化がGAの発症・進行に重要な役割を果たす1)3)。GAの前駆病変は、網膜色素上皮異常(色素ムラ・色素沈着・低色素)と軟性ドルーゼンである。
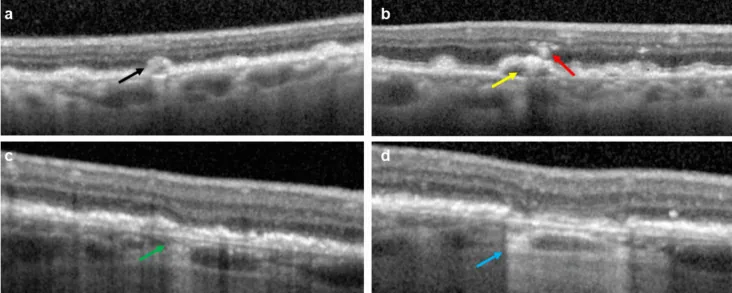
GAの診断にはマルチモーダルイメージングの組み合わせが推奨される2)。
各検査の特性を以下に示す。
| 検査法 | 主な目的 | 特記事項 |
|---|---|---|
| 眼底自発蛍光(FAF) | GA範囲の測定 | 標準的測定法。進行速度予測も可 |
| OCT(SD/SS) | 外層網膜・RPE評価 | EZ完全性で視力予後を予測4) |
| マイクロペリメトリー | 網膜感度の定量 | 残存機能の評価が可能4) |
ACPの投与法:2mg(20mg/mL溶液0.1mL)を月1回、硝子体内注射として投与する1)。
GATHER1(Phase 2/3)とGATHER2(Phase 3)の2つの無作為化二重盲検試験でACPの有効性が評価された。
| 試験 | GA拡大抑制率 | 統計 |
|---|---|---|
| GATHER1(12ヶ月、平方根変換) | 27.4%減少 | p=0.00727) |
| GATHER1(18ヶ月、観測値) | 32.2%減少 | 95%CI 0.480–1.8338) |
| GATHER2(12ヶ月、観測値) | 17.7%減少 | p=0.0041) |
Khananiら(2023)によるGATHER2の12ヶ月結果では、ACP群(n=271)対sham群(n=269)でGA成長率0.336対0.392 mm/年(差0.056 mm/年;95%CI 0.016–0.096;p=0.006)と有意な抑制が認められた6)。
GATHER2の24ヶ月データでは、月1回投与群で14%減少、12ヶ月後に月1回から隔月投与へ切り替えた群で19%減少を示した2)。
最高矯正視力に対する有意な改善は、GATHER1・GATHER2ともに示されていない1)2)。ただし事後解析では、15文字以上の最高矯正視力喪失がACP群4.0%に対しsham群7.6%、持続的な15文字喪失リスクは56%減少(HR 0.44;95%CI 0.21–0.92)と示唆された1)5)。
補体C3/C3b阻害薬のペグセタコプラン(Syfovre)はOAKS/DERBYのPhase 3試験で月1回投与において12ヶ月で21%(OAKS試験)のGA拡大抑制を示した2)。
主な副作用(GATHER1・GATHER2統合)を以下に示す1)。
| 副作用 | ACP群 | sham群 |
|---|---|---|
| 結膜下出血 | 13% | 9% |
| 眼圧上昇 | 9% | 1% |
| 霧視 | 8% | 5% |
| 黄斑新生血管転換 | 7% | 4% |
| 眼痛 | 4% | 3% |
眼内炎・虚血性視神経症は12ヶ月間で報告なし1)。眼圧上昇は注射手技に関連した一過性のものが主体である1)。
黄斑新生血管転換リスクについて、GATHER1ではACP 2mg群9.0%対sham群2.7%、GATHER2ではACP 2mg群6.7%対sham群4.1%であった1)。黄斑新生血管(脈絡膜新生血管)が発症した場合は抗VEGF治療による対応が必要である2)。
禁忌:眼・眼周囲感染症、活動性眼内炎症を有する患者。
GATHER試験では最高矯正視力の有意な改善は示されていない1)2)。ただし事後解析では、持続的な15文字以上の視力喪失リスクが56%減少(HR 0.44)することが示唆されており、長期的な視力維持への寄与が期待される5)。
GATHER試験の統合データでは治療群7%・sham群4%に黄斑新生血管転換が認められた2)。黄斑新生血管発症時は抗VEGF治療で対応する。定期的なOCTモニタリングが不可欠である。
GAの発症・進行には補体系の異常活性化が中心的役割を担う。
補体系は古典経路・レクチン経路・副経路の3経路から構成される1)。3経路はいずれもC3転換酵素によるC3切断(C3→C3a+C3b)で合流する1)。さらにC5転換酵素がC5をC5a(アナフィラトキシン)とC5bに切断する1)。
加齢に伴い補体系関連遺伝子の発現上方制御が増加する1)。CFH・CFB・C3・ARMS2の遺伝多型がGA感受性と関連する1)2)。
ACPは化学合成の一本鎖オリゴヌクレオチドであり、ペグ化により生体安定性の付与とクリアランスの遅延が図られている1)。
C5に高親和性で結合し、C5aとC5bへの切断を阻害する1)。
C5阻害の理論的利点:C5より上流のC3a(抗炎症・宿主防御機能を持つ)を温存しつつ、インフラマソーム動員とMAC形成を遮断する1)。C3阻害薬では上流からの感染防御機能が損なわれる可能性があるのに対し、C5阻害はより選択的な作用点とされる1)。
C5切断産物であるC5aとMACがRPEへの炎症傷害を介してGAを進行させると考えられている1)。C5を阻害することでMAC形成とC5a生成を防ぎ、かつ上流のC3aによる抗炎症・宿主防御機能を温存できる。C3阻害では感染リスク上昇の懸念があるため、C5はより安全な標的とされる1)。
GATHER2の24ヶ月データでは、月1回投与群で14%、12ヶ月後に隔月投与へ切り替えた群で19%のGA拡大抑制が示された2)。隔月投与への切り替えがGA抑制率を低下させない可能性が示唆されており、投与間隔の最適化が今後の課題である。
事後解析では持続的な15文字以上の視力喪失リスクの56%減少(HR 0.44)が示唆されたが、これは事後的・探索的な解析であり確定的な結論ではない1)5)。視力エンドポイントを主要評価項目とした前向き試験による検証が求められる。
EZ(エリプソイドゾーン)完全性のバイオマーカーとしての有用性が探索されている1)。機械学習によるOCTバイオマーカーからの視機能予測も研究が進んでいる4)。GA早期発見・早期治療介入の重要性が強調されており1)、これらのバイオマーカーが予後予測ツールとして確立されることが期待される。
補体阻害による黄斑新生血管(脈絡膜新生血管)発症リスク増加のメカニズム解明が残された重要な課題である1)。補体系が血管新生抑制にも関与しているとの仮説があり、そのバランスの解明が将来の薬剤設計に影響すると考えられる。